Clear Sky Science · nl
Chemische vangst van diazo-metabolieten onthult biosynthetische hydrazonoxidatie
Waarom instabiele moleculen voor ons belangrijk zijn
Schemici weten al lang dat sommige van de krachtigste geneesmiddelen en industriële reagentia ook de meest fragiele zijn. Ze vallen zo snel uiteen dat ze in de natuur vinden vergelijkbaar kan zijn met het proberen te vangen van zeepbellen in een storm. Deze studie pakt één dergelijke familie vluchtige moleculen aan, diazoverbindingen genaamd, die door microben worden gemaakt en zowel cellen kunnen beschadigen als nuttige chemische reacties kunnen aandrijven. Door een manier te bedenken om deze instabiele moleculen meteen te "vangen" zodra ze verschijnen, onthullen de onderzoekers nieuwe chemie in een menselijke longpathogeen en vinden ze een enzym dat een groene tool zou kunnen worden voor de productie van waardevolle reagentia.
Verborgen wapens van piepkleine microben
Micro-organismen zijn miniatuurfabriekjes voor chemie. Onder de vele verbindingen die ze maken bevinden zich natuurlijke producten met een diazogroep, die een paar stikstofatomen bevatten die klaarstaan om uiteen te springen en energie vrij te geven. Die reactiviteit stelt ze in staat biologische doelen aan te vallen, wat kan leiden tot antibioticum- en antikankeractiviteit, en maakt ze ook begeerde reagentia in synthetische chemielabs. Toch zijn er maar enkele tientallen natuurlijke diazoverbindingen bekend. De inventarisatie van genetische data door het team onthulde honderden microbiële genclusters die ernaar uitzagen dat ze diazomoleculen konden maken, verspreid over bodembacteriën, zeemicroben en pathogenen. De kloof tussen het genetische potentieel en het kleine aantal bekende verbindingen suggereerde dat veel diazo-moleculen onopgemerkt blijven, waarschijnlijk omdat ze te onstabiel zijn voor standaard ontdekkingstechnieken die vertrouwen op isolatie van stabiele, overvloedige producten.
Vluchtige moleculen vangen met een chemische haak
Om dit probleem op te lossen draaiden de onderzoekers de gebruikelijke zoekstrategie om. In plaats van te vragen of een microbe-extract kankercellen of bacteriën doodt, vroegen ze of de metabolieten een specifiek soort chemische reactiviteit delen. Ze ontwierpen een klein probenmolecuul gebaseerd op een gespannen ringvormig alkyne dat selectief en snel reageert met diazogroepen en zo een stabielere ring vormt, een pyrazool. Wanneer het wordt gemengd met microbiële bouillon werkt deze probe als een chemische haak: als een diazoverbinding aanwezig is, slaat de probe toe en zet die om in een zwaarder, gemakkelijker te detecteren product. Met gevoelige massaspectrometrie en vergelijkende metabolomica vergeleek het team monsters direct na toevoeging van de probe met monsters die een nacht waren geïncubeerd. Signalen die sterk groeiden in de tijd en het karakteristieke dubbele piekpatroon van de probeproducten toonden, wezen op verborgen diazo-metabolieten.
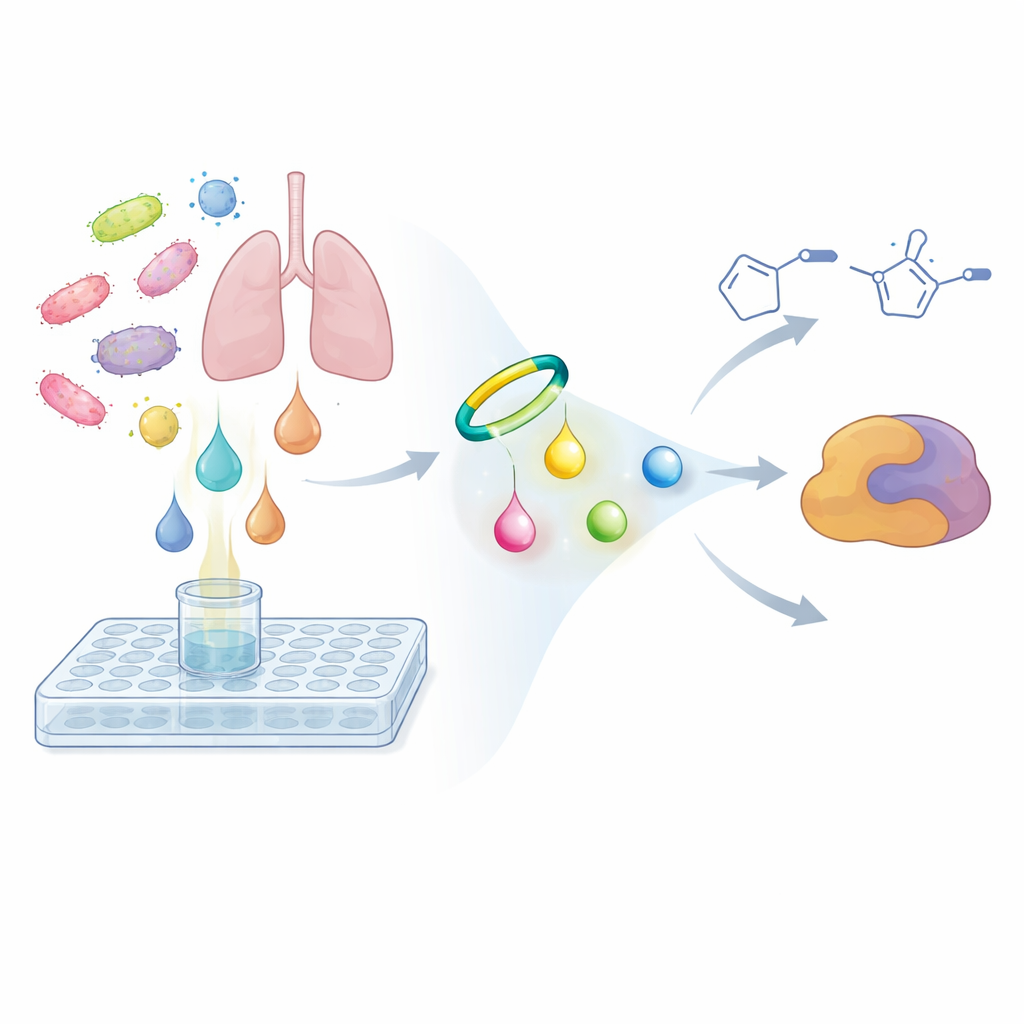
Nieuwe reactieve moleculen uit een longpathogeen
Screening van genetisch geselecteerde bacteriën met deze probe-gebaseerde werkwijze leidde het team naar de menselijke longpathogeen Nocardia ninae. In de kweekbouillon zagen ze twee paren probe-afgeleide producten die alleen na incubatie verschenen, de verwachte stikstofrijke samenstelling hadden en het gedrag lieten zien dat verwacht wordt voor gevangen diazoverbindingen. Door de bekende formule van de probe weg te rekenen en te redeneren over de overgebleven atomen, concludeerden ze dat de oorspronkelijke natuurlijke producten twee zeer eenvoudige maar eerder ongeziene moleculen waren: 4-diazo-3-oxoboterzuur (4-diazo-3-oxobutanoic acid) en diazoaceton. Dit zijn kleine bouwstenen vergeleken met veel natuurlijke producten, maar ze zijn zeer reactief. Controle-experimenten toonden aan dat de onbewerkte moleculen nagenoeg onzichtbaar waren voor routine-analyse, terwijl de probe-gelabelde versies gedetecteerd konden worden bij concentraties zo laag als enkele honderden delen per miljard, wat benadrukt hoe gemakkelijk dergelijke metabolieten gemist kunnen zijn.
Ontdekken van een ongebruikelijk enzymatisch pad
Het vinden van de moleculen was slechts de helft van het verhaal; de onderzoekers traceerden vervolgens hoe de bacterie ze produceert. Door het genoom te onderzoeken, identificeerden ze een gencluster, gedoopt dob, dat leek op bekende paden voor het opbouwen van stikstofrijke eenheden die hydrazonen heten, maar met extra enzymen die nieuwe stappen suggereerden. Door dit gencluster in een andere bacterie te introduceren en te tonen dat de gastheer dezelfde probe-gedetecteerde producten ging produceren, bevestigden ze de rol ervan. Gedetailleerde biochemische experimenten toonden een trap-voor-trap assemblagelijn: gewone aminozuren worden omgevormd tot een hydrazon-bevattend intermediair, dat wordt verlengd door een polyketide-synthase-enzym tot een klein hydrazonzuur. Een tweede enzym, een metalloenzym genaamd Dob3, voert vervolgens een zeldzame chemische prestatie uit: het oxideert het hydrazon tot een diazogroep. Deze reactie, hydrazonoxidatie genoemd, was voorgesteld maar nog niet rechtstreeks gedemonstreerd in de natuur.
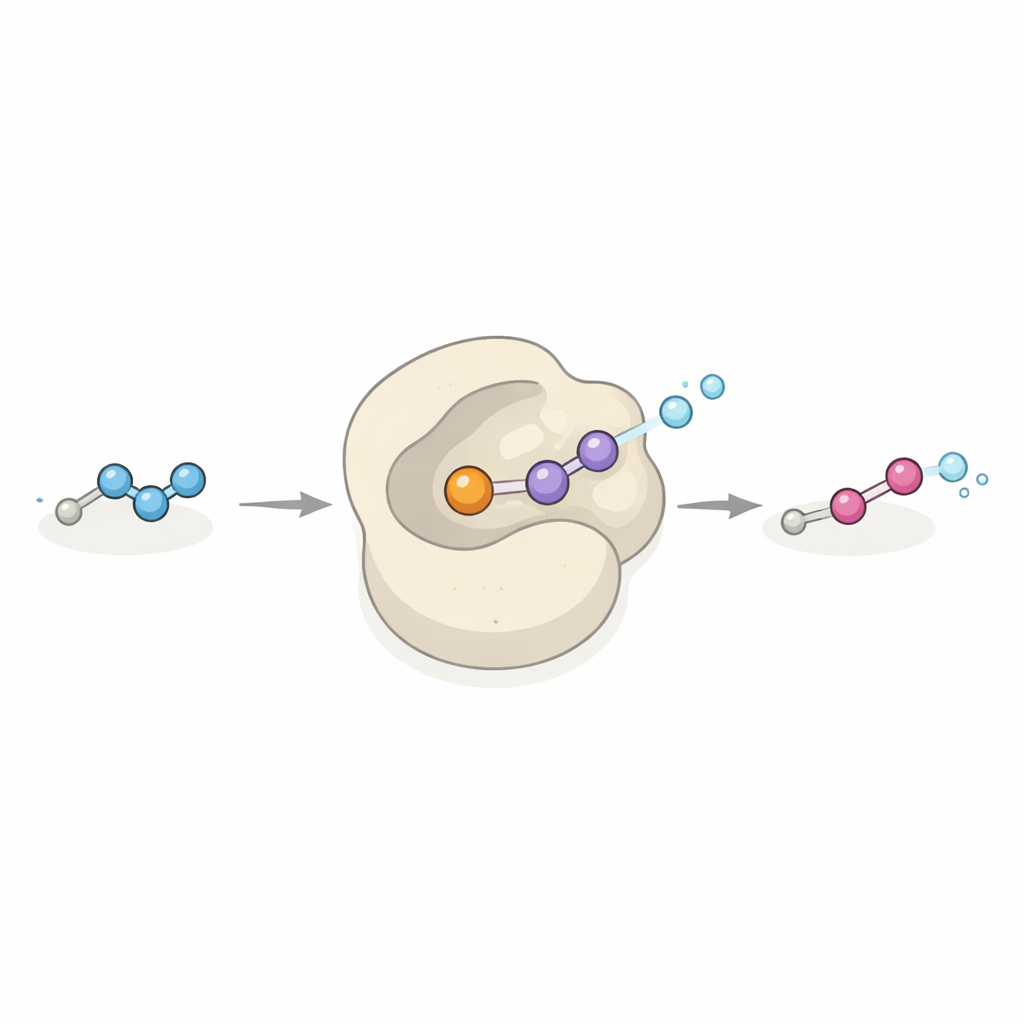
Een nieuw soort katalysator met industriële belofte
Dob3 behoort tot een familie van eiwitten die gewoonlijk zuurstofatomen toevoegen aan koolstof–waterstof- of stikstof–waterstofbindingen met behulp van een paar ijzeratomen en zuurstof uit de lucht. Hier breidt Dob3 dat repertoire uit door een relatief stabiel hydrazon om te zetten in een sterk geënergetiseerde diazogroep in een geconcerteerde twee-elektronen oxidatiestap. Het enzym accepteert in reageerbuistests een reeks verschillende hydrazonsubstraten en zet die om in de overeenkomstige diazoverbindingen. Omdat veel diazoreagentia hoekstenen zijn van de moderne synthetische chemie, vooral voor het vormen van koolstof–koolstofbindingen via zogeheten carbene-overdrachtreacties, zou Dob3 een veelzijdige "groene" katalysator kunnen worden om deze reagentia uit eenvoudige voorlopers te maken onder milde, milieuvriendelijke omstandigheden.
Wat dit werk voor de toekomst betekent
Voor niet-specialisten is de kernboodschap dat de chemie die binnen microben plaatsvindt rijker en delicaat is dan we tot nu toe konden zien. Door reactiviteit zelf als baken te gebruiken—instabiele moleculen te vangen op het moment dat ze worden gemaakt—onthult deze studie nieuwe diazoverbindingen in een menselijke pathogeen en vestigt ze onomstotelijk hydrazonoxidatie als een natuurlijke route naar deze reactieve groepen. De ontdekking van Dob3, een di-ijzer enzym dat deze uitdagende transformatie uitvoert, opent deuren naar het ontwerpen van microben om industriële diazoreagentia duurzaam te produceren. In bredere zin suggereert het werk dat veel reactieve natuurlijke producten nog deel uitmaken van een microbiële „donkere materie” van chemie, wachtend om ontdekt te worden met vergelijkbaar slimme, reactiviteitsgédrijfde zoekstrategieën.
Bronvermelding: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Trefwoorden: diazo-natuurlijke producten, reactiviteitsgebaseerde screening, microbiële metabolieten, biokatalyse, enzymontdekking