Clear Sky Science · ja
ジアゾ代謝物の化学的捕捉が生合成的ヒドラゾン酸化を明らかにする
不安定な分子が私たちにとって重要な理由
化学者は長年、最も強力な医薬品や工業用試薬の中に、同時に最も壊れやすいものが含まれていることを知ってきました。あまりに迅速に分解するため、自然界でそれらを見つけることは嵐の中でシャボン玉を捕まえるようなものです。本研究は、微生物によって作られ、細胞を損なう一方で有用な化学反応を引き起こすジアゾ化合物と呼ばれる、一群の短命な分子に取り組んでいます。この不安定な分子を出現と同時に「捕まえる」方法を考案することで、研究者たちはヒトの肺病原体内で新たな化学反応を明らかにし、価値ある試薬の製造に使えるグリーンな酵素を明らかにしました。
小さな微生物が持つ隠れた武器
微生物は小さな化学工場です。彼らが作る多くの化合物の中には、ジアゾ基を含む天然物があり、二つの窒素原子がすぐに分離してエネルギーを放出する準備ができています。その反応性によって生物学的標的を攻撃し、抗生物質や抗がん活性を示すことがあり、一方で合成化学の研究室では貴重な試薬として評価されます。しかし、既知の天然ジアゾ化合物はほんの数十種にとどまります。研究チームが遺伝情報を調査したところ、土壌細菌や海洋微生物、病原体に散在する、ジアゾ分子を作れると思われる何百もの遺伝子クラスターが見つかりました。遺伝的な潜在能力と知られている化合物数の間に矛盾があることは、多くのジアゾ分子が未発見のままであり、その理由は標準的な発見法が安定で豊富な生成物の単離に依存しているため、不安定すぎて見逃されている可能性が高いことを示唆します。
化学的フックで短命分子を捕まえる
この問題を解決するために、研究者たちは従来の探索戦略を逆転させました。微生物の抽出物ががん細胞や細菌を殺すかどうかを問う代わりに、その代謝物が特定の化学的反応性を共有するかどうかを問いました。彼らは歪んだ環状アルキンに基づく小さなプローブ分子を設計し、これはジアゾ基と選択的かつ迅速に反応してピラゾールと呼ばれるより安定な環を形成します。微生物の培地と混ぜると、このプローブは化学的なフックのように働き、ジアゾ化合物が存在すればプローブが結合してより重く、検出しやすい生成物に変換します。高感度な質量分析と比較代謝解析を用いて、チームはプローブ添加直後のサンプルと一晩インキュベートしたサンプルを比較しました。時間とともに強く増加し、プローブ生成物に特徴的な二重ピークパターンを示す信号が、隠れたジアゾ代謝物の存在を示しました。
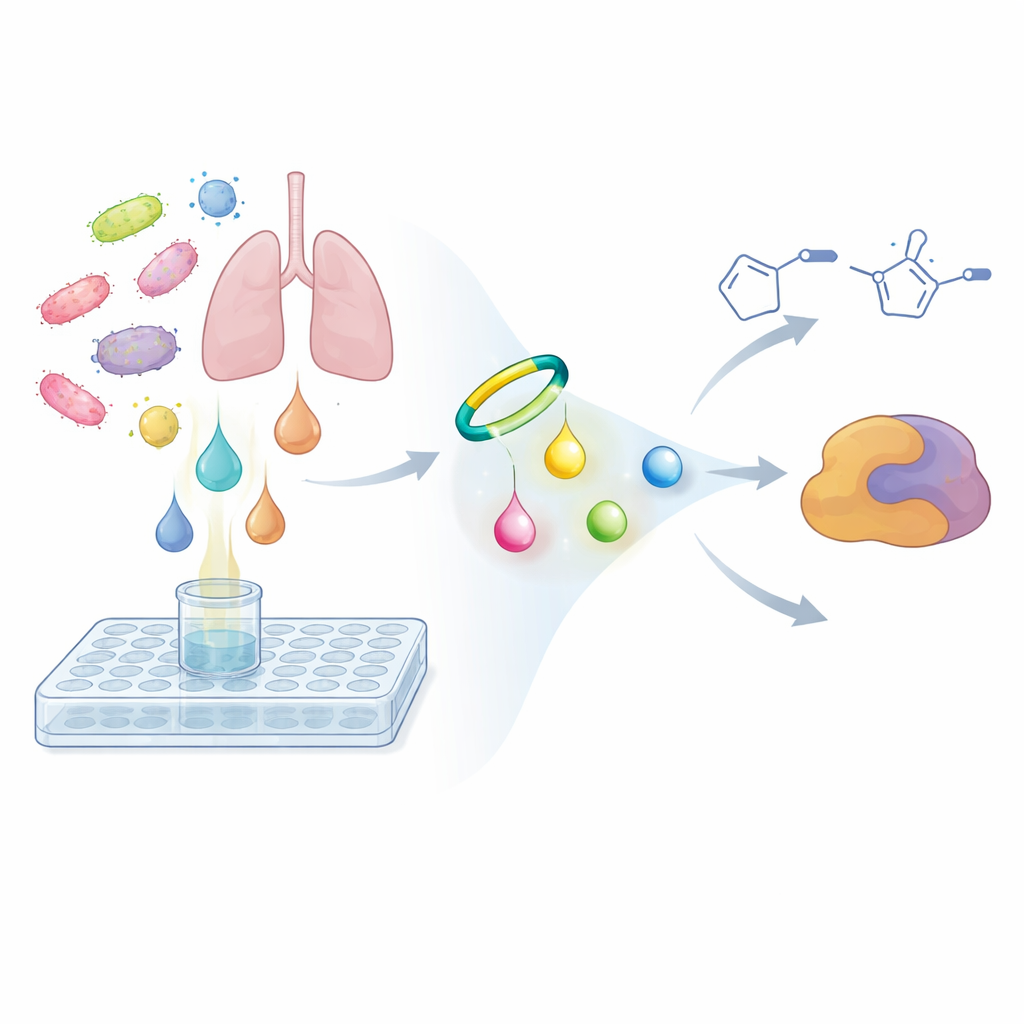
肺病原体から見つかった新しい反応性分子
遺伝的に選択した細菌をこのプローブベースのワークフローでスクリーニングしたところ、研究者たちはヒトの肺病原体であるNocardia ninaeに行き当たりました。その培養液中で、インキュベーション後にのみ現れ、期待される窒素に富む組成を持ち、捕捉されたジアゾ化合物としての振る舞いに一致するプローブ由来の生成物の対が二組観察されました。プローブの既知の組成を差し引き、残りの原子から推論することで、元の天然物はこれまで見られていなかった非常に単純な二つの分子、すなわち4-ジアゾ-3-オキソ酪酸とジアゾアセトンであったと推定しました。これらは多くの天然物と比べれば小さな構成要素ですが非常に反応性が高いことが分かりました。対照実験により、未修飾の分子は通常の分析ではほとんど見えない一方で、プローブで標識されたバージョンは数百ppb(10億分の数百)という濃度で検出可能であり、このような代謝物がいかに見逃されやすかったかが強調されました。
異例の酵素経路の発見
分子を見つけることは物語の半分に過ぎません。研究者たちは次に、その細菌がそれらをどのように作るかを追跡しました。ゲノムを調べることで、彼らはdobと名付けられた遺伝子クラスターを特定しました。これはヒドラゾンを含む窒素リッチな単位を構築する既知の経路に似ている一方で、新たな段階を示唆する余分な酵素を含んでいました。この遺伝子クラスターを別の細菌に導入し、宿主が同じプローブ検出生成物を産生し始めたことを示すことで、その役割が確認されました。詳細な生化学的実験により、一連の段階的な組み立てラインが明らかになりました:一般的なアミノ酸がヒドラゾンを持つ中間体に再構成され、それがポリケチド合成酵素によって延長されて小さなヒドラゾン酸が形成されます。二つ目の酵素である金属酵素Dob3は、稀な化学的所作を行います。すなわちヒドラゾンを酸化してジアゾ基に変換するのです。この反応(ヒドラゾン酸化)はこれまで提案されてはいたものの、自然界で直接的に実証されたことはありませんでした。
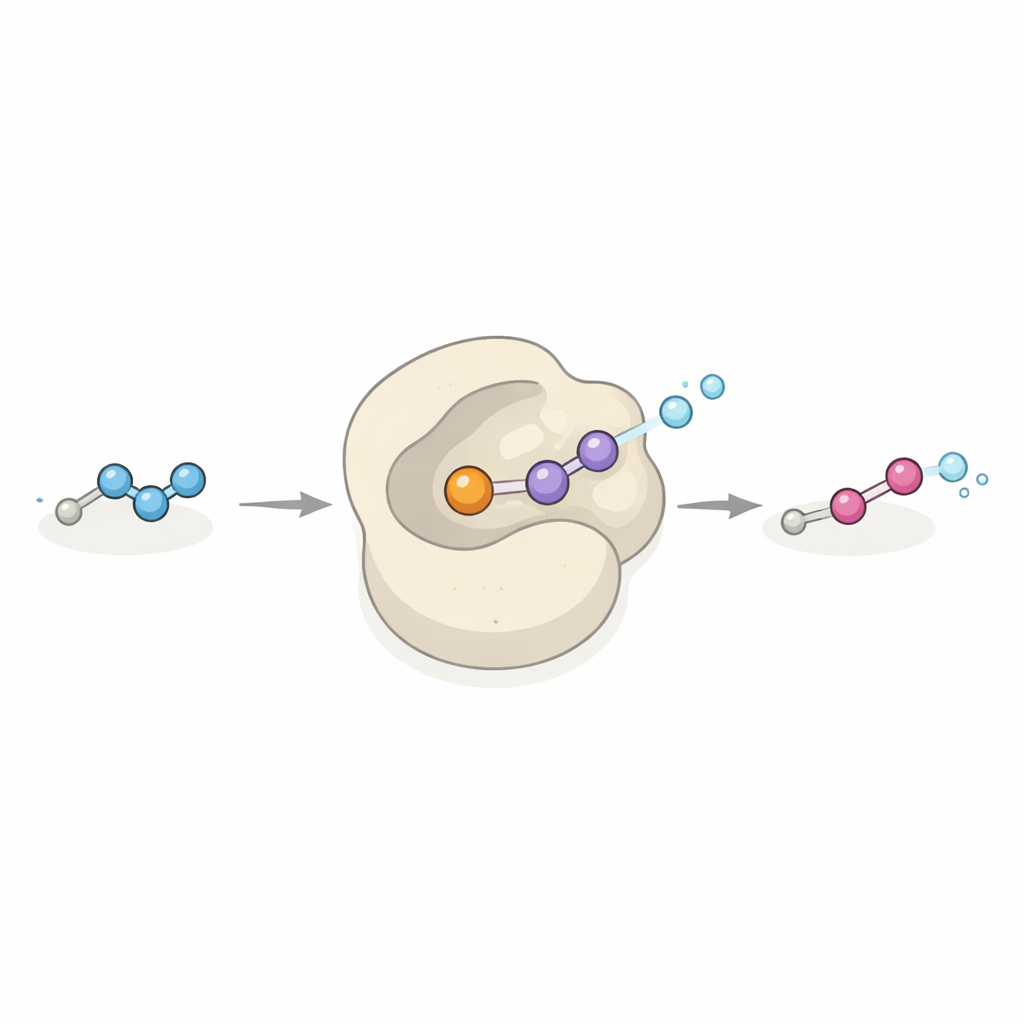
工業的な可能性を秘めた新しいタイプの触媒
Dob3は通常、二つの鉄原子と大気中の酸素を使って炭素–水素結合や窒素–水素結合に酸素原子を付加するタンパク質族に属します。ここでDob3はその手法を拡張し、比較的安定なヒドラゾンを高度に励起したジアゾ基へと、協奏的な2電子酸化ステップで変換します。試験管内実験では、この酵素はさまざまなヒドラゾン基質を受け入れ、それらを対応するジアゾ化合物へと変換しました。多くのジアゾ試薬は現代合成化学、特にカルベン移動反応を介した炭素–炭素結合形成の基盤であるため、Dob3は単純な前駆体から穏やかで環境に優しい条件でこれらの試薬を作るための多用途な“グリーン”触媒になる可能性があります。
今後の意義
専門外の読者にとっての主要なメッセージは、微生物内部で起きている化学は、私たちがこれまで観察してきたよりも豊かで繊細であるということです。反応性そのものを指標として用い——生成された瞬間に不安定な分子を捕まえることで——本研究はヒト病原体内の新しいジアゾ化合物を明らかにし、ヒドラゾン酸化がこれらの反応性基へ到達する自然な経路であることを確実に示しました。困難な変換を行う二鉄酵素Dob3の発見は、産業用ジアゾ試薬を持続可能に生産するために微生物を設計する道を開きます。より広く見れば、本研究は多くの反応性天然物が“微生物化学のダークマター”として存在し、同様に巧妙な反応性指向の探索戦略によって発見されるのを待っていることを示唆しています。
引用: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
キーワード: ジアゾ天然物, 反応性に基づくスクリーニング, 微生物代謝物, バイオ触媒, 酵素発見