Clear Sky Science · de
Chemische Erfassung von Diazo-Metaboliten enthüllt biosynthetische Hydrazon‑Oxidation
Warum instabile Moleküle für uns wichtig sind
Chemiker wissen seit langem, dass einige der wirksamsten Medikamente und industriellen Reagenzien auch zu den empfindlichsten Verbindungen gehören. Sie zerfallen so schnell, dass man sie in der Natur zu finden mit dem Versuch vergleichbar ist, Seifenblasen in einem Sturm zu fangen. Diese Studie widmet sich einer solchen Familie flüchtiger Moleküle, den Diazoverbindungen, die von Mikroben gebildet werden und sowohl Zellen schädigen als auch nützliche chemische Reaktionen antreiben können. Indem die Forschenden eine Methode entwickeln, diese instabilen Moleküle sofort nach ihrem Entstehen „einzufangen“, decken sie neue Chemie in einem menschlichen Lungenpathogen auf und identifizieren ein Enzym, das zu einem umweltfreundlichen Werkzeug für die Herstellung wertvoller Reagenzien werden könnte.
Versteckte Waffen winziger Mikroben
Mikroorganismen sind winzige chemische Fabriken. Zu den vielen Verbindungen, die sie produzieren, gehören natürliche Produkte mit Diazogruppen, die ein Paar Stickstoffatome tragen, das darauf wartet, auseinanderzuspringen und Energie freizusetzen. Diese Reaktivität ermöglicht es ihnen, biologische Ziele anzugreifen und verleiht ihnen antibiotische und antitumorale Eigenschaften; gleichzeitig machen sie sie zu begehrten Reagenzien in der synthetischen Chemie. Dennoch sind nur einige Dutzend natürliche Diazoverbindungen bekannt. Die genomweite Untersuchung des Teams förderte Hunderte mikrobieller Gencluster zutage, die offenbar zur Bildung von Diazo-Molekülen fähig sind, verteilt in Bodenbakterien, Meeresmikroben und Krankheitserregern. Die Diskrepanz zwischen dem genetischen Potenzial und der geringen Zahl bekannter Verbindungen deutete darauf hin, dass viele Diazo-Moleküle unentdeckt bleiben, vermutlich weil sie zu instabil für übliche Entdeckungsmethoden sind, die auf der Isolierung stabiler, reichlich vorhandener Produkte beruhen.
Flüchtige Moleküle mit einem chemischen Haken fangen
Um dieses Problem zu lösen, kehrten die Forschenden die übliche Suchstrategie um. Statt zu prüfen, ob Extrakte eines Mikrobenwachstums Krebszellen oder Bakterien abtöten, fragten sie, ob dessen Metaboliten eine bestimmte Form chemischer Reaktivität teilen. Sie entwickelten eine kleine Sondenmolekül, das auf einem gespanntem, ringförmigen Alkin basiert und selektiv sowie schnell mit Diazogruppen reagiert und dabei einen stabileren Ring, ein Pyrazol, bildet. Wenn dieses Probe mit mikrobieller Brühe gemischt wird, wirkt es wie ein chemischer Haken: Ist ein Diazoverbindung vorhanden, bindet die Sonde sie und wandelt sie in ein schwereres, leichter nachweisbares Produkt um. Mithilfe empfindlicher Massenspektrometrie und vergleichender Metabolomik verglich das Team Proben, die unmittelbar nach Zugabe der Sonde entnommen wurden, mit Proben, die über Nacht inkubiert wurden. Signale, die über die Zeit stark zunahmen und das charakteristische Doppelspitzenmuster der Sondenprodukte zeigten, markierten verborgene Diazo‑Metaboliten.
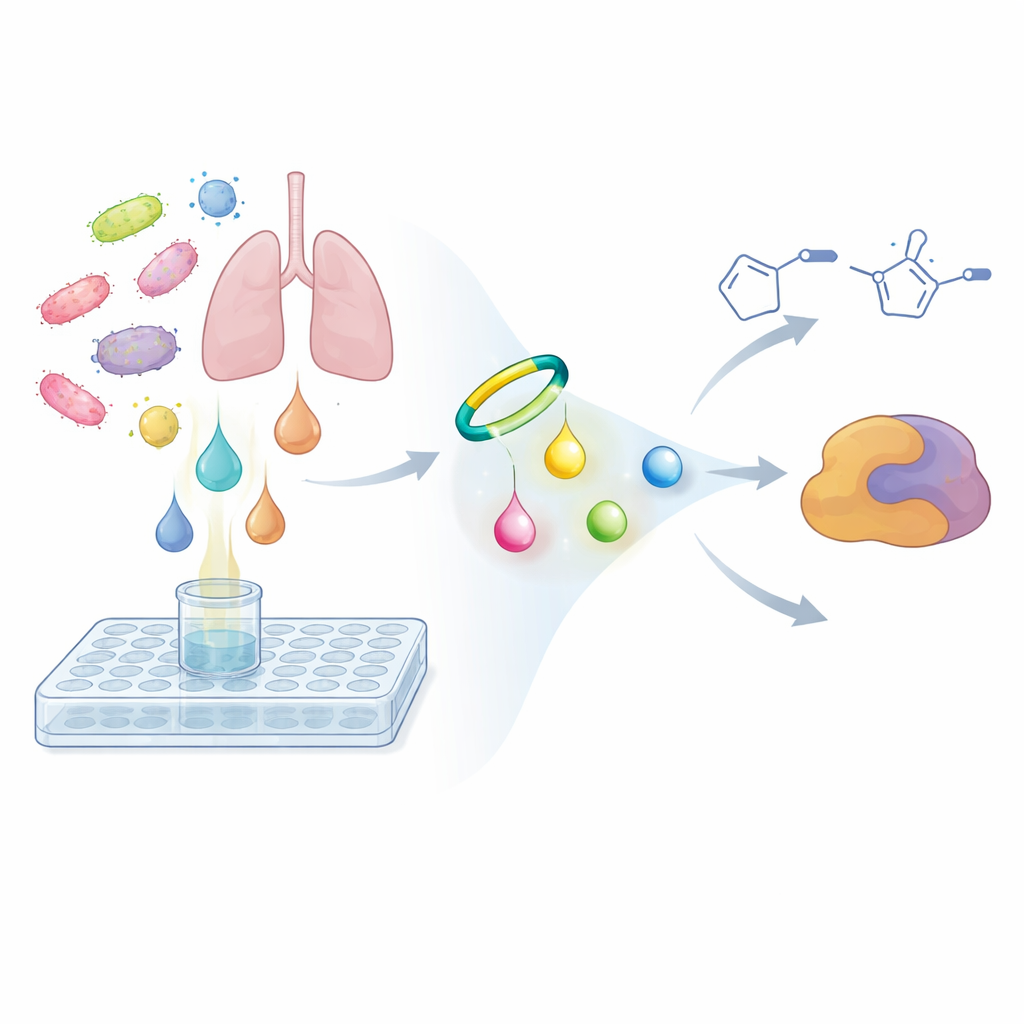
Neue reaktive Moleküle aus einem Lungenpathogen
Die Untersuchung genetisch ausgewählter Bakterien mit diesem sondengestützten Workflow führte das Team zu dem menschlichen Lungenpathogen Nocardia ninae. In dessen Kulturbrühe beobachteten sie zwei Paare von sondenabgeleiteten Produkten, die erst nach Inkubation auftraten, die erwartete stickstoffreiche Zusammensetzung hatten und sich wie eingefangene Diazoverbindungen verhielten. Durch Subtraktion der bekannten Formel der Sonde und Analyse der verbleibenden Atome schlossen sie, dass die ursprünglichen Naturstoffe zwei sehr einfache, zuvor unbekannte Moleküle waren: 4‑Diazo‑3‑oxobuttersäure und Diazacetone. Diese sind im Vergleich zu vielen Naturstoffen kleine Bausteine, aber hochreaktiv. Kontrollversuche zeigten, dass die unveränderten Moleküle für Routineanalysen de facto unsichtbar sind, während die sondenmarkierten Varianten in Konzentrationen von nur wenigen Hundert Teilen pro Milliarde nachweisbar waren — ein Hinweis darauf, wie leicht solche Metaboliten übersehen werden können.
Aufdeckung eines ungewöhnlichen Enzymwegs
Die Identifizierung der Moleküle war nur die halbe Geschichte; anschließend verfolgten die Forschenden nach, wie das Bakterium sie synthetisiert. Durch Analyse seines Genoms lokalisierten sie einen Gencluster, den sie dob tauften, der bekannten Wegen zur Bildung stickstoffreicher Einheiten, sogenannter Hydrazone, ähnelte, jedoch zusätzliche Enzyme enthielt, die neue Schritte andeuteten. Durch Übertragung dieses Genclusters in ein anderes Bakterium und den Nachweis, dass der Wirtsorganismus daraufhin dieselben sondenerfassten Produkte produzierte, bestätigten sie dessen Funktion. Detaillierte biochemische Experimente zeigten eine schrittweise Produktionslinie: Allgemeine Aminosäuren werden zu einem hydrazonhaltigen Zwischenprodukt umgebaut, das durch eine Polyketidsynthase erweitert wird, um eine kleine Hydrazonsäure zu bilden. Ein zweites Enzym, ein Metalloenzym namens Dob3, vollzieht dann eine seltene chemische Leistung: Es oxidiert das Hydrazon zur Diazogruppe. Diese Reaktion, die Hydrazon‑Oxidation genannt wird, war vorgeschlagen worden, aber zuvor nicht direkt in der Natur nachgewiesen.
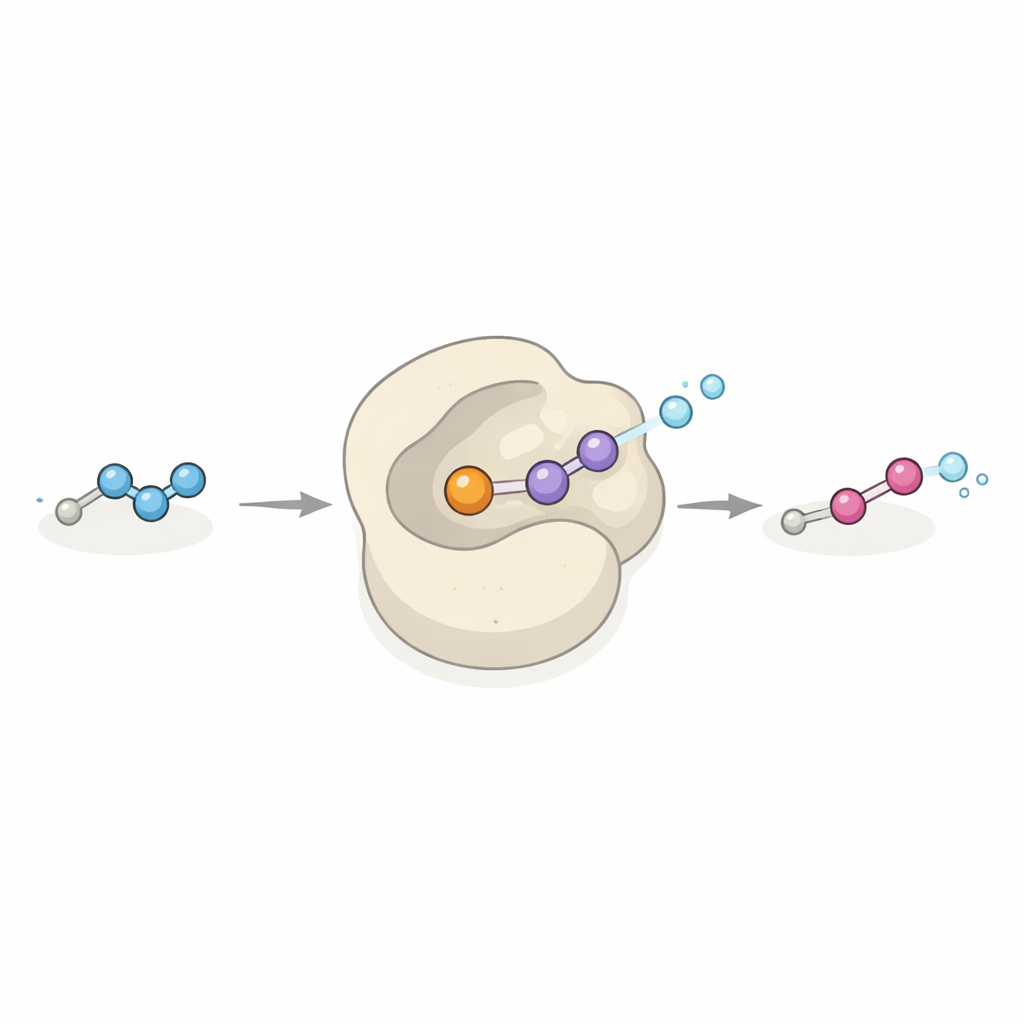
Eine neue Art von Katalysator mit industriellem Potenzial
Dob3 gehört zu einer Proteinfamilie, die üblicherweise Sauerstoffatome an C–H‑ oder N–H‑Bindungen einfügt, mithilfe eines Paars Eisenatome und Sauerstoff aus der Luft. Hier erweitert Dob3 dieses Repertoire, indem es ein relativ stabiles Hydrazon in einem konzertierten Zwei‑Elektronen‑Oxidationsschritt in eine hochenergetische Diazogruppe überführt. Das Enzym akzeptiert in Reagenzglasversuchen eine Reihe unterschiedlicher Hydrazonsubstrate und wandelt sie in die entsprechenden Diazoverbindungen um. Da viele Diazoreagenzien Grundbausteine der modernen synthetischen Chemie sind, insbesondere für die Bildung von C–C‑Bindungen durch sogenannte Carbene‑Transfer‑Reaktionen, könnte Dob3 zu einem vielseitigen „grünen“ Katalysator werden, der diese Reagenzien aus einfachen Vorläufern unter milden, umweltfreundlichen Bedingungen herstellt.
Was diese Arbeit für die Zukunft bedeutet
Für Nicht‑Fachleute ist die zentrale Botschaft, dass die Chemie in Mikroben reicher und zugleich zarter ist, als wir bisher sehen konnten. Indem Reaktivität selbst als Leitsignal genutzt wird — und instabile Moleküle in dem Moment eingefangen werden, in dem sie entstehen — zeigt diese Studie neue Diazoverbindungen in einem humanen Pathogen auf und etabliert die Hydrazon‑Oxidation als natürlichen Weg zu diesen reaktiven Gruppen. Die Entdeckung von Dob3, einem Di‑Eisen‑Enzym, das diese anspruchsvolle Umwandlung durchführt, eröffnet Möglichkeiten, Mikroben so zu konstruieren, dass sie industrielle Diazoreagenzien nachhaltig produzieren. Allgemeiner legt die Arbeit nahe, dass viele reaktive Naturstoffe Teil einer mikrobiellen „Dunkelmaterie“ der Chemie sind, die darauf wartet, mit ähnlich raffinierten, reaktivitätsgesteuerten Suchstrategien aufgedeckt zu werden.
Zitation: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Schlüsselwörter: diazo Naturstoffe, reaktivitätsbasierte Suche, mikrobielle Metaboliten, Biokatalyse, Enzymentdeckung