Clear Sky Science · fr
Capture chimique des métabolites diazo révèle l’oxydation biosynthétique des hydrazones
Pourquoi les molécules instables comptent pour nous
Les chimistes savent depuis longtemps que certains des médicaments et réactifs industriels les plus puissants sont aussi les plus fragiles. Ils se décomposent si rapidement que les trouver dans la nature peut revenir à essayer d’attraper des bulles de savon dans une tempête. Cette étude s’attaque à une famille de molécules éphémères, les composés diazo, produits par des microbes et capables à la fois d’endommager des cellules et de catalyser des réactions chimiques utiles. En inventant une façon de « capturer » ces molécules instables dès leur apparition, les chercheurs mettent au jour une nouvelle chimie dans un agent pathogène pulmonaire humain et identifient une enzyme qui pourrait devenir un outil écologique pour la fabrication de réactifs de valeur.
Armes cachées chez de minuscules microbes
Les micro-organismes sont de minuscules usines chimiques. Parmi les nombreux composés qu’ils produisent figurent des produits naturels contenant un groupe diazo, qui porte une paire d’atomes d’azote prêts à se rompre et à libérer de l’énergie. Cette réactivité leur permet d’attaquer des cibles biologiques, conférant des activités antibiotiques et anticancéreuses, et en fait aussi des réactifs prisés dans les laboratoires de chimie synthétique. Pourtant, seuls quelques dizaines de composés diazo naturels sont connus. L’analyse des données génétiques par l’équipe a révélé des centaines de clusters géniques microbiens susceptibles de produire des molécules diazo, répartis dans des bactéries du sol, des microbes marins et des agents pathogènes. Le décalage entre ce potentiel génétique et le faible nombre de composés identifiés suggère que de nombreuses molécules diazo restent invisibles, probablement parce qu’elles sont trop instables pour les méthodes de découverte standard qui reposent sur l’isolement de produits stables et abondants.
Attraper des molécules fugitives avec un hameçon chimique
Pour résoudre ce problème, les chercheurs ont renversé la stratégie de recherche habituelle. Plutôt que de demander si les extraits d’un microbe tuent des cellules cancéreuses ou des bactéries, ils ont interrogé si ses métabolites partagent un type spécifique de réactivité chimique. Ils ont conçu une petite molécule-sonde basée sur un alcyne cyclique contraint qui réagit sélectivement et rapidement avec les groupes diazo, formant un anneau plus stable appelé pyrazole. Lorsqu’on la mélange au bouillon microbien, cette sonde agit comme un hameçon chimique : si un composé diazo est présent, la sonde s’y fixe et le convertit en un produit plus lourd et plus facilement détectable. En utilisant la spectrométrie de masse sensible et la métabolomique comparative, l’équipe a comparé des échantillons pris immédiatement après l’ajout de la sonde avec des échantillons incubés toute la nuit. Les signaux qui augmentaient fortement avec le temps et présentaient le motif caractéristique de double pic des produits sondés indiquaient la présence de métabolites diazo cachés.
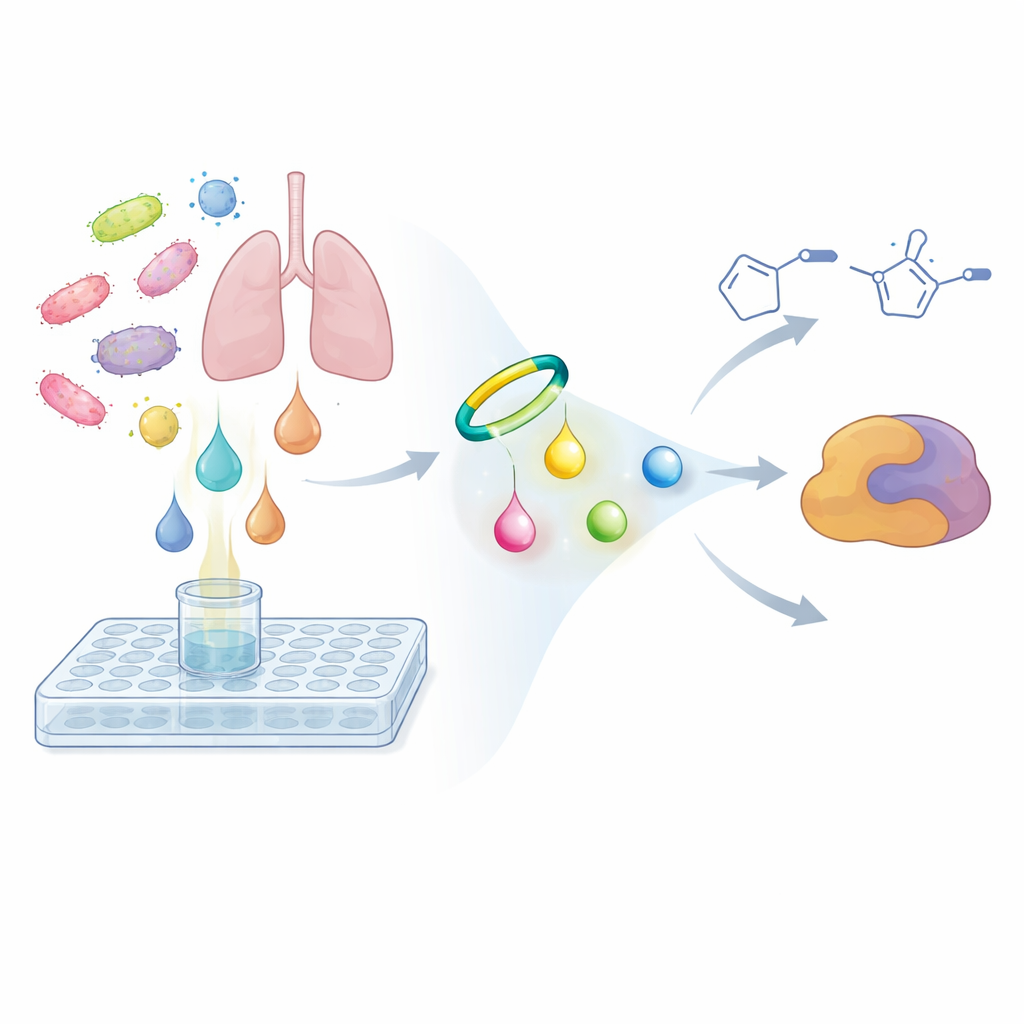
Nouvelles molécules réactives chez un pathogène pulmonaire
Le criblage de bactéries sélectionnées génétiquement avec ce protocole fondé sur une sonde a mené l’équipe vers l’agent pathogène pulmonaire humain Nocardia ninae. Dans son bouillon de culture, ils ont observé deux paires de produits dérivés de la sonde n’apparaissant qu’après incubation, ayant la composition riche en azote attendue et se comportant comme des composés diazo capturés. En soustrayant la formule connue de la sonde et en déduisant les atomes restants, ils ont conclu que les produits naturels originaux étaient deux molécules très simples mais inédites : l’acide 4-diazo-3-oxobutanoïque et la diazoacétone. Ce sont de minuscules blocs de construction comparés à de nombreux produits naturels, mais ils sont hautement réactifs. Des expériences témoins ont montré que les molécules non modifiées étaient essentiellement invisibles à l’analyse de routine, tandis que les versions marquées par la sonde pouvaient être détectées à des concentrations aussi faibles que quelques centaines de parties par milliard, soulignant combien ces métabolites pouvaient facilement avoir été manqués.
Mise au jour d’une voie enzymatique inhabituelle
La découverte des molécules n’était que la moitié de l’histoire ; les chercheurs ont ensuite retracé leur biosynthèse. En examinant le génome de la bactérie, ils ont identifié un cluster de gènes, nommé dob, qui ressemblait à des voies connues pour assembler des unités riches en azote appelées hydrazones, mais avec des enzymes supplémentaires suggérant des étapes nouvelles. En transférant ce cluster génique dans une autre bactérie et en montrant que l’hôte commençait à produire les mêmes produits détectés par la sonde, ils ont confirmé son rôle. Des expériences biochimiques détaillées ont révélé une chaîne d’assemblage étape par étape : des acides aminés courants sont transformés en un intermédiaire portant une hydrazone, qui est allongé par une enzyme synthase polykétidique pour former un petit acide hydrazone. Une seconde enzyme, une métalloprotéine nommée Dob3, accomplit alors une prouesse chimique rare : elle oxyde l’hydrazone en un groupe diazo. Cette réaction, appelée oxydation d’hydrazone, avait été proposée mais non démontrée directement dans la nature.
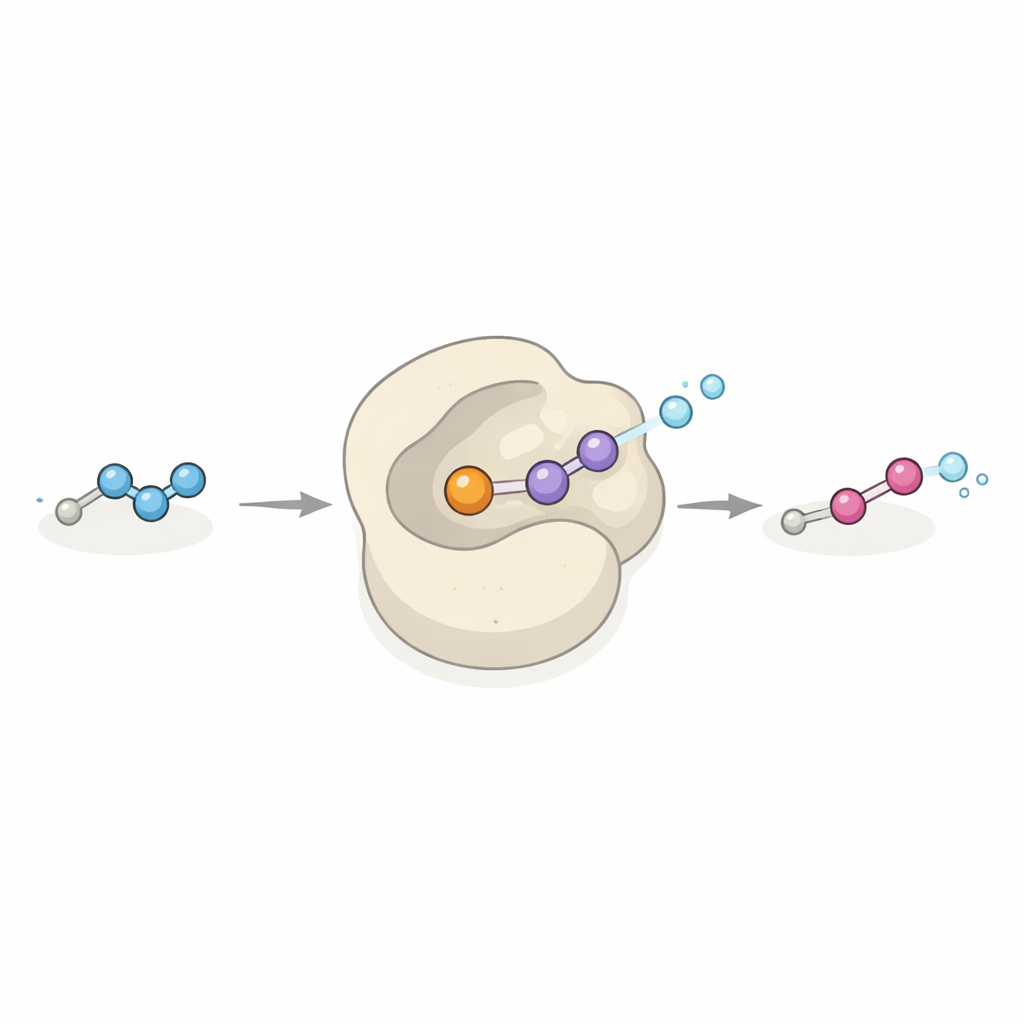
Un nouveau type de catalyseur au potentiel industriel
Dob3 appartient à une famille de protéines qui ajoutent habituellement des atomes d’oxygène aux liaisons carbone–hydrogène ou azote–hydrogène en utilisant une paire d’atomes de fer et l’oxygène de l’air. Ici, Dob3 étend ce répertoire en transformant une hydrazone relativement stable en un groupe diazo hautement énergisé via une étape d’oxydation concertée à deux électrons. L’enzyme accepte une gamme de substrats hydrazones différents dans des expériences en éprouvette, les convertissant en leurs composés diazo correspondants. Parce que de nombreux réactifs diazo sont des piliers de la chimie synthétique moderne, notamment pour la formation de liaisons carbone–carbone via les réactions de transfert de carbène, Dob3 pourrait devenir un catalyseur « vert » polyvalent pour produire ces réactifs à partir de précurseurs simples sous des conditions douces et respectueuses de l’environnement.
Ce que signifie ce travail pour l’avenir
Pour les non-spécialistes, le message clé est que la chimie qui se déroule à l’intérieur des microbes est à la fois plus riche et plus délicate que ce que nous pouvions observer. En utilisant la réactivité elle-même comme balise — en capturant les molécules instables au moment même de leur formation — cette étude révèle de nouveaux composés diazo au sein d’un agent pathogène humain et établit de façon convaincante l’oxydation d’hydrazone comme voie naturelle vers ces groupes réactifs. La découverte de Dob3, une enzyme di-ferro accomplissant cette transformation exigeante, ouvre la voie à l’ingénierie de microbes pour produire durablement des réactifs diazo industriels. Plus largement, le travail suggère que de nombreux produits naturels réactifs font encore partie d’une « matière noire » chimique microbienne, en attente d’être révélés par des stratégies de recherche astucieuses guidées par la réactivité.
Citation: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Mots-clés: produits naturels diazo, dépistage basé sur la réactivité, métabolites microbiens, biocatalyse, découverte d’enzymes