Clear Sky Science · es
Captura química de metabolitos diazo revela la oxidación biosintética de hidrazonas
Por qué nos importan las moléculas inestables
Los químicos saben desde hace tiempo que algunos de los fármacos y reactivos industriales más potentes son también los más frágiles. Se descomponen tan rápido que encontrarlos en la naturaleza puede ser como intentar atrapar pompas de jabón en plena tormenta. Este estudio aborda una de esas familias de moléculas efímeras, llamadas compuestos diazo, que producen los microbios y que pueden tanto dañar células como impulsar reacciones químicas útiles. Al inventar una forma de “atrapar” estas moléculas inestables en el momento en que aparecen, los investigadores descubren nueva química en un patógeno pulmonar humano y revelan una enzima que podría convertirse en una herramienta ecológica para fabricar reactivos valiosos.
Armas ocultas de microbios minúsculos
Los microorganismos son pequeñas fábricas químicas. Entre los muchos compuestos que producen están los productos naturales que contienen diazo, que llevan un par de átomos de nitrógeno listos para separarse y liberar energía. Esa reactividad les permite atacar objetivos biológicos, dando lugar a actividad antibiótica y anticancerígena, y también los convierte en reactivos preciados en laboratorios de síntesis. Sin embargo, solo se conocen unas pocas docenas de compuestos diazo naturales. La revisión de datos genéticos del equipo descubrió cientos de cúmulos genéticos microbianos con apariencia de poder sintetizar diazo, distribuidos entre bacterias del suelo, microbios marinos y patógenos. La discrepancia entre el potencial genético y el reducido número de compuestos conocidos sugiere que muchos diazo permanecen ocultos, probablemente porque son demasiado inestables para los métodos de descubrimiento estándar, que dependen de aislar productos estables y abundantes.
Atrapar moléculas fugaces con un anzuelo químico
Para resolver este problema, los investigadores invirtieron la estrategia habitual de búsqueda. En lugar de preguntar si los extractos microbianos matan células cancerosas o bacterias, preguntaron si sus metabolitos comparten un tipo específico de reactividad química. Diseñaron una pequeña molécula sonda basada en un alquino en anillo forzado que reacciona selectiva y rápidamente con grupos diazo, formando un anillo más estable llamado pirazol. Al mezclarse con caldo microbiano, esta sonda actúa como un anzuelo químico: si hay algún compuesto diazo presente, la sonda se une y lo convierte en un producto más pesado y más fácilmente detectable. Usando espectrometría de masas sensible y metabolómica comparativa, el equipo comparó muestras tomadas inmediatamente tras añadir la sonda con muestras incubadas durante la noche. Las señales que crecían marcadamente con el tiempo y mostraban el patrón característico de doble pico de los productos de la sonda delataron metabolitos diazo ocultos.
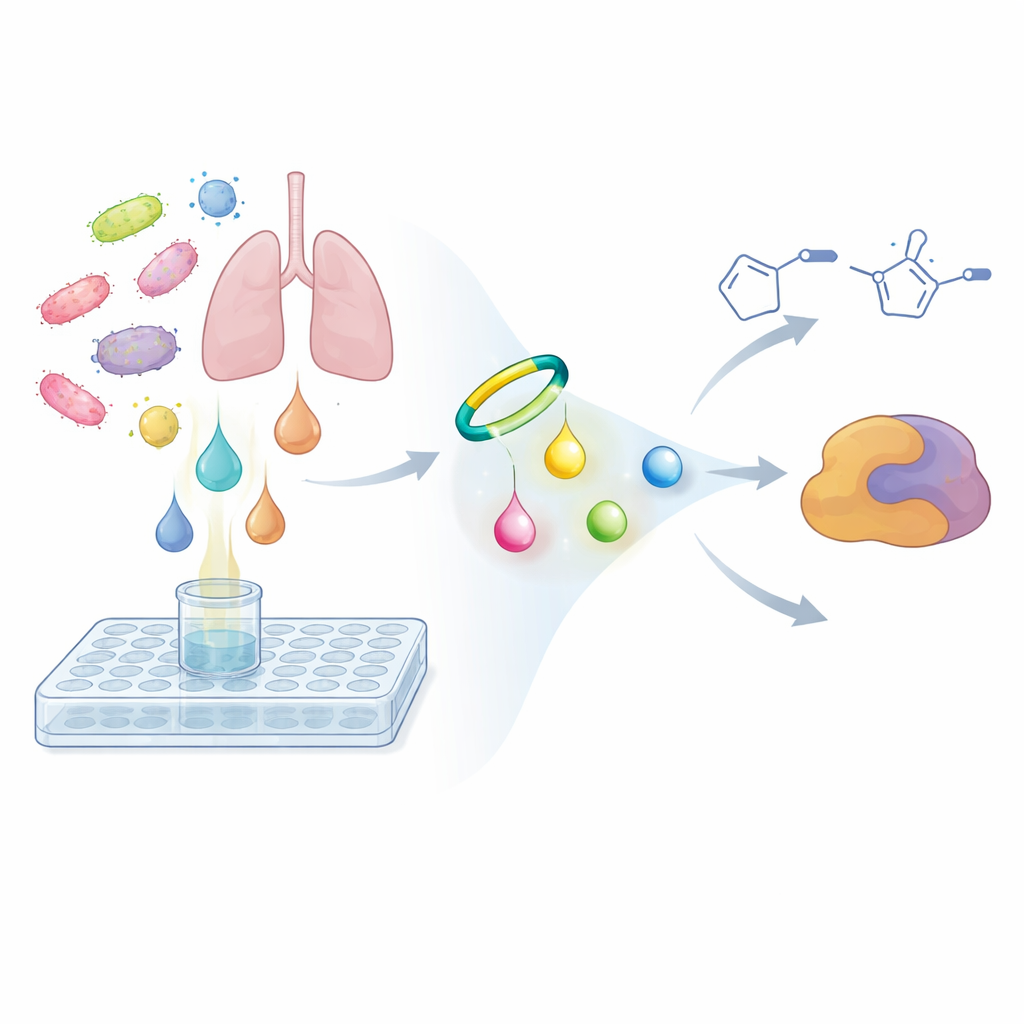
Nuevas moléculas reactivas de un patógeno pulmonar
El cribado de bacterias seleccionadas genéticamente con este flujo de trabajo basado en sondas llevó al equipo al patógeno pulmonar humano Nocardia ninae. En su caldo de cultivo observaron dos pares de productos derivados de la sonda que aparecían solo después de la incubación, tenían la composición rica en nitrógeno esperada y coincidían con el comportamiento previsto para compuestos diazo capturados. Al restar la fórmula conocida de la sonda y razonar sobre los átomos restantes, dedujeron que los productos naturales originales eran dos moléculas muy simples hasta entonces no descritas: ácido 4-diazo-3-oxobutírico y diazoacetona. Estos son bloques constructores diminutos en comparación con muchos productos naturales, pero muy reactivos. Experimentos de control mostraron que las moléculas no modificadas eran esencialmente invisibles para el análisis rutinario, mientras que las versiones etiquetadas por la sonda podían detectarse en concentraciones tan bajas como unos pocos cientos de partes por mil millones, lo que subraya lo fácilmente que tales metabolitos podrían haber pasado desapercibidos.
Descubrimiento de una vía enzimática inusual
Encontrar las moléculas fue solo la mitad de la historia; a continuación los investigadores rastrearon cómo las fabrica la bacteria. Al examinar su genoma, localizaron un cúmulo de genes, denominado dob, que se parecía a vías conocidas para construir unidades ricas en nitrógeno llamadas hidrazonas, pero con enzimas adicionales que sugerían pasos nuevos. Al trasladar este cúmulo génico a otra bacteria y mostrar que el huésped comenzaba a producir los mismos productos detectados por la sonda, confirmaron su papel. Experimentos bioquímicos detallados revelaron una línea de ensamblaje por pasos: aminoácidos comunes se remodelan hasta dar un intermedio portador de hidrazona, que se amplía mediante una enzima sintasa poliquetídica para formar un pequeño ácido con hidrazona. Una segunda enzima, una metaloproteína llamada Dob3, realiza entonces una hazaña química rara: oxida la hidrazona hasta convertirla en un grupo diazo. Esta reacción, llamada oxidación de hidrazona, se había propuesto pero no se había demostrado directamente en la naturaleza.
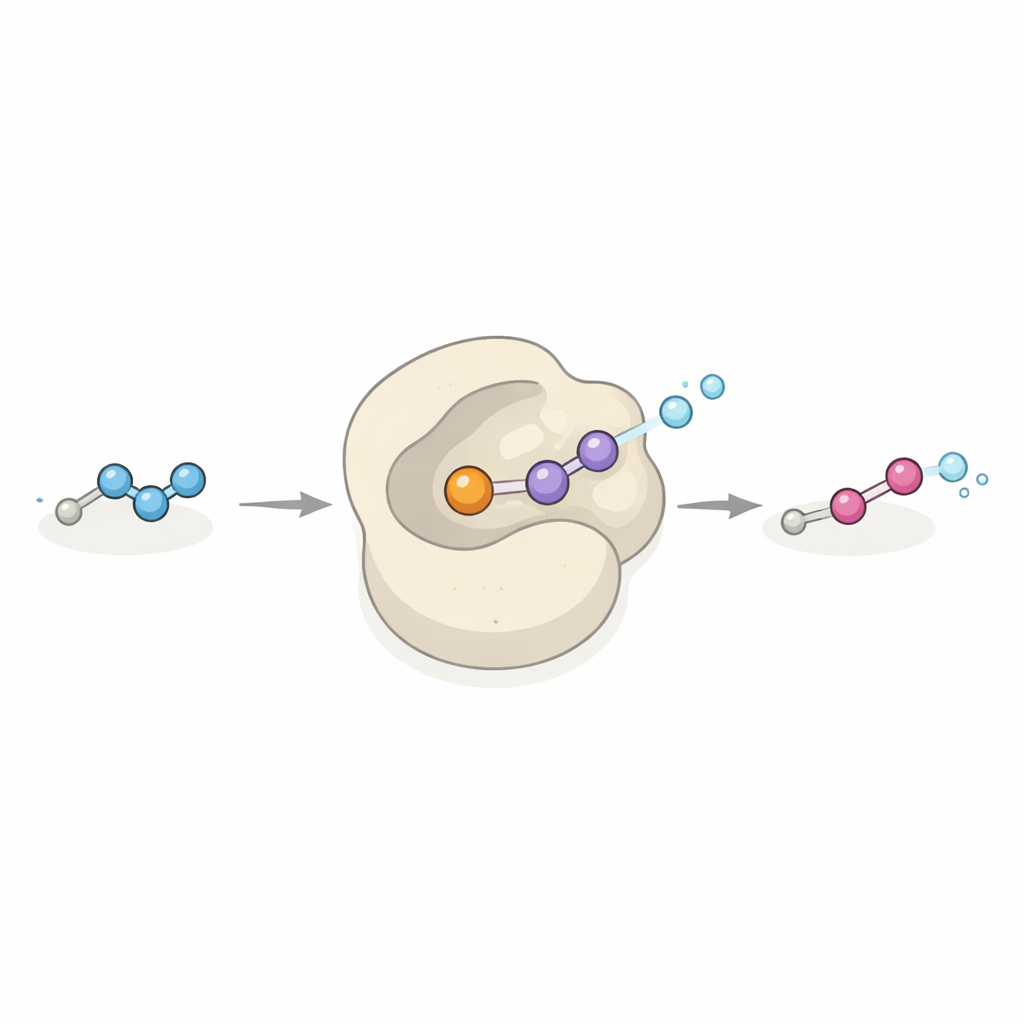
Un nuevo tipo de catalizador con promesa industrial
Dob3 pertenece a una familia de proteínas que normalmente añaden átomos de oxígeno a enlaces carbono–hidrógeno o nitrógeno–hidrógeno usando un par de átomos de hierro y oxígeno del aire. Aquí, Dob3 amplía ese repertorio al convertir una hidrazona relativamente estable en un grupo diazo altamente energizado mediante un paso de oxidación concertada de dos electrones. La enzima acepta una variedad de sustratos de hidrazona en experimentos de tubo de ensayo, convirtiéndolos en sus correspondientes compuestos diazo. Dado que muchos reactivos diazo son pilares de la síntesis moderna, especialmente para forjar enlaces carbono–carbono mediante las llamadas reacciones de transferencia de carbénos, Dob3 podría convertirse en un catalizador “verde” versátil para fabricar estos reactivos a partir de precursores simples en condiciones suaves y respetuosas con el medio ambiente.
Qué significa este trabajo de cara al futuro
Para el público no especializado, el mensaje clave es que la química que ocurre dentro de los microbios es tanto más rica como más delicada de lo que habíamos podido ver. Al usar la reactividad misma como guía —atrapando moléculas inestables en el instante en que se forman— este estudio revela nuevos compuestos diazo dentro de un patógeno humano y establece de forma firme la oxidación de hidrazonas como una vía natural hacia estos grupos reactivos. El descubrimiento de Dob3, una enzima dihierro que realiza esta transformación desafiante, abre la puerta a la ingeniería de microbios para producir reactivos diazo industriales de forma sostenible. En términos más amplios, el trabajo sugiere que muchos productos naturales reactivos siguen formando parte de una “materia oscura” microbiana de química, esperando ser descubiertos con estrategias de búsqueda igualmente ingeniosas y guiadas por la reactividad.
Cita: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Palabras clave: productos naturales diazo, cribado basado en reactividad, metabolitos microbianos, biocatálisis, descubrimiento de enzimas