Clear Sky Science · pl
Chemiczne wychwytywanie metabolitów diazo ujawnia biosyntetyczną oksydację hydrazonów
Dlaczego niestabilne cząsteczki mają dla nas znaczenie
Chemicy od dawna wiedzą, że niektóre z najpotężniejszych leków i reagentów przemysłowych są także najbardziej kruche. Rozpadają się tak szybko, że odnalezienie ich w przyrodzie bywa jak łapanie baniek mydlanych na burzy. To badanie zajmuje się jedną z takich ulotnych rodzin cząsteczek, zwanych związkami diazo, które wytwarzają mikroby i które mogą zarówno uszkadzać komórki, jak i napędzać przydatne reakcje chemiczne. Dzięki wynalezieniu sposobu „złapania” tych niestabilnych cząsteczek zaraz po ich powstaniu, badacze odkrywają nową chemię w patogenie ludzkiego płuca i ujawniają enzym, który mógłby stać się ekologicznym narzędziem w wytwarzaniu cennych reagentów.
Ukryte bronie od maleńkich mikrobów
Mikroorganizmy to miniaturowe fabryki chemiczne. Wśród wielu związków, które produkują, są naturalne produkty zawierające grupy diazo, niosące parę atomów azotu gotowych do rozpadu i uwolnienia energii. Ta reaktywność pozwala im atakować cele biologiczne, co daje właściwości przeciwbakteryjne i przeciwnowotworowe, a także czyni je cenionymi reagentami w laboratoriach syntez organicznych. Mimo to znanych jest tylko kilka lub kilkadziesiąt naturalnych związków diazo. Przegląd danych genetycznych zespołu ujawnił setki szczepów genowych mikroorganizmów, które wydają się zdolne do wytwarzania związków diazo, rozsianych w bakteriach glebowych, mikroorganizmach morskich i patogenach. Rozbieżność między potencjałem genetycznym a niewielką liczbą znanych związków sugerowała, że wiele molekuł diazo pozostaje niewidocznych, prawdopodobnie dlatego, że są zbyt niestabilne dla standardowych metod odkrywania opartych na izolacji trwałych, obfitych produktów.
Łapanie ulotnych cząsteczek chemicznym haczykiem
Aby rozwiązać ten problem, badacze odwrócili zwykłą strategię poszukiwań. Zamiast pytać, czy ekstrakty mikroba zabijają komórki rakowe lub bakterie, pytali, czy jego metabolity wykazują określony rodzaj reaktywności chemicznej. Zaprojektowali małą sondę opartą na napiętym alkinie w pierścieniu, który reaguje selektywnie i szybko z grupami diazo, tworząc bardziej stabilny pierścień zwany pyrazolem. Po zmieszaniu z bulionem mikrobiologicznym ta sonda działa jak chemiczny haczyk: jeśli obecny jest jakikolwiek związek diazo, sonda przyłącza się i przekształca go w cięższy, łatwiejszy do wykrycia produkt. Przy użyciu czułej spektrometrii mas i porównawczej metabolomiki zespół porównał próbki pobrane natychmiast po dodaniu sondy z próbkami inkubowanymi przez noc. Sygnały, które silnie rosły w czasie i wykazywały charakterystyczny podwójny wzorzec pików produktów sondy, wskazywały ukryte metabolity diazo.
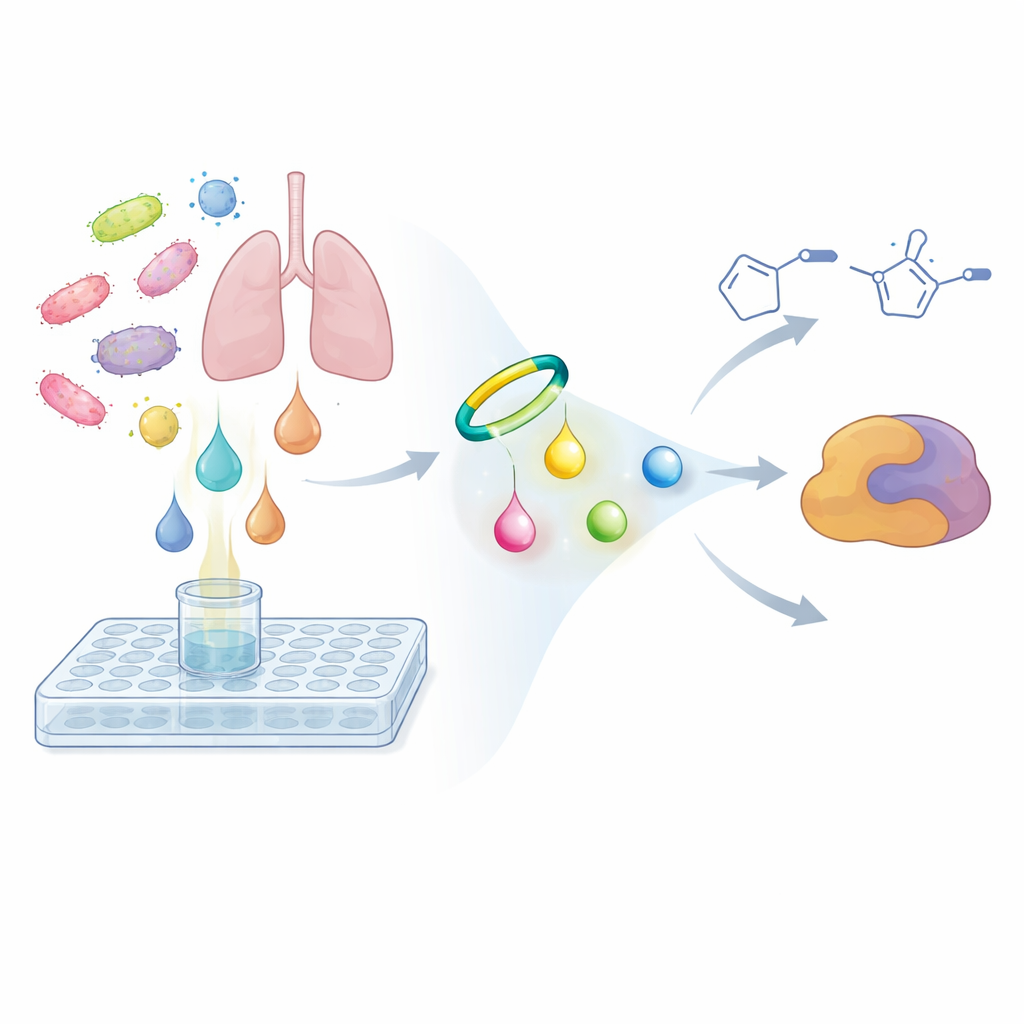
Nowe reaktywne molekuły z patogenu płuc
Screening genetycznie wybranych bakterii przy użyciu tego workflow opartego na sondzie doprowadził zespół do ludzkiego patogena płuc Nocardia ninae. W jego bulionie hodowlanym zaobserwowali dwie pary produktów pochodzących od sondy, które pojawiły się dopiero po inkubacji, miały oczekiwaną bogatą w azot kompozycję i pasowały do zachowania spodziewanego dla wychwyconych związków diazo. Odejmując znany wzór cząsteczki sondy i analizując pozostałe atomy, wywnioskowali, że oryginalne naturalne produkty to dwie bardzo proste, wcześniej nieopisane cząsteczki: kwas 4-diazo-3-oksobutanowy oraz diazoaceton. To maleńkie cegiełki w porównaniu z wieloma naturalnymi produktami, lecz bardzo reaktywne. Kontrolne eksperymenty pokazały, że niezmodyfikowane cząsteczki były praktycznie niewidoczne dla rutynowych analiz, podczas gdy wersje znaczone sondą dało się wykryć w stężeniach rzędu kilkuset części na miliard, co podkreśla, jak łatwo takie metabolity mogły zostać przeoczone.
Odkrycie nietypowej ścieżki enzymatycznej
Odnalezienie molekuł to była tylko połowa historii; badacze następnie prześledzili, jak bakteria je wytwarza. Analizując genom, zidentyfikowali klaster genów nazwany dob, który przypominał znane ścieżki tworzenia jednostek bogatych w azot zwanych hydrazonami, ale z dodatkowymi enzymami sugerującymi nowe kroki. Przenosząc ten klaster genów do innej bakterii i pokazując, że gospodarz zaczął produkować te same produkty wykryte przez sondę, potwierdzili jego rolę. Szczegółowe eksperymenty biochemiczne ujawniły etapową linię montażową: powszechne aminokwasy są przekształcane w pośrednik zawierający hydrazon, który jest przedłużany przez enzym syntazę poliketydową do utworzenia małego kwasu z hydrazonem. Drugi enzym, metaloproteina nazwana Dob3, przeprowadza rzadkie chemiczne osiągnięcie: utlenia hydrazon do grupy diazo. Ta reakcja, zwana oksydacją hydrazonu, była proponowana wcześniej, ale nie została bezpośrednio udokumentowana w przyrodzie.
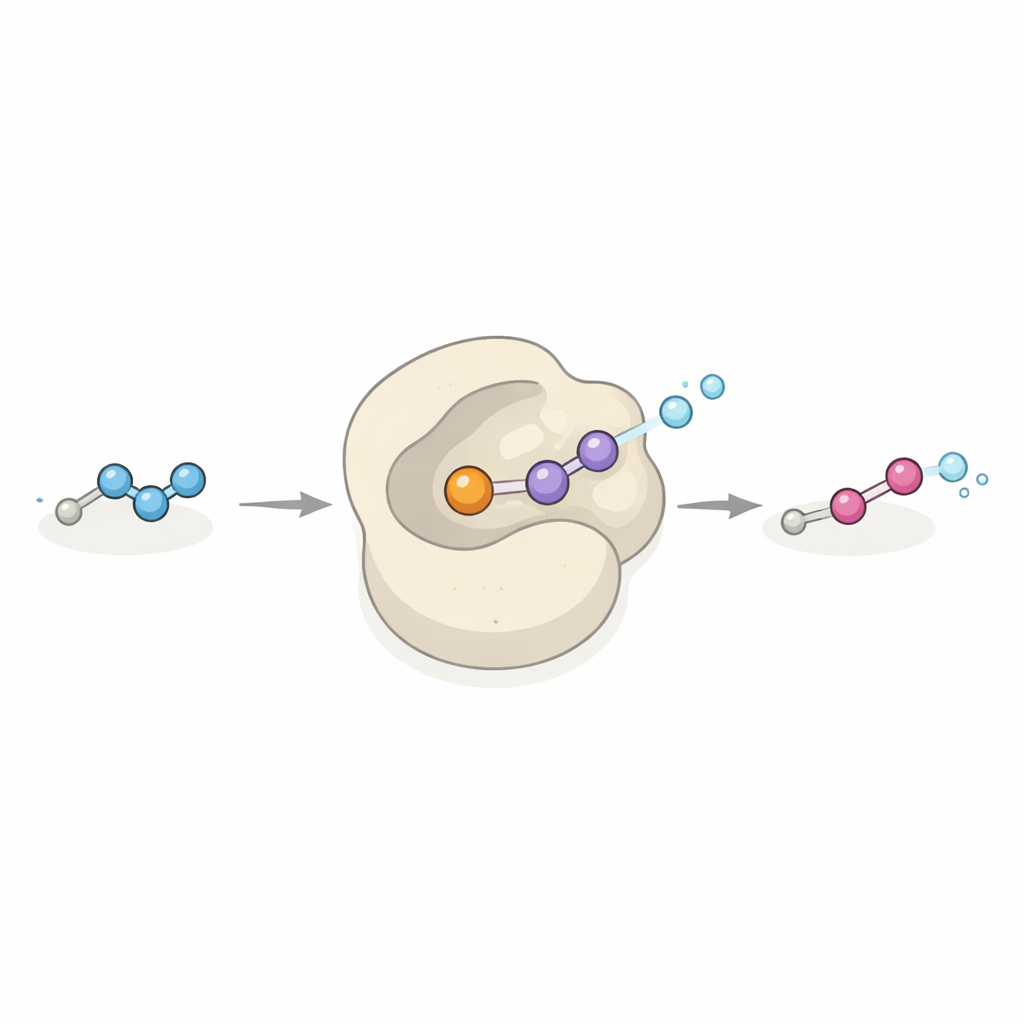
Nowy rodzaj katalizatora z perspektywą przemysłową
Dob3 należy do rodziny białek, które zwykle wprowadzają atomy tlenu do wiązań węgiel–wodór lub azot–wodór, używając pary atomów żelaza i tlenu z powietrza. Tutaj Dob3 rozszerza to repertuar, przekształcając stosunkowo stabilny hydrazon w wysokoenergetyczną grupę diazo w skoordynowanym, dwuelektronowym kroku utleniania. Enzym akceptuje różne substraty hydrazonowe w eksperymentach w probówkach, przekształcając je w odpowiadające im związki diazo. Ponieważ wiele reagentów diazo stanowi fundament współczesnej syntezy organicznej, zwłaszcza przy tworzeniu wiązań węgiel–węgiel przez tzw. reakcje transferu karbenów, Dob3 może stać się wszechstronnym „zielonym” katalizatorem do wytwarzania tych reagentów z prostych prekursorów w łagodnych, przyjaznych środowisku warunkach.
Co to oznacza na przyszłość
Dla laika kluczowy wniosek jest taki, że chemia zachodząca w mikroorganizmach jest bogatsza i delikatniejsza, niż do tej pory potrafiliśmy zaobserwować. Używając samej reaktywności jako drogowskazu — łapiąc niestabilne cząsteczki w chwili ich powstawania — to badanie ujawnia nowe związki diazo w patogenie ludzkim i zdecydowanie potwierdza oksydację hydrazonu jako naturalną drogę do tych reaktywnych grup. Odkrycie Dob3, di‑żelazowego enzymu wykonującego to wymagające przekształcenie, otwiera drzwi do inżynierii mikroorganizmów produkujących przemysłowe reagentia diazo w sposób zrównoważony. Szerzej, praca sugeruje, że wiele reaktywnych naturalnych produktów pozostaje częścią mikrobiologicznej „ciemnej materii” chemii, czekając na odkrycie przy użyciu podobnie sprytnych strategii poszukiwań kierowanych reaktywnością.
Cytowanie: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Słowa kluczowe: naturalne produkty diazo, screening oparty na reaktywności, metabolity mikrobiologiczne, biokataliza, odkrywanie enzymów