Clear Sky Science · pt
Captura química de metabólitos diazo revela oxidação biossintética de hidrazonas
Por que moléculas instáveis importam para nós
Químicos sabem há muito tempo que alguns dos medicamentos e reagentes industriais mais potentes também são os mais frágeis. Eles se degradam tão rapidamente que encontrá‑los na natureza pode ser como tentar apanhar bolhas de sabão numa tempestade. Este estudo enfrenta uma família dessas moléculas efêmeras, chamadas compostos diazo, que são produzidas por microrganismos e podem tanto danificar células quanto promover reações químicas úteis. Ao criar uma maneira de “capturar” essas moléculas instáveis assim que surgem, os pesquisadores descobrem nova química em um patógeno pulmonar humano e revelam uma enzima que pode se tornar uma ferramenta verde para fabricar reagentes valiosos.
Armas ocultas de micróbios minúsculos
Microorganismos são pequenas fábricas químicas. Entre os muitos compostos que produzem estão produtos naturais contendo diazo, que carregam um par de átomos de nitrogênio prontas para se separar e liberar energia. Essa reatividade lhes permite atacar alvos biológicos, originando atividades antibióticas e anticâncer, e também os torna reagentes valiosos em laboratórios de síntese. Ainda assim, apenas algumas dezenas de compostos diazo naturais são conhecidos. O levantamento de dados genéticos da equipe revelou centenas de agrupamentos genéticos microbianos que parecem capazes de produzir moléculas diazo, espalhados por bactérias do solo, micróbios marinhos e patógenos. A discrepância entre o potencial genético e o pequeno número de compostos conhecidos sugeriu que muitas moléculas diazo permanecem invisíveis, provavelmente porque são instáveis demais para os métodos de descoberta padrão, que dependem do isolamento de produtos estáveis e abundantes.
Capturando moléculas fugazes com um gancho químico
Para resolver esse problema, os pesquisadores inverteram a estratégia usual de busca. Em vez de perguntar se os extratos de um microrganismo matam células cancerígenas ou bactérias, eles perguntaram se seus metabólitos compartilham um tipo específico de reatividade química. Projetaram uma pequena molécula‑sonda baseada em um alcino em anel tensionado que reage seletiva e rapidamente com grupos diazo, formando um anel mais estável chamado pirazol. Quando misturada ao meio de cultura microbiano, essa sonda age como um gancho químico: se houver qualquer composto diazo presente, a sonda se liga e o converte em um produto mais pesado e mais facilmente detectável. Usando espectrometria de massa sensível e metabolômica comparativa, a equipe comparou amostras tomadas imediatamente após a adição da sonda com amostras incubadas durante a noite. Sinais que cresceram fortemente ao longo do tempo e mostraram o padrão característico de picos duplicados dos produtos da sonda sinalizaram metabólitos diazo ocultos.
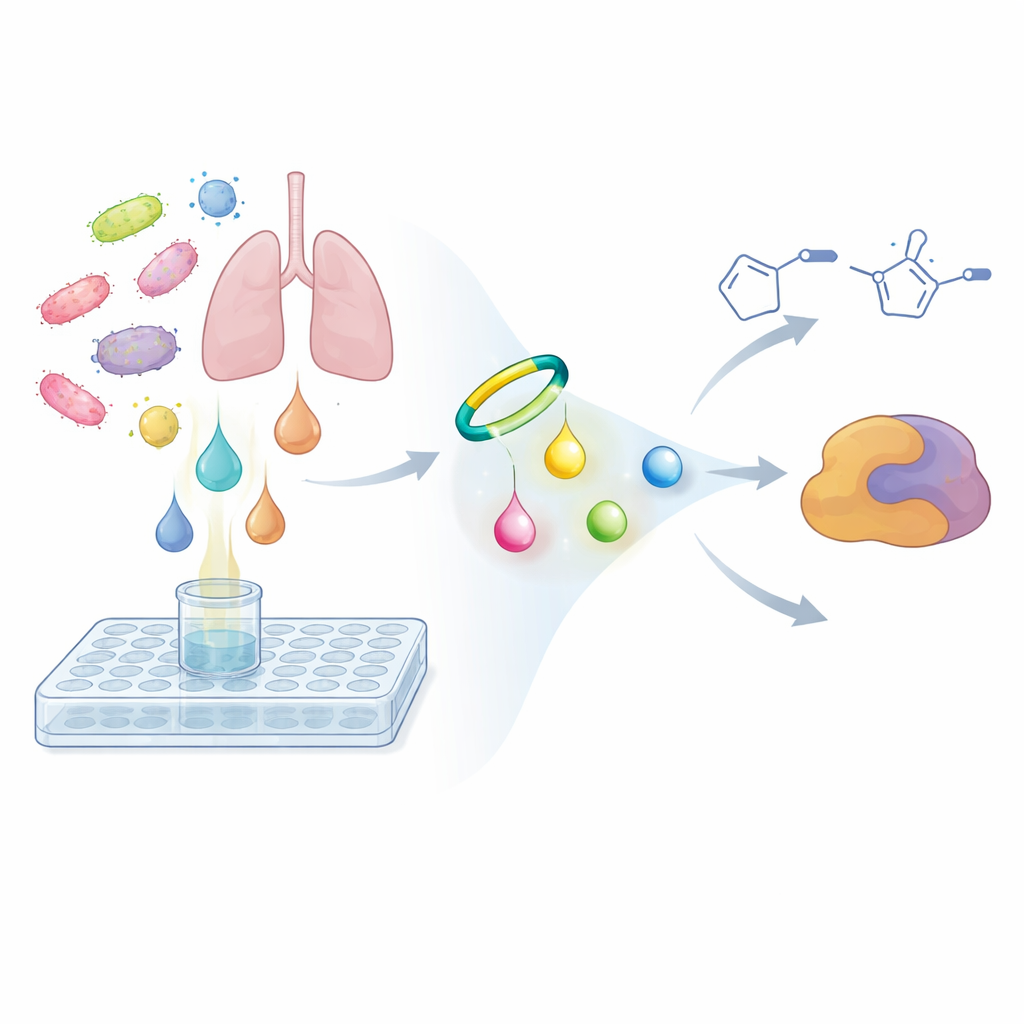
Novas moléculas reativas de um patógeno pulmonar
A triagem de bactérias selecionadas geneticamente com esse fluxo de trabalho baseado em sondas levou a equipe ao patógeno pulmonar humano Nocardia ninae. Em seu caldo de cultura, observaram dois pares de produtos derivados da sonda que apareceram apenas após incubação, tinham a composição rica em nitrogênio esperada e correspondiam ao comportamento previsto para compostos diazo capturados. Ao subtrair a fórmula conhecida da sonda e raciocinar sobre os átomos restantes, deduziram que os produtos naturais originais eram duas moléculas muito simples, porém antes não vistas: ácido 4‑diazo‑3‑oxobutanoico e diazoacetona. Esses são blocos de construção pequenos comparados com muitos produtos naturais, mas altamente reativos. Experimentos de controle mostraram que as moléculas não modificadas eram essencialmente invisíveis à análise rotineira, enquanto as versões marcadas pela sonda podiam ser detectadas em concentrações tão baixas quanto algumas centenas de partes por bilhão, destacando quão facilmente tais metabólitos poderiam ter passado despercebidos.
Descoberta de uma via enzimática incomum
Encontrar as moléculas foi apenas metade da história; os pesquisadores então rastrearam como a bactéria as produz. Ao examinar seu genoma, identificaram um agrupamento de genes, chamado dob, que lembrava vias conhecidas para a construção de unidades ricas em nitrogênio chamadas hidrazonas, mas com enzimas adicionais sugerindo etapas novas. Ao transferir esse agrupamento gênico para outra bactéria e mostrar que o hospedeiro passou a produzir os mesmos produtos detectados pela sonda, confirmaram sua função. Experimentos bioquímicos detalhados revelaram uma linha de montagem passo a passo: aminoácidos comuns são remodelados em um intermediário contendo hidrazona, que é estendido por uma enzima poliquinona sintase para formar um pequeno ácido com hidrazona. Uma segunda enzima, uma metalenzima chamada Dob3, então realiza uma façanha química rara: ela oxida a hidrazona formando um grupo diazo. Essa reação, chamada oxidação de hidrazona, havia sido proposta, mas não demonstrada diretamente na natureza.
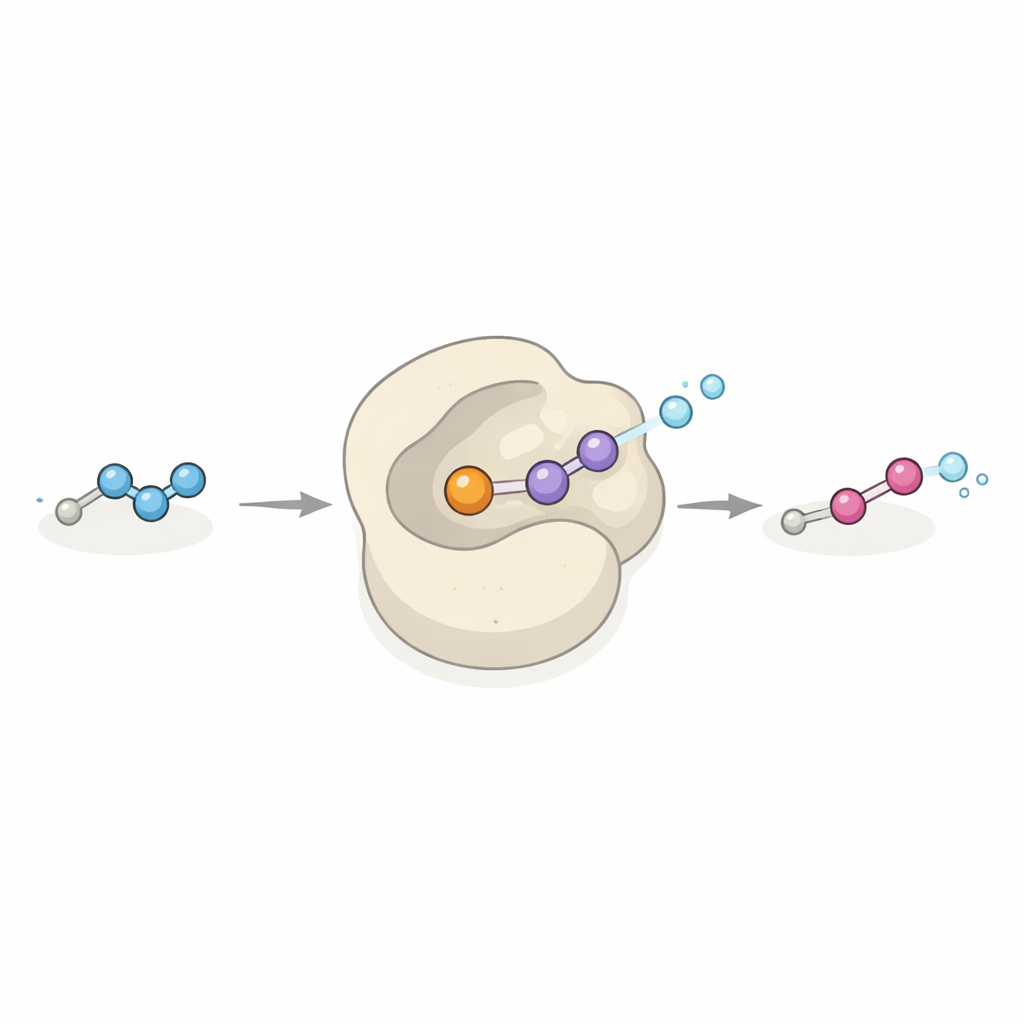
Um novo tipo de catalisador com promessa industrial
Dob3 pertence a uma família de proteínas que normalmente adicionam átomos de oxigênio a ligações carbono–hidrogênio ou nitrogênio–hidrogênio usando um par de átomos de ferro e oxigênio do ar. Aqui, Dob3 amplia esse repertório ao transformar uma hidrazona relativamente estável em um grupo diazo altamente energizado em um passo oxidativo concertado de dois elétrons. A enzima aceita uma gama de substratos hidrazona em experimentos de tubo de ensaio, convertendo‑os em seus compostos diazo correspondentes. Como muitos reagentes diazo são pilares da química sintética moderna, especialmente para formar ligações carbono–carbono por meio das chamadas reações de transferência de carbene, Dob3 pode se tornar um catalisador “verde” versátil para produzir esses reagentes a partir de precursores simples sob condições suaves e ambientalmente amigáveis.
O que este trabalho significa daqui para frente
Para não especialistas, a mensagem principal é que a química que ocorre dentro dos micróbios é tanto mais rica quanto mais delicada do que éramos capazes de ver. Ao usar a reatividade em si como um farol — capturando moléculas instáveis no momento em que são produzidas — este estudo revela novos compostos diazo dentro de um patógeno humano e estabelece firmemente a oxidação de hidrazona como uma via natural para esses grupos reativos. A descoberta de Dob3, uma enzima di‑ferro que realiza essa transformação desafiadora, abre portas para a engenharia de micróbios capazes de produzir reagentes diazo industriais de forma sustentável. Mais amplamente, o trabalho sugere que muitos produtos naturais reativos permanecem como uma “matéria escura” microbiana da química, esperando para serem desvelados com estratégias de busca igualmente engenhosas e guiadas pela reatividade.
Citação: Pfeifer, K., Van Cura, D., Wu, K.J.Y. et al. Chemical capture of diazo metabolites reveals biosynthetic hydrazone oxidation. Nature 652, 517–525 (2026). https://doi.org/10.1038/s41586-025-10079-x
Palavras-chave: produtos naturais diazo, triagem baseada em reatividade, metabólitos microbianos, biocatálise, descoberta de enzimas