Clear Sky Science · sv
En regelbaserad simuleringsmodell belyser rollen för asymmetrisk mitokondriell fission för betacells hälsa
Varför små kraftverk spelar roll för blodsockret
Inuti varje insulinproducerande cell i bukspottkörteln finns dussintals mitokondrier, cellens små kraftverk. Deras uppgift är att omvandla socker till energisignalen som får dessa celler att frigöra insulin och hålla blodsockret i schack. Vid typ 2-diabetes sviktar detta system, och mitokondrierna ser ofta skadade och fragmenterade ut i mikroskopet. Denna studie använder avancerade datorsimuleringar för att ställa en enkel men viktig fråga: hur påverkar sättet mitokondrier delar sig och förnyar sig långsiktigt dessa cellers hälsa och deras förmåga att frigöra insulin?
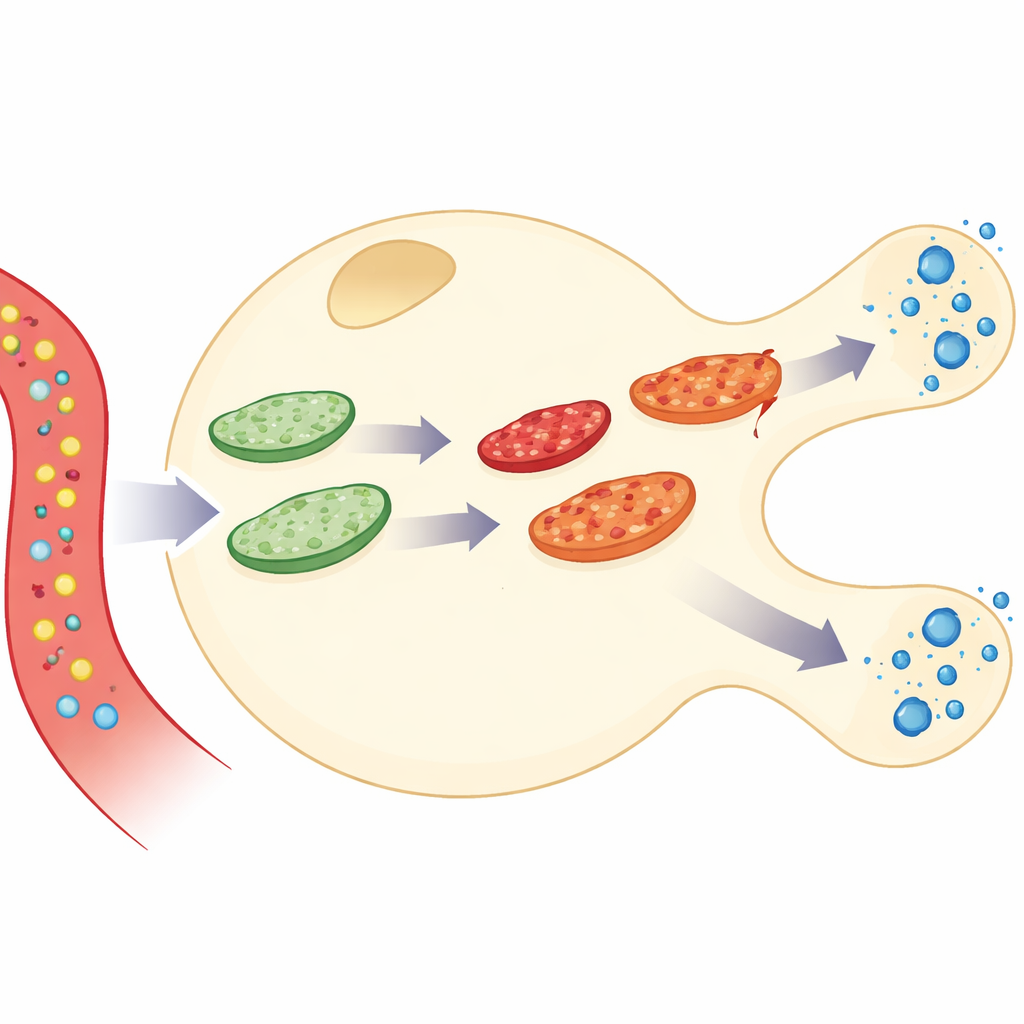
Koppla energianvändning till insulinutsöndring
Författarna byggde en detaljerad simulering av en enskild pankreas betacell, den celltyp som bildar och sekreterar insulin. Deras modell länkar tre aktivitetslager: hur glukos förbränns för att skapa energimolekylen ATP, hur kalcium i cellen svarar, och hur insulinpaket släpps ut. Utöver detta lade de till ett dynamiskt mitokondriellt ”nätverk” som ständigt fusionerar och delar sig. Genom att kombinera dessa delar kan modellen följa vad som händer när glukos kommer in i cellen, ATP ökar, kalciumpulser uppstår och insulin sekreteras — samtidigt som mitokondrierna själva åldras, ackumulerar skador, repareras och avlägsnas.
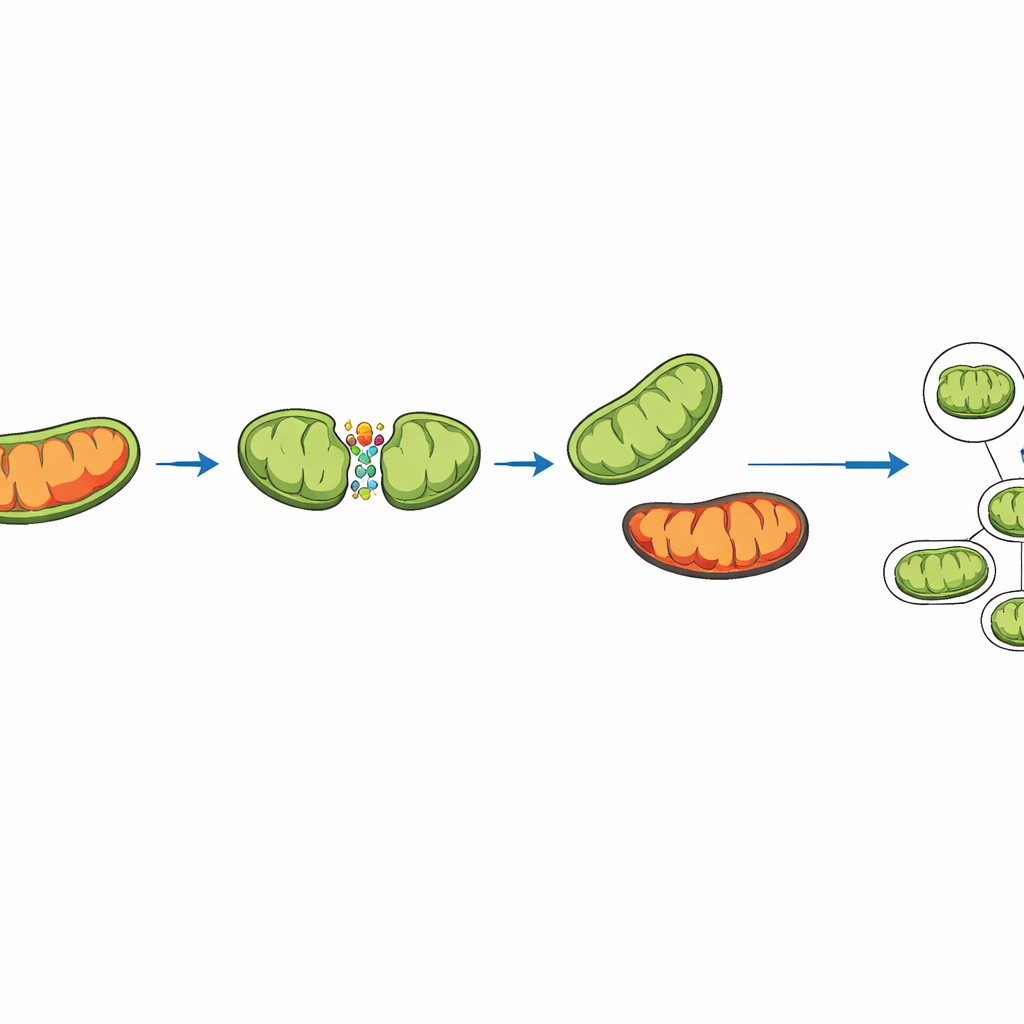
Två sätt att dela sig — och varför ett räddar situationen
Nyare experiment visar att mitokondrier inte alltid delar sig på samma sätt. Ibland delar de sig nära mitten och bildar två likartade dottermitokondrier. Andra gånger avknoppas en liten, mycket skadad spets, vilket lämnar kvar en större, friskare del. Simuleringen fångar båda typerna av delning genom att representera nyckelproteiner som förankrar fissionsmaskineriet på olika platser på mitokondriernas yta. I modellen följs en ”skadesumma” för varje mitokondrie. När en perifer delning sker leds extra skada avsiktligt in i den lilla fragmentet. Detta fragment är mer benäget att bli uppslukat och återvinningsbart av cellen, en process som kallas mitofagi, medan den större, renare delen stannar kvar i nätverket.
Hur sortering av skador håller nätverket ungt
Genom att systematiskt variera hur starkt skada sorteras in i det lilla fragmentet och hur skadad en mitokondrie kan vara innan den tas bort, undersökte forskarna tusentals virtuella scenarier. När delningen inte sorterade skador drev nästan alla mitokondrier mot samma, relativt ohälsosamma nivå av slitage. I kontrast sänkte även en blygsam bias som skickade bara lite mer skada till det lilla fragmentet medelvärdet av skador i nätverket avsevärt. Upprepade omgångar av sådan asymmetrisk delning och selektiv borttagning skapade ett självrenande system där friska mitokondrier förblev kapabla att producera ATP effektivt.
När viktiga fissionsproteiner saknas
Teamet efterliknade sedan vanliga experimentella manipulationer. Ett förankringsprotein, Fis1, främjar i första hand perifera fissionsevent som koncentrerar skada till små fragment. Att minska Fis1 i modellen ledde till färre perifera delningar, mer jämnt fördelade skador och ett sammanbrott av nätverkets hälsa. En annan förankrare, MFF, gynnar mittzonsdelningar som producerar lika dotterdelar. Att sänka MFF orsakade bara milda förändringar i skadenivåer men gav större, mer sammansmälta mitokondrier, vilket stämmer överens med laboratorieobservationer att denna väg mer handlar om att förbereda celler för delning än om att rensa skador. När det centrala fissionsproteinet Drp1 reducerades upphörde delning nästan helt. Skadorna steg då nära det möjliga maximumet och lämnade nätverket allvarligt komprometterat.
Från utmattade mitokondrier till sämre insulinutsöndring
Eftersom modellen kopplar mitokondriell hälsa till ATP-produktion kan den förutsäga hur dessa strukturella förändringar påverkar insulinutsöndringen. Vid måttlig förlust av Fis1 frisatte cellen fortfarande insulin vid låg glukos, men dess respons på hög glukos dämpades — liknande betaceller från personer med tidig metabol sjukdom. Vid kraftig Drp1-förlust blev cellen nästan oresponsiv mot glukos: insulinutsöndringen höll sig nära en låg basalnivå även när sockret var högt. Dessa mönster liknar rapporterade experimentella resultat och antyder att balanserat uttryck av fissionsproteinerna är avgörande för att hålla betaceller både energifyllda och responsiva.
Vad detta innebär för förståelsen av diabetes
För lekmannen är studiens budskap att hur mitokondrierna bryts isär är lika viktigt som hur de producerar energi. Ett noggrant avvägt ”bra brott” skär bort skadade delar och håller nätverket ungt, vilket stödjer stark insulinutsöndring. När den mekanismen för trimning försvagas eller slås ut staplas skadade mitokondrier på hög, ATP-produktionen sviktar och betaceller får svårt att svara på stigande blodsocker. Genom att fånga dessa samband i en flexibel datormodell erbjuder arbetet en testbädd för framtida idéer om hur man kan skydda eller återställa mitokondriers kvalitet vid diabetes, vilket potentiellt kan vägleda nya behandlingar som hjälper betaceller att förbli friska längre.
Citering: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Nyckelord: mitokondrier, insulinutsöndring, betaceller, typ 2-diabetes, datorbaserad modellering