Clear Sky Science · pt
Um modelo de simulação baseado em regras ilumina o papel da fissão mitocondrial assimétrica na saúde das células beta
Por que as pequenas usinas importam para o açúcar no sangue
Dentro de cada célula produtora de insulina do pâncreas existem dezenas de mitocôndrias, as minúsculas usinas de energia da célula. Sua função é transformar açúcar no sinal energético que indica a essas células que liberem insulina e mantenham o açúcar no sangue sob controle. Na diabetes tipo 2, esse sistema falha, e as próprias mitocôndrias frequentemente aparecem danificadas e fragmentadas ao microscópio. Este estudo usa simulações computacionais avançadas para fazer uma pergunta simples, porém importante: como a forma como as mitocôndrias se dividem e se renovam afeta a saúde a longo prazo dessas células e sua capacidade de liberar insulina?
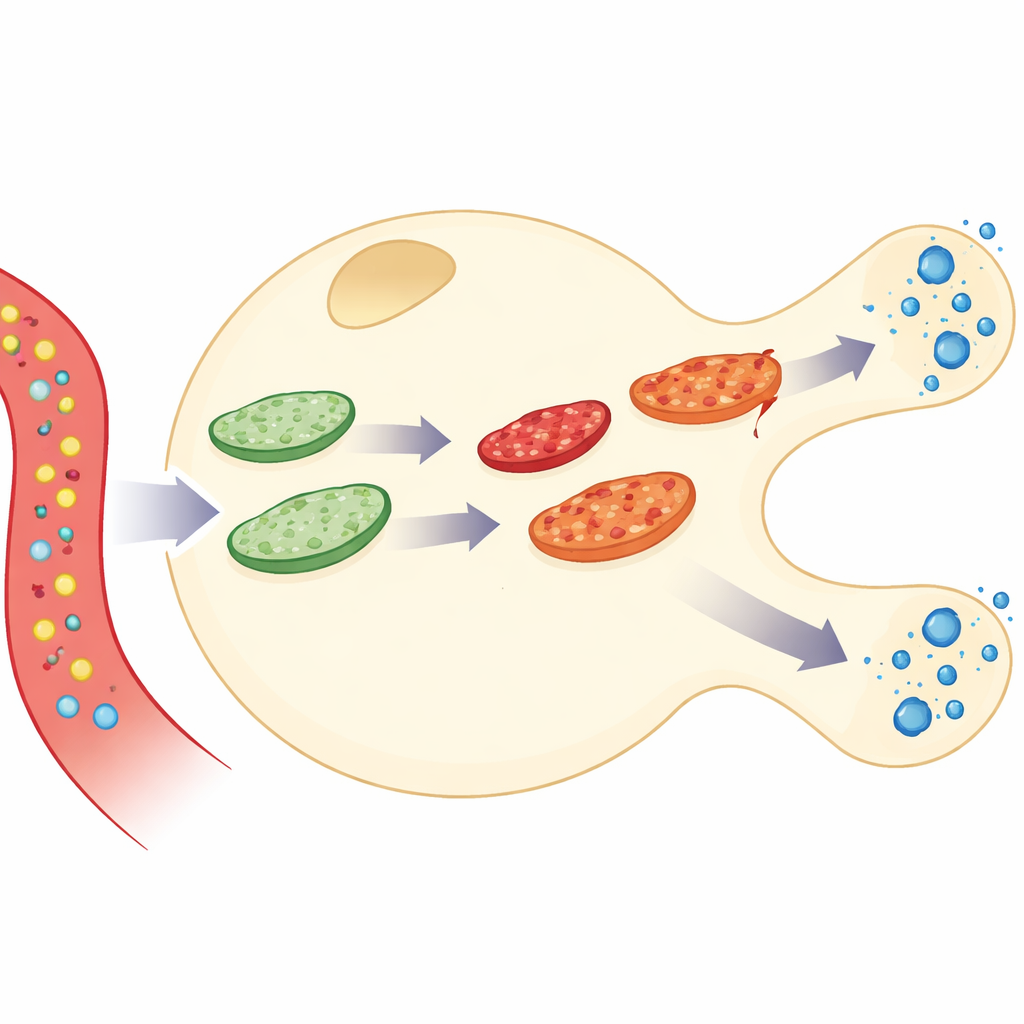
Ligando o uso de energia à liberação de insulina
Os autores construíram uma simulação detalhada de uma única célula beta pancreática, o tipo celular que produz e secreta insulina. O modelo conecta três camadas de atividade: como a glicose é queimada para produzir a molécula energética ATP, como o cálcio intracelular responde, e como os grânulos de insulina são liberados. Sobre isso, adicionaram uma “rede” mitocondrial dinâmica que está constantemente se fundindo e se dividindo. Ao combinar essas partes, o modelo pode acompanhar o que acontece quando a glicose entra na célula, o ATP sobe, o cálcio pulsa e a insulina é secretada — enquanto as próprias mitocôndrias envelhecem, acumulam dano, se recuperam e são removidas.
DuAS formas de divisão mitocondrial — e por que uma delas salva o dia
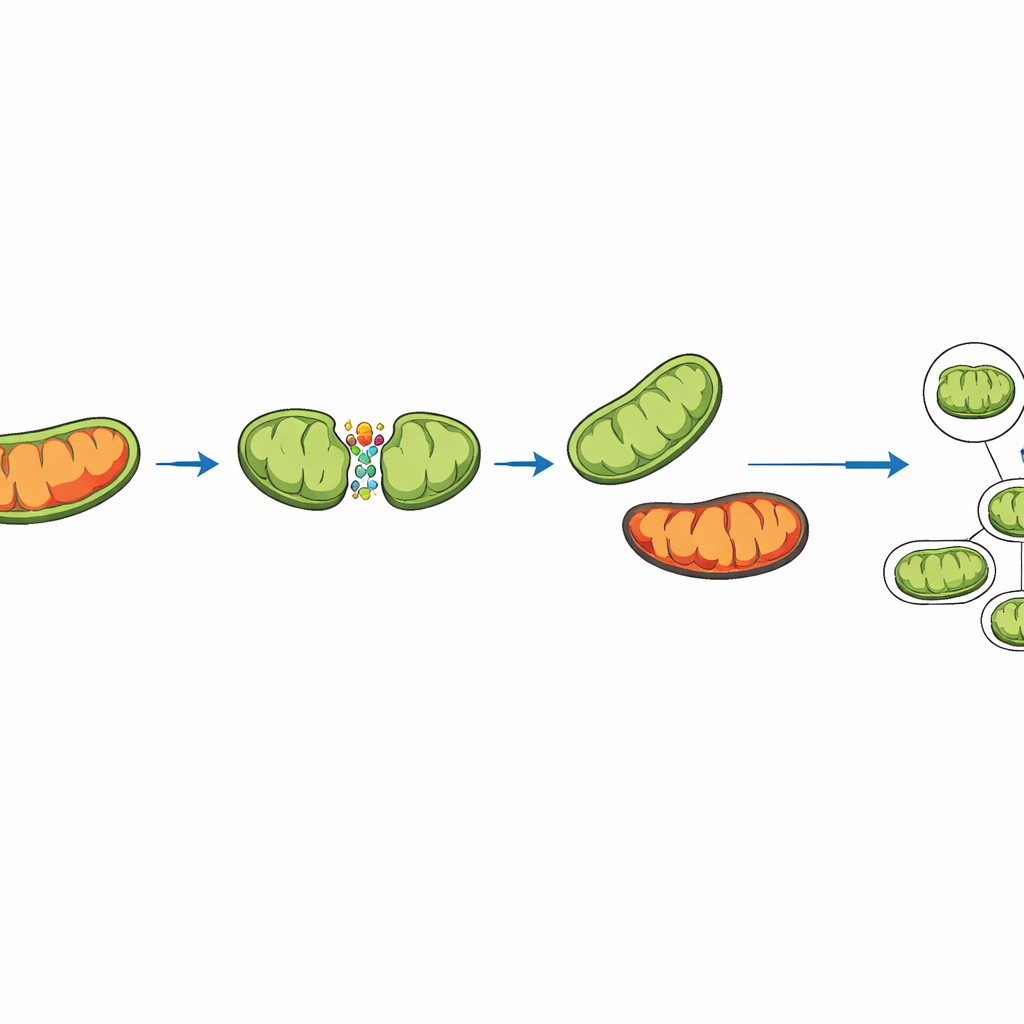
Experimentos recentes mostram que as mitocôndrias não se dividem todas da mesma maneira. Às vezes elas separtem perto do meio, gerando duas mitocôndrias filhas semelhantes. Outras vezes dividem-se em uma ponta pequena e altamente danificada, deixando para trás um fragmento maior e mais saudável. A simulação captura ambos os tipos de fissão ao representar proteínas-chave que ancoram a maquinaria de divisão em diferentes pontos da superfície mitocondrial. No modelo, é acompanhado um “placar de dano” para cada mitocôndria. Quando ocorre uma fissão periférica, dano extra é deliberadamente redirecionado para o pequeno fragmento. Esse fragmento tem mais probabilidade de ser engolido e reciclado pela célula, um processo chamado mitofagia, enquanto o fragmento maior e mais limpo permanece na rede.
Como a triagem de danos mantém a rede jovem
Ao variar sistematicamente quão fortemente o dano é direcionado para o pequeno fragmento e quão danificada uma mitocôndria pode ficar antes de ser removida, os pesquisadores exploraram milhares de cenários virtuais. Quando a fissão não fazia triagem de danos, quase todas as mitocôndrias evoluíam para o mesmo nível relativamente alto de desgaste. Em contraste, mesmo um viés modesto que empurrasse um pouco mais de dano para o fragmento pequeno reduzia bastante o dano médio na rede. Rodadas repetidas dessa divisão assimétrica e remoção seletiva criaram um sistema de autolimpeza, no qual mitocôndrias saudáveis permaneciam capazes de produzir ATP de forma eficiente.
Quando proteínas chave da fissão desaparecem
A equipe então imitou manipulações experimentais comuns. Uma proteína âncora, Fis1, promove principalmente eventos de fissão periférica que concentram o dano em pequenos fragmentos. Reduzir Fis1 no modelo levou a menos fissões periféricas, mitocôndrias mais uniformemente danificadas e à quebra da saúde da rede. Outra âncora, MFF, favorece fissões na região central que produzem filhas semelhantes. Diminuir MFF causou apenas mudanças leves nos níveis de dano, mas produziu mitocôndrias maiores e mais fundidas, condizendo com observações de laboratório de que essa via está mais relacionada a preparar células para dividir-se do que a remover danos. Quando a proteína central de fissão Drp1 foi reduzida, a divisão praticamente cessou. O dano então subiu perto do máximo possível, deixando a rede seriamente comprometida.
De mitocôndrias cansadas a liberação de insulina prejudicada
Porque o modelo vincula a saúde mitocondrial à produção de ATP, ele pode prever como essas mudanças estruturais impactam a secreção de insulina. Com perda moderada de Fis1, a célula ainda liberou insulina em glicose baixa, mas sua resposta à glicose alta ficou atenuada — semelhante às células beta de pessoas com doença metabólica inicial. Com forte perda de Drp1, a célula tornou-se quase não responsiva à glicose: a liberação de insulina permaneceu em um nível basal baixo mesmo quando a glicose estava elevada. Esses padrões se assemelham a resultados experimentais relatados e sugerem que a expressão equilibrada das proteínas de fissão é essencial para manter as células beta energizadas e responsivas.
O que isso significa para entender o diabetes
Para leigos, a mensagem do estudo é que a forma como as mitocôndrias se partem é tão importante quanto a forma como produzem energia. Uma “boa divisão” afinada remove pedaços danificados e mantém a rede jovem, sustentando uma forte liberação de insulina. Quando esse mecanismo de poda é enfraquecido ou interrompido, mitocôndrias danificadas se acumulam, a produção de ATP falha e as células beta lutam para responder ao aumento do açúcar no sangue. Ao capturar essas ligações em um modelo computacional flexível, o trabalho oferece um campo de testes para ideias futuras sobre como proteger ou restaurar a qualidade mitocondrial no diabetes, potencialmente orientando novos tratamentos que ajudem as células beta a permanecerem saudáveis por mais tempo.
Citação: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Palavras-chave: mitocôndrias, secreção de insulina, células beta, diabetes tipo 2, modelagem computacional