Clear Sky Science · ar
نموذج محاكاة قائم على قواعد يوضّح دور الانشطار المتباين للميتوكوندريا في صحة خلايا بيتا
لماذا تهم هذه المحطات الصغيرة لتنظيم السكر في الدم
داخل كل خلية من خلايا البنكرياس المنتجة للإنسولين توجد عشرات الميتوكوندريا، محطات الطاقة الصغيرة للخلية. تكمن وظيفتها في تحويل السكر إلى إشارة طاقية تخبر هذه الخلايا بإطلاق الإنسولين للحفاظ على مستوى السكر في الدم. في داء السكري من النوع 2 يتعطل هذا النظام، وغالبًا ما تظهر الميتوكوندريا نفسها تالفة ومجزأة تحت المجهر. تستخدم هذه الدراسة محاكاة حاسوبية متقدمة لطرح سؤال بسيط لكنه مهم: كيف يؤثر أسلوب انقسام الميتوكوندريا وتجددها على الصحة طويلة الأمد لهذه الخلايا وقدرتها على إفراز الإنسولين؟
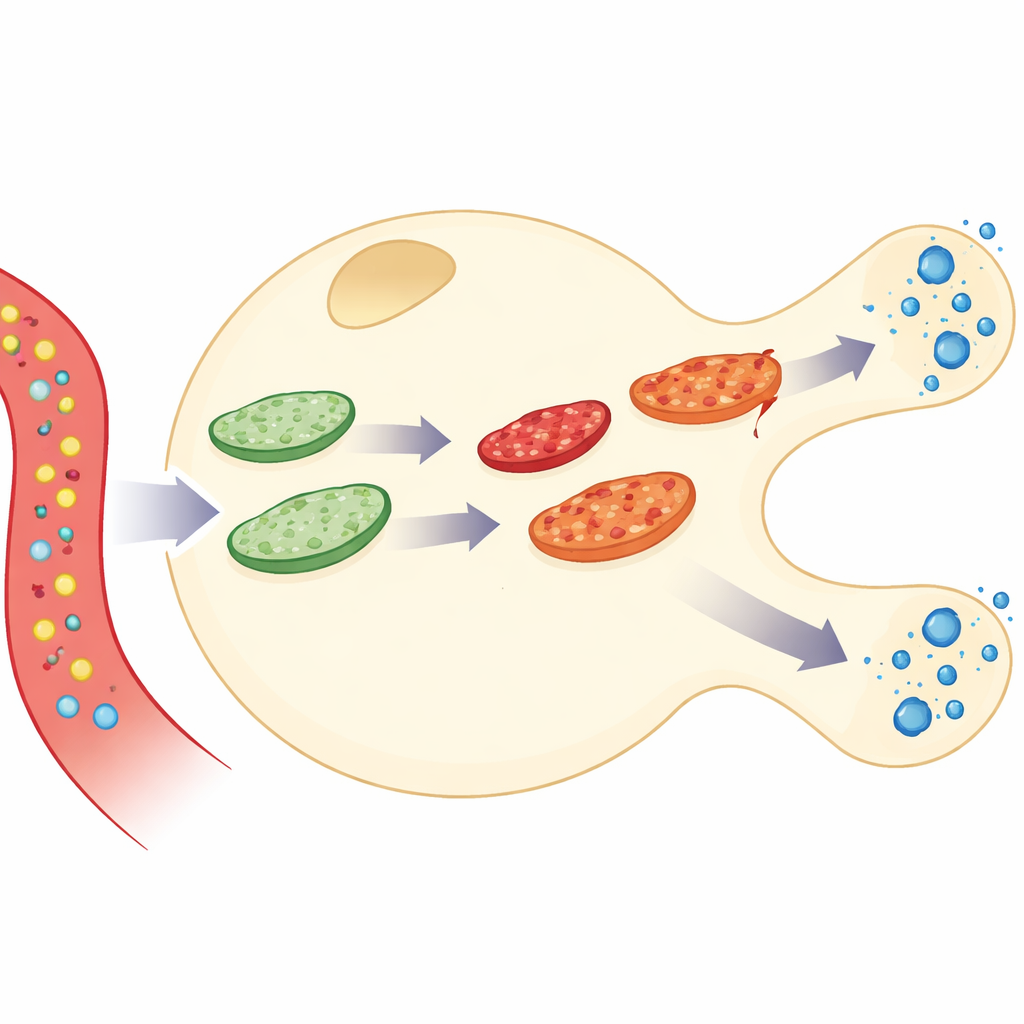
ربط استهلاك الطاقة بإطلاق الإنسولين
بنى المؤلفون محاكاة مفصّلة لخلية بيتا واحدة في البنكرياس، وهو نوع الخلية الذي يصنع ويُفرز الإنسولين. يربط نموذجهم ثلاث طبقات من النشاط: كيف يُحرق الجلوكوز لصنع جزيء الطاقة ATP، وكيف يستجيب الكالسيوم داخل الخلية، وكيف تُفرَج حزمات الإنسولين. بالإضافة إلى ذلك أضافوا «شبكة» ميتوكوندرية ديناميكية تندمج وتتجزأ باستمرار. بدمج هذه الأجزاء، يمكن للنموذج متابعة ما يحدث عند دخول الجلوكوز إلى الخلية، وارتفاع ATP، ونبضات الكالسيوم، وإفراز الإنسولين—بينما تتقدم الميتوكوندريا في العمر، وتراكم الأضرار، وتُصلح، وتُزال.
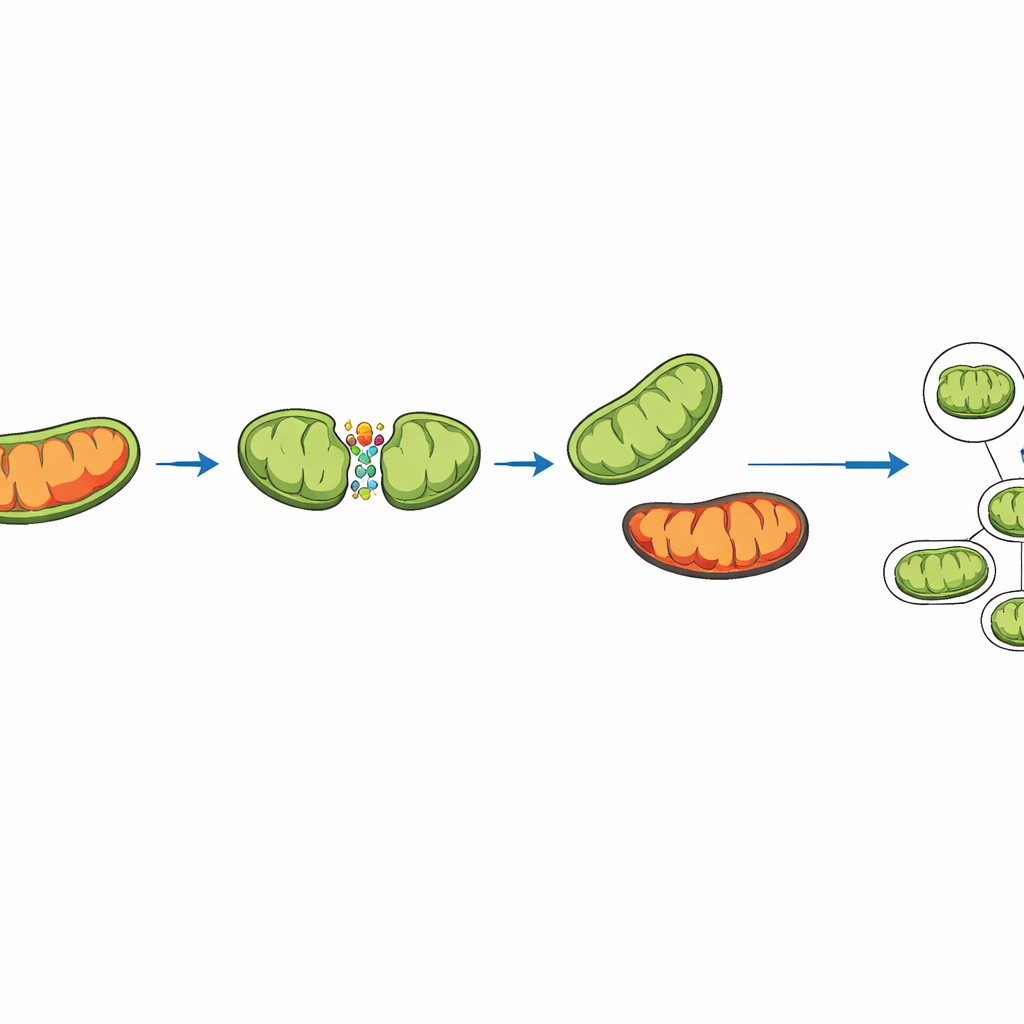
طريقتان لانقسام الميتوكوندريا—ولماذا واحدة تنقذ الموقف
تُظهر تجارب حديثة أن الميتوكوندريا لا تنقسم كلها بنفس الأسلوب. أحيانًا تنقسم بالقرب من المنتصف، فتنتج ميتوكوندريّتين متشابهتين. أحيانًا أخرى تنفصل قطعة صغيرة متضررة بشدة من الطرف، تاركة خلفها جزءًا أكبر وأصح. يلتقط النموذج كلا نوعي الانقسام بتمثيل بروتينات رئيسية تُثبت آلية الانشطار في مواقع مختلفة على سطح الميتوكوندريا. يتتبع النموذج «درجة الضرر» لكل ميتوكوندريون. عند وقوع انقسام طرفي، يُحوَّل قدر إضافي من الضرر عمدًا إلى الشظية الصغيرة. هذه الشظية تكون أكثر عرضة لأن تُبتلع وتُعاد تدويرها بواسطة الخلية، وهي عملية تُسمى البلعمة الميتوكوندرية (mitophagy)، بينما يبقى الجزء الأكبر الأنظف في الشبكة.
كيف يحافظ فرز الأضرار على شباب الشبكة
من خلال تغيير منهجي لمدى قوة فرز الضرر إلى الشظية الصغيرة ومدى التحمل الضرري قبل إزالة الميتوكوندريون، استكشف الباحثون آلاف السيناريوهات الافتراضية. عندما لم يفرِّق الانقسام في توزيع الضرر، انجرفت معظم الميتوكوندريا نحو مستوى تآكل موحد وغير صحي إلى حد كبير. بالمقابل، حتى انحياز طفيف يدفع قدرًا أكبر من الضرر إلى الشظية الصغيرة قلل كثيرًا متوسط الضرر عبر الشبكة. كرّات متكررة من مثل هذا الانقسام غير المتناظر والإزالة الانتقائية خلقت نظامًا ينظف نفسه، حيث ظلت الميتوكوندريا الصحية قادرة على إنتاج ATP بكفاءة.
عند غياب بروتينات الانشطار الرئيسية
بعد ذلك قلّد الفريق تلاعبات تجريبية شائعة. يروج بروتين مرساة واحد، Fis1، في المقام الأول لحدوث الانقسامات الطرفية التي تركز الضرر في شظايا صغيرة. أدى تقليل Fis1 في النموذج إلى قلة الانقسامات الطرفية، وميتوكوندريا أكثر تضررًا بشكل موحد، وانهيار في صحة الشبكة. أما مرساة أخرى، MFF، فتميل إلى الانقسامات المنتصفية التي تُنتج بنتين متشابهتين. أدى خفض MFF إلى تغييرات طفيفة فقط في مستويات الضرر لكنه أنتج ميتوكوندريا أكبر وأكثر اندماجًا، ما يتطابق مع ملاحظات المختبر بأن هذا المسار مرتبط أكثر بتحضير الخلايا للانقسام منه بتنظيف الضرر. عندما نُقص البروتين المركزي للانشطار Drp1، تكاد تحدث الانقسامات من الأساس. في تلك الحالة ارتفعت الأضرار إلى مستوى يقترب من الحد الأقصى الممكن، تاركة الشبكة متدهورة بشدة.
من ميتوكوندريا متعبة إلى إفراز إنسولين ضعيف
نظرًا لأن النموذج يربط صحة الميتوكوندريا بإنتاج ATP، يمكنه التنبؤ بكيفية تأثير هذه التغيرات الهيكلية على إفراز الإنسولين. مع فقدان معتدل لـ Fis1، استمرت الخلية في إفراز الإنسولين على مستوى منخفض عند الجلوكوز المنخفض، لكن استجابتها للجلوكوز المرتفع تراجعت—مماثلة لخلايا بيتا من أشخاص في المراحل المبكرة من المرض الأيضي. مع فقدان كبير لـ Drp1، أصبحت الخلية شبه غير مستجيبة للجلوكوز: ظل إفراز الإنسولين قريبًا من مستوى أساسي منخفض حتى عندما كان السكر مرتفعًا. تشبه هذه الأنماط النتائج التجريبية المبلغ عنها وتشير إلى أن التعبير المتوازن لبروتينات الانشطار ضروري للحفاظ على خلايا بيتا نشطة ومستجيبة.
ما مغزى هذا لفهم داء السكري
للقارئ العام، رسالة الدراسة هي أن طريقة تفكك الميتوكوندريا لا تقل أهمية عن طريقتها في توليد الطاقة. «الانقسام الجيد» المضبوط بعناية يقص الأجزاء التالفة ويحافظ على شباب الشبكة، داعمًا إفراز إنسولين قويًا. عندما يضعف هذا الآلية أو تُوقف، تتراكم الميتوكوندريا التالفة، يتعطل إنتاج ATP، وتكافح خلايا بيتا للاستجابة لارتفاع سكر الدم. من خلال تجسيد هذه الروابط في نموذج حاسوبي مرن، يوفر العمل بيئة اختبار للأفكار المستقبلية حول كيفية حماية أو استعادة جودة الميتوكوندريا في داء السكري، مما قد يوجّه علاجات جديدة تساعد خلايا بيتا على البقاء صحية لفترة أطول.
الاستشهاد: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
الكلمات المفتاحية: الميتوكوندريا, إفراز الإنسولين, خلايا بيتا, داء السكري من النوع 2, نمذجة حاسوبية