Clear Sky Science · fr
Un modèle de simulation basé sur des règles éclaire le rôle de la fission mitochondriale asymétrique sur la santé des cellules bêta
Pourquoi ces petites centrales comptent pour la glycémie
À l’intérieur de chaque cellule productrice d’insuline du pancréas se trouvent des dizaines de mitochondries, ces mini‑centrales énergétiques de la cellule. Leur rôle est de transformer le glucose en signal énergétique qui indique à ces cellules de libérer de l’insuline et de maintenir la glycémie. Dans le diabète de type 2, ce système se dérègle, et les mitochondries apparaissent souvent abîmées et fragmentées au microscope. Cette étude utilise des simulations informatiques avancées pour poser une question simple mais importante : de quelle manière la façon dont les mitochondries se divisent et se renouvellent affecte‑t‑elle la santé à long terme de ces cellules et leur capacité à sécréter de l’insuline ?
Relier l’utilisation d’énergie à la sécrétion d’insuline
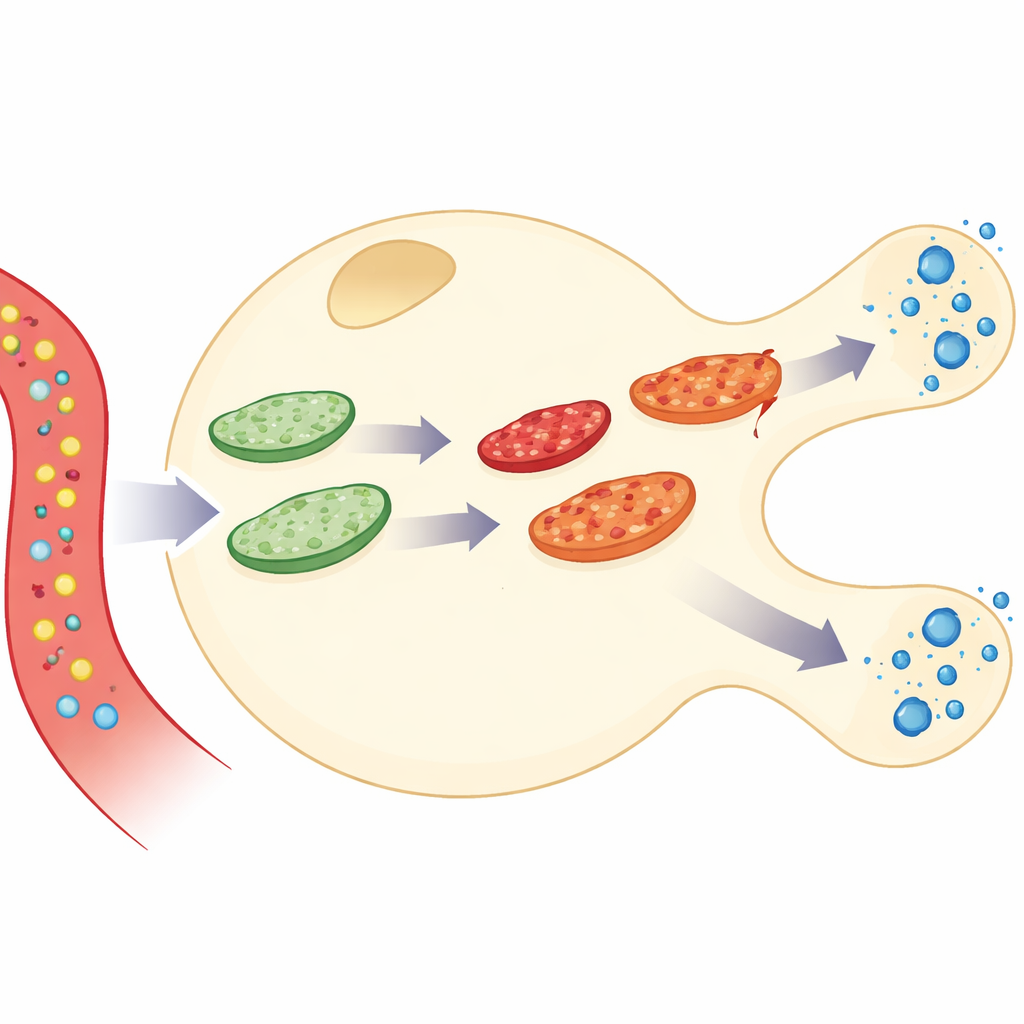
Les auteurs ont construit une simulation détaillée d’une seule cellule bêta pancréatique, le type cellulaire qui fabrique et sécrète l’insuline. Leur modèle relie trois niveaux d’activité : la combustion du glucose pour produire la molécule énergétique ATP, la réponse du calcium intracellulaire, et la libération des granules d’insuline. Par‑dessus cela, ils ont ajouté un « réseau » mitochondrial dynamique qui fusionne et se scinde en permanence. En combinant ces éléments, le modèle peut suivre ce qui se passe lorsqu’un apport en glucose fait monter l’ATP, que le calcium pulse et que l’insuline est sécrétée — tandis que les mitochondries elles‑mêmes vieillissent, accumulent des dommages, se réparent et sont éliminées.
Deux façons de se diviser — et pourquoi l’une sauve la situation
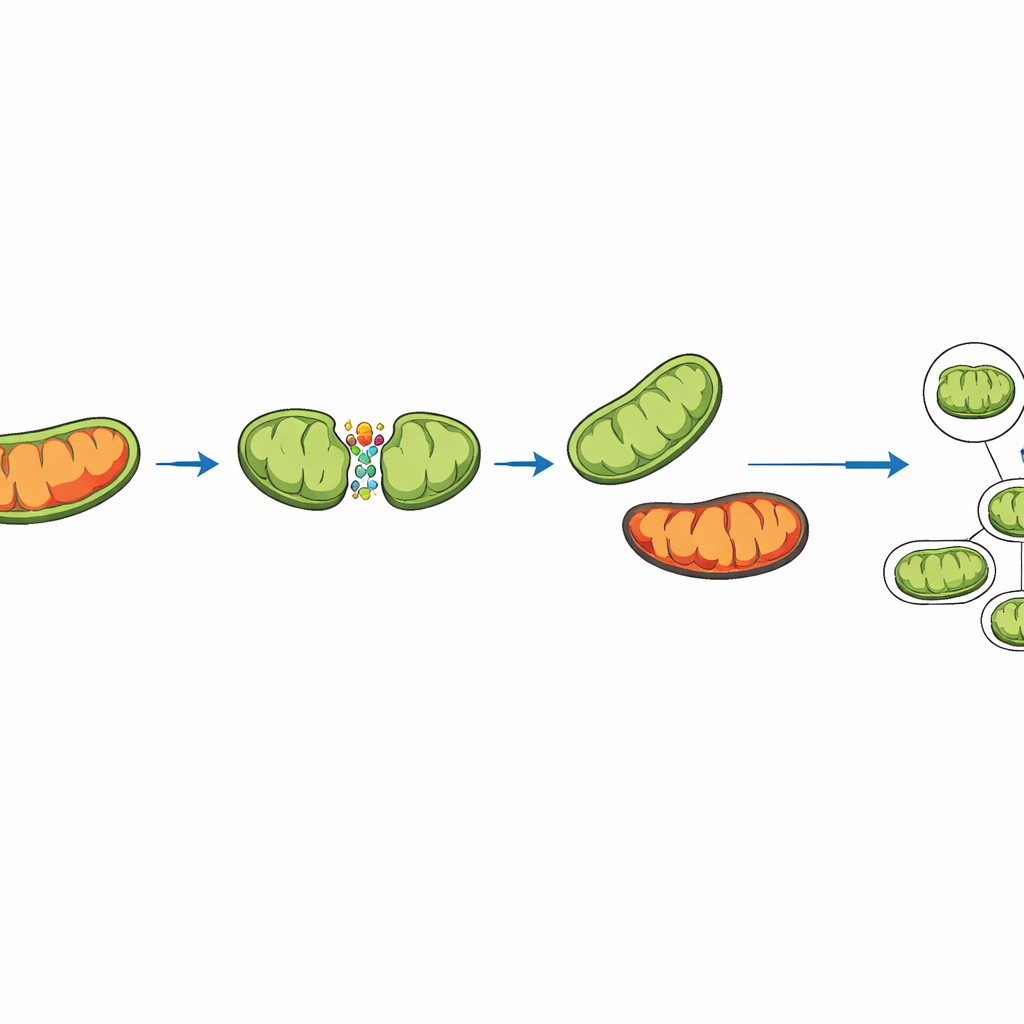
Des expériences récentes montrent que les mitochondries ne se divisent pas toutes de la même manière. Parfois, elles se scindent près du milieu, donnant deux mitochondries filles similaires. D’autres fois, elles se détachent au niveau d’une petite extrémité fortement endommagée, laissant derrière elles une partie plus grande et plus saine. La simulation capture ces deux types de fission en représentant des protéines clés qui ancrent la machinerie de fission à différents endroits de la surface mitochondriale. Dans le modèle, un « score de dommage » est suivi pour chaque mitochondrie. Lors d’une fission périphérique, un excès de dommage est volontairement orienté vers le petit fragment. Ce fragment a davantage de chances d’être phagocyté et recyclé par la cellule, un processus appelé mitophagie, tandis que le fragment plus grand et plus propre reste dans le réseau.
Comment le tri des dommages maintient le réseau jeune
En faisant varier systématiquement l’intensité du tri des dommages vers le petit fragment et le seuil de dommage au‑delà duquel une mitochondrie est éliminée, les chercheurs ont exploré des milliers de scénarios virtuels. Lorsque la fission ne triât pas les dommages, presque toutes les mitochondries dérivaient vers le même niveau plutôt malsain d’usure. En revanche, même un léger biais qui dirigeait un peu plus de dommages vers le petit fragment réduisait fortement le dommage moyen dans le réseau. Des cycles répétés de fission asymétrique et d’élimination sélective créaient un système d’auto‑nettoyage, où les mitochondries saines restaient capables de produire l’ATP efficacement.
Quand des protéines clés de fission manquent
L’équipe a ensuite simulé des manipulations expérimentales courantes. Une protéine d’ancrage, Fis1, favorise principalement les événements de fission périphérique qui concentrent les dommages dans de petits fragments. Réduire Fis1 dans le modèle entraînait moins de fissions périphériques, des mitochondries plus uniformément endommagées et une détérioration de la santé du réseau. Un autre ancrage, MFF, favorise les fissions en zone médiane qui produisent des filles similaires. Diminuer MFF provoquait seulement de légers changements dans les niveaux de dommage mais donnait des mitochondries plus grosses et plus fusionnées, concordant avec des observations en laboratoire montrant que cette voie est davantage liée à la préparation à la division cellulaire qu’au nettoyage des dommages. Lorsque la protéine centrale de fission Drp1 était diminuée, la fission était presque entièrement arrêtée. Les dommages montaient alors près du maximum possible, laissant le réseau fortement compromis.
Des mitochondries fatiguées à une sécrétion d’insuline défaillante
Parce que le modèle relie la santé mitochondriale à la production d’ATP, il peut prédire comment ces changements structurels affectent la sécrétion d’insuline. Avec une perte modérée de Fis1, la cellule libérait encore de l’insuline à faible glucose, mais sa réponse au glucose élevé était atténuée — semblable aux cellules bêta de personnes en début de maladie métabolique. Avec une perte marquée de Drp1, la cellule devenait presque non réactive au glucose : la sécrétion d’insuline restait proche d’un niveau basal faible même lorsque le sucre était élevé. Ces profils ressemblent aux résultats expérimentaux rapportés et suggèrent qu’une expression équilibrée des protéines de fission est essentielle pour maintenir les cellules bêta à la fois énergisées et réactives.
Ce que cela signifie pour la compréhension du diabète
Pour un non‑spécialiste, le message de l’étude est que la manière dont les mitochondries se fragmentent est aussi importante que leur capacité à produire de l’énergie. Une « bonne cassure » finement réglée supprime les morceaux endommagés et garde le réseau jeune, soutenant une forte sécrétion d’insuline. Lorsque ce mécanisme d’élagage est affaibli ou arrêté, les mitochondries endommagées s’accumulent, la production d’ATP décline et les cellules bêta peinent à répondre à l’augmentation de la glycémie. En capturant ces liens dans un modèle informatique flexible, ce travail offre un terrain d’essai pour des idées futures visant à protéger ou restaurer la qualité mitochondriale dans le diabète, orientant potentiellement de nouveaux traitements pour aider les cellules bêta à rester en bonne santé plus longtemps.
Citation: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Mots-clés: mitochondries, sécrétion d'insuline, cellules bêta, diabète de type 2, modélisation informatique