Clear Sky Science · nl
Een regelgebaseerd simulatiemodel verheldert de rol van asymmetrische mitochondriale splitsing voor de gezondheid van bètacellen
Waarom kleine energiecentrales ertoe doen voor de bloedsuiker
In elke insulineproducerende cel van de alvleesklier zitten tientallen mitochondriën, de miniatuur energiecentrales van de cel. Hun taak is suiker om te zetten in het energiemolecuul dat deze cellen aanzet tot insulineafgifte en zo de bloedsuiker reguleert. Bij type 2 diabetes faalt dit systeem vaak, en onder de microscoop zien de mitochondriën er vaak beschadigd en gefragmenteerd uit. Deze studie gebruikt geavanceerde computersimulaties om een eenvoudige maar belangrijke vraag te stellen: hoe beïnvloedt de manier waarop mitochondriën zich splitsen en vernieuwen de gezondheid van deze cellen op de lange termijn en hun vermogen om insuline af te geven?
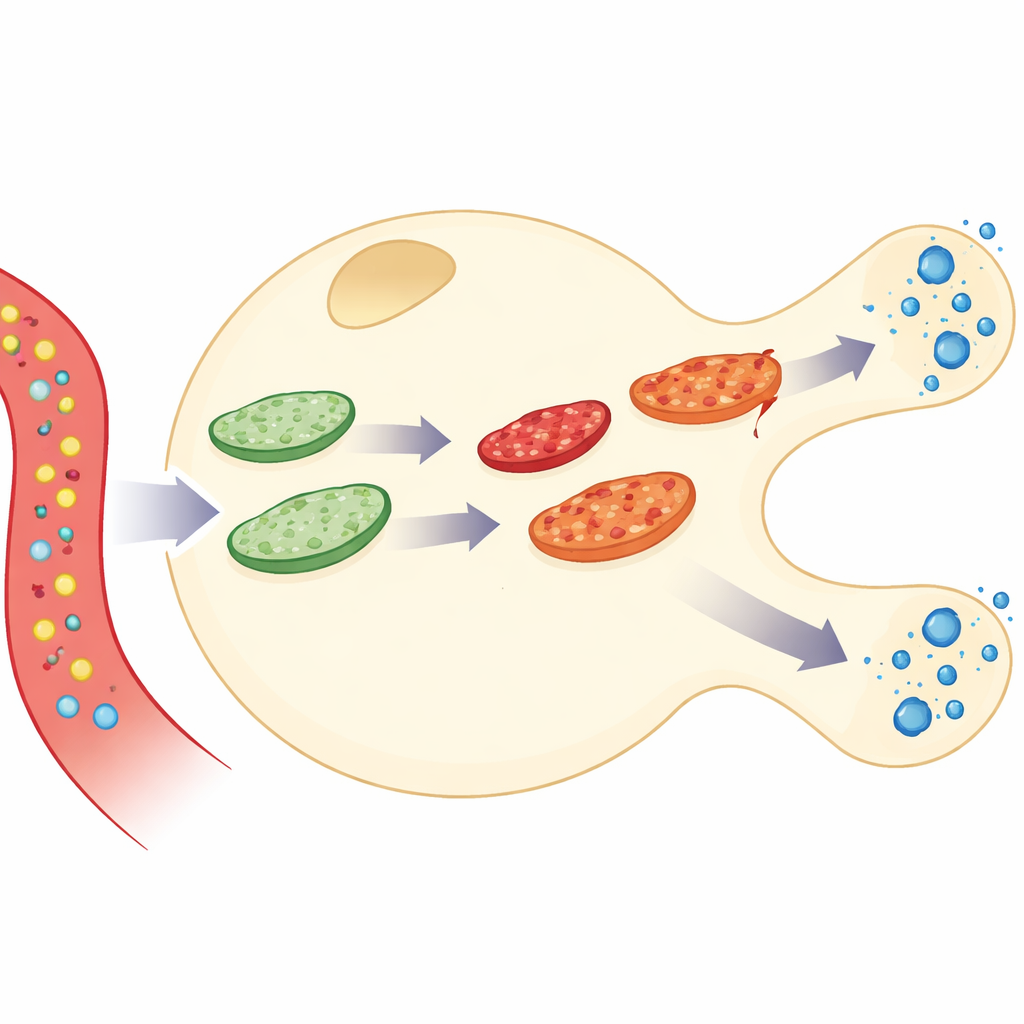
De koppeling tussen energieverbruik en insulineafgifte
De auteurs bouwden een gedetailleerde simulatie van een enkele pancreatische bètacel, het celtype dat insuline maakt en afgeeft. Hun model verbindt drie activiteitslagen: hoe glucose wordt verbrand om het energiemolecuul ATP te maken, hoe calcium in de cel daarop reageert, en hoe insulineblaasjes worden vrijgegeven. Daarbovenop voegden ze een dynamisch mitochondriaal "netwerk" toe dat voortdurend fuseert en uiteenvalt. Door deze onderdelen te combineren kan het model volgen wat er gebeurt wanneer glucose de cel binnenkomt, ATP stijgt, calcium pulsen vertoont en insuline wordt afgescheiden—terwijl de mitochondriën zelf verouderen, schade opeenstapelen, herstellen en worden verwijderd.
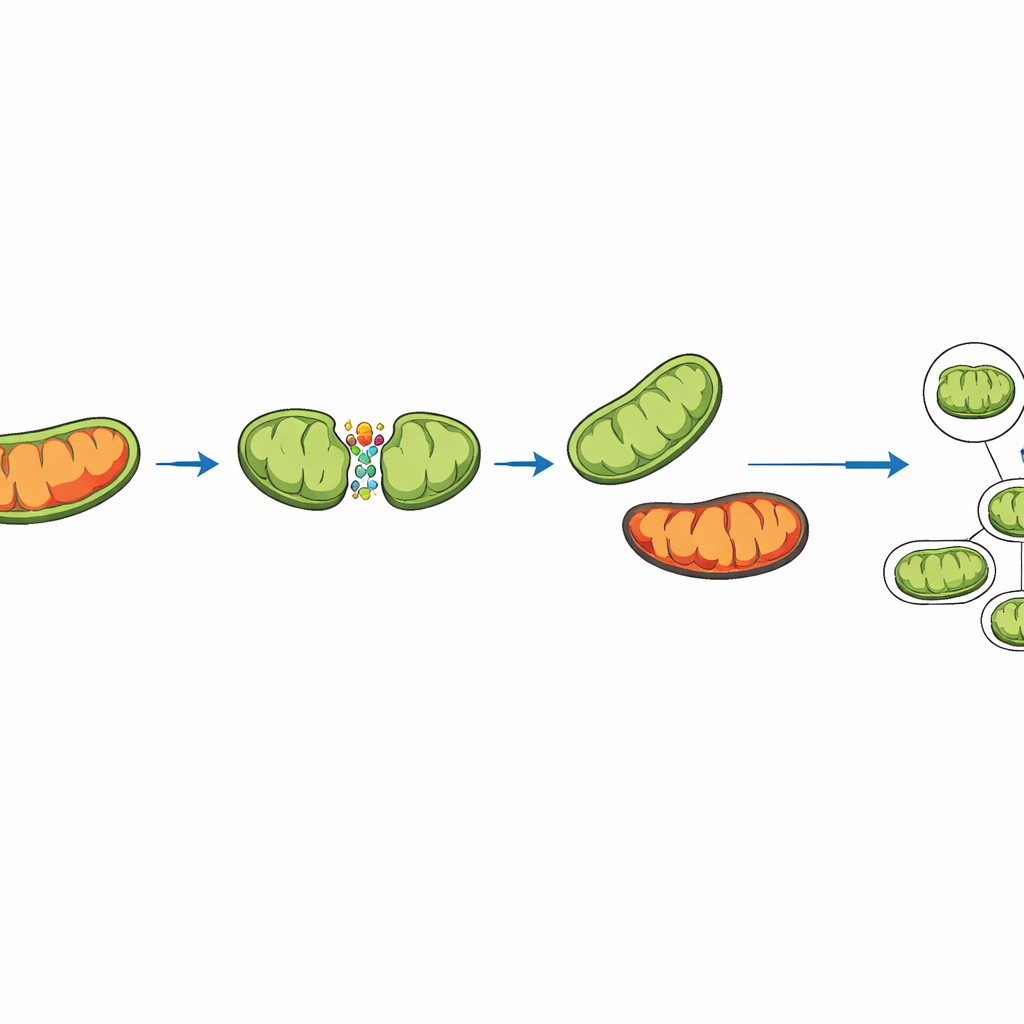
Twee manieren van splitsen van mitochondriën — en waarom één redding brengt
Recente experimenten tonen dat mitochondriën niet allemaal op dezelfde manier delen. Soms splitsen ze nabij het midden, waardoor twee vergelijkbare dochter‑mitochondriën ontstaan. Andere keren delen ze een kleine, sterk beschadigde punt af, waarbij een groter, gezonder deel overblijft. De simulatie vat beide typen splitsing samen door sleutelproteïnen te representeren die de fission‑machinerie op verschillende plekken aan het mitochondriale oppervlak ankeren. In het model wordt voor elk mitochondrion een "schadescore" bijgehouden. Wanneer een perifere splitsing optreedt, wordt extra schade doelbewust in het kleine fragment geduwd. Dit fragment wordt eerder opgenomen en gerecycled door de cel via mitophagie, terwijl het grotere, schonere fragment in het netwerk blijft.
Hoe schadesortering het netwerk jong houdt
Door systematisch te variëren hoe sterk schade naar het kleine fragment wordt doorgesorteerd en hoe beschadigd een mitochondrion mag worden voordat het wordt verwijderd, verkenden de onderzoekers duizenden virtuele scenario's. Wanneer splitsing geen schade sorteerde, dreigden bijna alle mitochondriën naar hetzelfde, tamelijk ongezonde niveau van slijtage te drijven. In contrast verminderde zelfs een bescheiden bias die iets meer schade naar het kleine fragment duwde de gemiddelde schade in het netwerk aanzienlijk. Herhaalde rondes van dergelijke asymmetrische splitsing en selectieve verwijdering creëerden een zelfreinigend systeem, waarin gezonde mitochondriën in staat bleven om efficiënt ATP te produceren.
Wanneer sleutelproteïnen voor splitsing ontbreken
Het team imiteerde vervolgens veelvoorkomende experimentele manipulaties. Eén ankerprotein, Fis1, bevordert voornamelijk perifere fission‑gebeurtenissen die schade concentreren in kleine fragmenten. Het verlagen van Fis1 in het model leidde tot minder perifere splitsingen, meer uniform beschadigde mitochondriën en een instorting van de netwerkgeneeslijkheid. Een ander anker, MFF, bevordert midzone‑splitsingen die vergelijkbare dochters produceren. Verlaging van MFF veroorzaakte slechts milde veranderingen in schadeniveaus maar resulteerde in grotere, meer gefuseerde mitochondriën, wat overeenkomt met laboratoriumwaarnemingen dat dit pad meer te maken heeft met het voorbereiden van cellen op deling dan met schadeverwijdering. Wanneer het kernfibrillatie‑proteïne Drp1 werd verlaagd, stopte splitsing vrijwel geheel. De schade nam toen toe tot bijna het maximale, waardoor het netwerk ernstig aangetast raakte.
Van vermoeide mitochondriën naar verminderde insulineafgifte
Aangezien het model de gezondheid van mitochondriën koppelt aan ATP‑output, kan het voorspellen hoe deze structurele veranderingen insulineafgifte beïnvloeden. Bij een matig verlies van Fis1 gaf de cel nog insuline af bij lage glucose, maar was de reactie op hoge glucose afgezwakt—vergelijkbaar met bètacellen van mensen in vroege metabole ziekte. Bij sterke vermindering van Drp1 werd de cel vrijwel ongevoelig voor glucose: de insulineafgifte bleef rond een laag basaalniveau, zelfs wanneer de suikerhoogte toenam. Deze patronen lijken op gerapporteerde experimentele resultaten en suggereren dat een gebalanceerde expressie van de fission‑proteïnen essentieel is om bètacellen zowel energiek als responsief te houden.
Wat dit betekent voor het begrijpen van diabetes
Voor een leek is de boodschap van de studie dat de manier waarop mitochondriën uit elkaar vallen even belangrijk is als hoe ze energie produceren. Een zorgvuldig afgestemde "goede breuk" snoeit beschadigde stukjes weg en houdt het netwerk jong, wat sterke insulineafgifte ondersteunt. Wanneer dat snoeimechanisme verzwakt of wordt uitgeschakeld, stapelen beschadigde mitochondriën zich op, hapert de ATP‑productie en hebben bètacellen moeite te reageren op stijgende bloedsuikers. Door deze verbanden vast te leggen in een flexibel computermodel, biedt het werk een testomgeving voor toekomstige ideeën over hoe mitochondriale kwaliteit bij diabetes beschermd of hersteld kan worden, mogelijk richtinggevend voor nieuwe behandelingen die bètacellen helpen langer gezond te blijven.
Bronvermelding: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Trefwoorden: mitochondriën, insulineafgifte, bètacellen, type 2 diabetes, computermodelering