Clear Sky Science · es
Un modelo de simulación basado en reglas ilumina el papel de la fisión mitocondrial asimétrica en la salud de las células beta
Por qué importan estos pequeños generadores para el azúcar en sangre
Dentro de cada célula pancreática productora de insulina hay docenas de mitocondrias, las pequeñas centrales energéticas de la célula. Su tarea es convertir la glucosa en la señal energética que indica a estas células que liberen insulina y mantengan el azúcar en sangre bajo control. En la diabetes tipo 2, este sistema falla y las mitocondrias a menudo parecen deterioradas y fragmentadas al microscopio. Este estudio usa simulaciones informáticas avanzadas para preguntar algo simple pero importante: ¿cómo afecta la manera en que las mitocondrias se dividen y se renuevan a la salud a largo plazo de estas células y a su capacidad para liberar insulina?
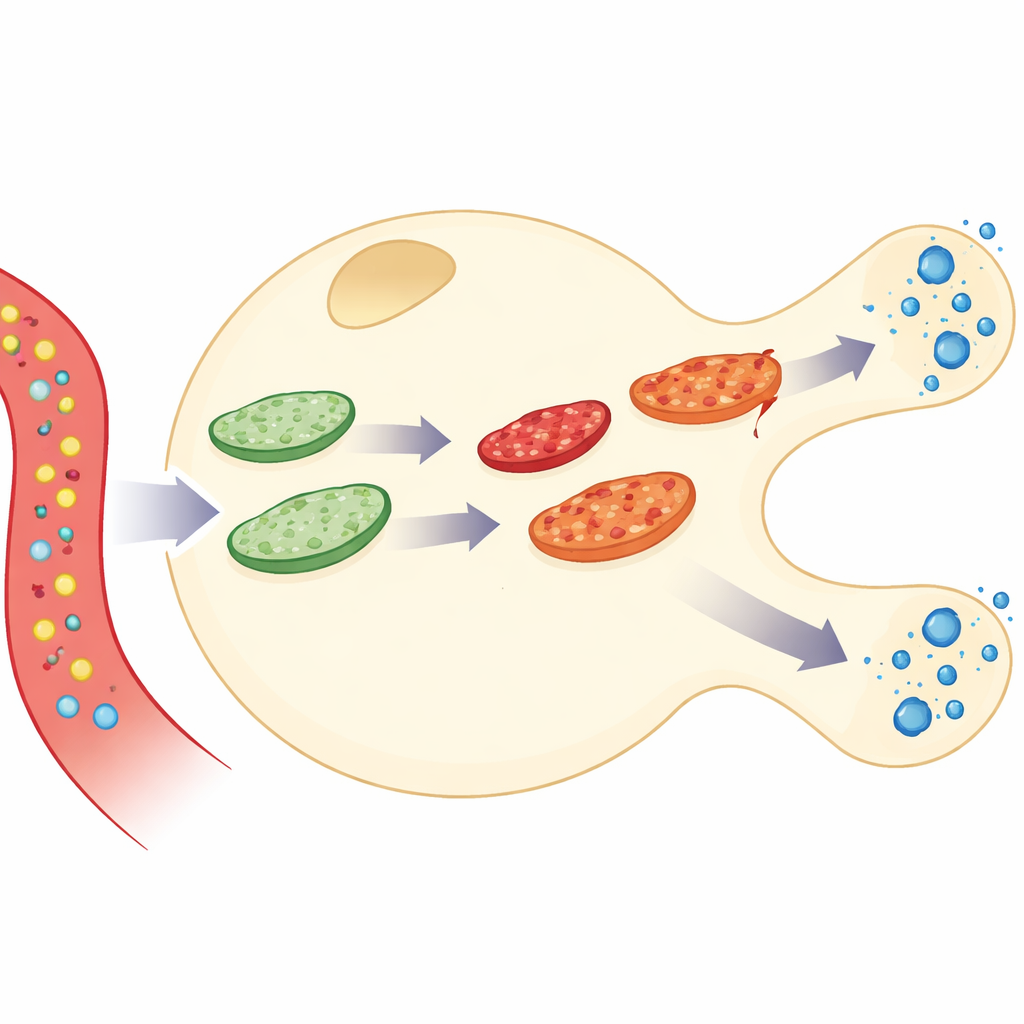
Conectando el uso de energía con la liberación de insulina
Los autores construyeron una simulación detallada de una sola célula beta pancreática, el tipo celular que produce y secreta insulina. Su modelo vincula tres capas de actividad: cómo se quema la glucosa para generar la molécula energética ATP, cómo responde el calcio intracelular y cómo se liberan los gránulos de insulina. Sobre esto añadieron una “red” mitocondrial dinámica que constantemente se fusiona y se fragmenta. Al combinar estas partes, el modelo puede seguir lo que ocurre cuando entra glucosa a la célula, sube el ATP, aparecen pulsos de calcio y se secreta insulina—mientras las propias mitocondrias envejecen, acumulan daño, se reparan y son eliminadas.
Dos formas de fisión mitocondrial—y por qué una salva la situación
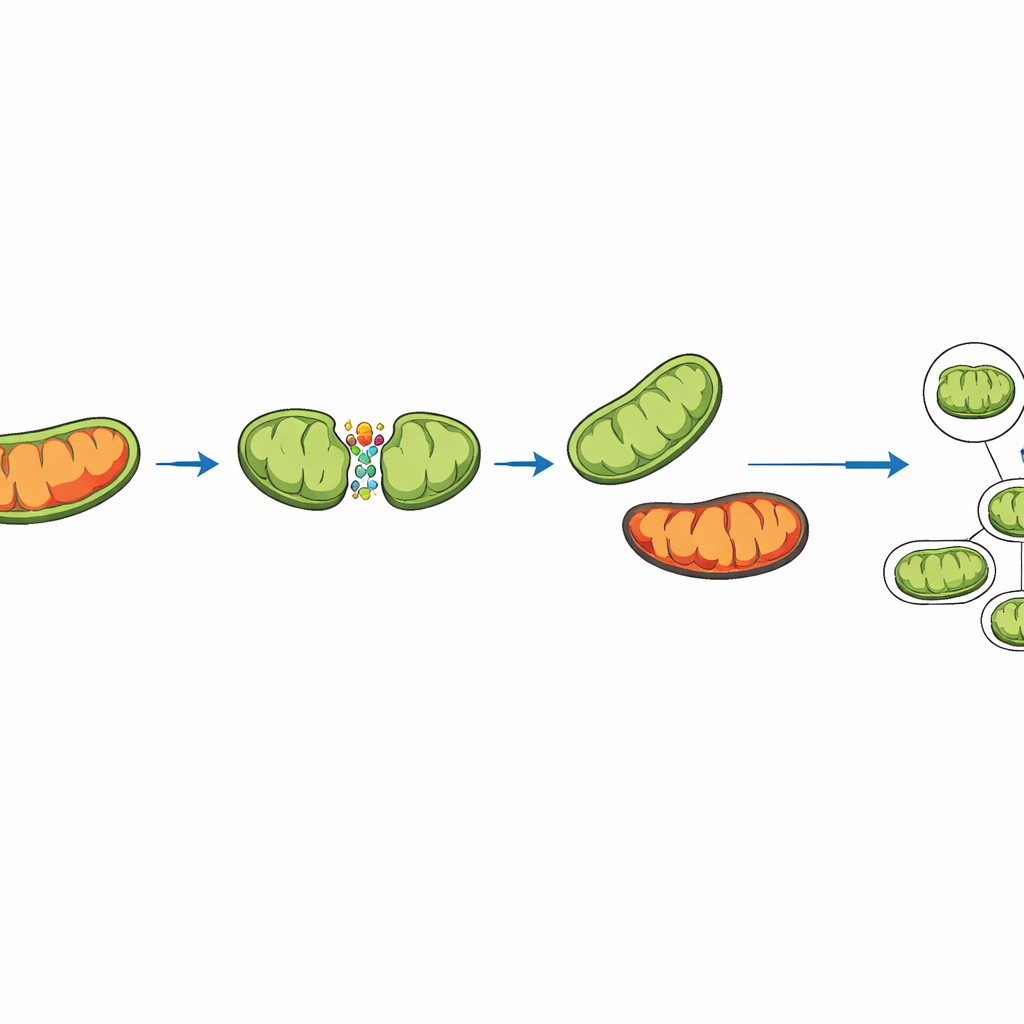
Experimentos recientes muestran que las mitocondrias no siempre se dividen de la misma manera. A veces se parten por la zona media, dando lugar a dos mitocondrias hijas similares. Otras veces se separa una pequeña punta muy dañada del extremo, dejando atrás un fragmento más grande y saludable. La simulación captura ambos tipos de fisión representando proteínas clave que anclan la maquinaria de fisión en distintos puntos de la superficie mitocondrial. En el modelo se sigue una “puntuación de daño” para cada mitocondria. Cuando ocurre una fisión periférica, el daño extra se canaliza deliberadamente hacia el fragmento pequeño. Este fragmento tiene más probabilidades de ser devorado y reciclado por la célula, un proceso llamado mitofagia, mientras que el fragmento mayor y más limpio permanece en la red.
Cómo el ordenamiento del daño mantiene la red joven
Variando sistemáticamente cuánto se concentra el daño en el fragmento pequeño y cuán dañada puede estar una mitocondria antes de ser eliminada, los investigadores exploraron miles de escenarios virtuales. Cuando la fisión no ordenaba el daño, casi todas las mitocondrias derivaban hacia el mismo nivel, bastante malsano, de desgaste. En contraste, incluso un sesgo modesto que empujara un poco más de daño hacia el fragmento pequeño redujo en gran medida el daño medio de la red. Rondas repetidas de esta fisión asimétrica y eliminación selectiva crearon un sistema de auto-limpieza, en el que las mitocondrias sanas seguían siendo capaces de producir ATP de forma eficiente.
Cuando faltan proteínas clave de la fisión
El equipo simuló entonces manipulaciones experimentales comunes. Una proteína ancla, Fis1, promueve principalmente los eventos de fisión periférica que concentran el daño en pequeños fragmentos. Reducir Fis1 en el modelo condujo a menos fisiones periféricas, mitocondrias con daño más uniforme y un colapso de la salud de la red. Otro ancla, MFF, favorece las fisiones en la zona media que producen hijas similares. Bajar MFF causó sólo cambios leves en los niveles de daño pero generó mitocondrias más grandes y fusionadas, coincidiendo con observaciones de laboratorio que indican que esta vía tiene más que ver con preparar las células para dividirse que con eliminar daño. Cuando se redujo la proteína central de fisión Drp1, la división casi se detuvo por completo. Entonces el daño subió cerca del máximo posible, dejando la red seriamente comprometida.
De mitocondrias fatigadas a una pobre liberación de insulina
Porque el modelo vincula la salud mitocondrial con la producción de ATP, puede predecir cómo estos cambios estructurales afectan la secreción de insulina. Con una pérdida moderada de Fis1, la célula aún liberaba insulina a glucosa baja, pero su respuesta a glucosa alta se atenuó—similar a las células beta de personas con enfermedad metabólica temprana. Con una pérdida fuerte de Drp1, la célula se volvió casi no receptiva a la glucosa: la liberación de insulina se mantuvo cerca de un nivel basal bajo incluso cuando el azúcar era alto. Estos patrones se parecen a resultados experimentales reportados y sugieren que una expresión equilibrada de las proteínas de fisión es esencial para mantener las células beta tanto energizadas como sensibles.
Lo que esto significa para entender la diabetes
Para un lector no especializado, el mensaje del estudio es que la forma en que las mitocondrias se parten es tan importante como la forma en que generan energía. Una “buena rotura” finamente ajustada recorta las piezas dañadas y mantiene la red joven, apoyando una fuerte liberación de insulina. Cuando ese mecanismo de recorte se debilita o se detiene, las mitocondrias dañadas se acumulan, la producción de ATP falla y las células beta tienen dificultades para responder al aumento de glucosa en sangre. Al capturar estos vínculos en un modelo informático flexible, el trabajo ofrece un banco de pruebas para futuras ideas sobre cómo proteger o restaurar la calidad mitocondrial en la diabetes, orientando potencialmente nuevos tratamientos que ayuden a que las células beta se mantengan saludables por más tiempo.
Cita: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Palabras clave: mitocondrias, secreción de insulina, células beta, diabetes tipo 2, modelización por ordenador