Clear Sky Science · de
Ein regelbasiertes Simulationsmodell beleuchtet die Rolle asymmetrischer mitochondrialer Spaltung für die Gesundheit von Beta‑Zellen
Warum winzige Kraftwerke für den Blutzucker wichtig sind
In jeder insulinproduzierenden Zelle der Bauchspeicheldrüse sitzen Dutzende Mitochondrien, die kleinen Kraftwerke der Zelle. Ihre Aufgabe ist es, Zucker in das Energiesignal umzuwandeln, das diese Zellen veranlasst, Insulin freizusetzen und so den Blutzucker zu regulieren. Bei Typ‑2‑Diabetes gerät dieses System aus dem Gleichgewicht, und die Mitochondrien erscheinen unter dem Mikroskop oft zerstört und fragmentiert. Diese Studie nutzt fortgeschrittene Computersimulationen, um eine einfache, aber wichtige Frage zu stellen: Wie beeinflusst die Art und Weise, wie Mitochondrien sich teilen und erneuern, die langfristige Gesundheit dieser Zellen und ihre Fähigkeit, Insulin freizusetzen?
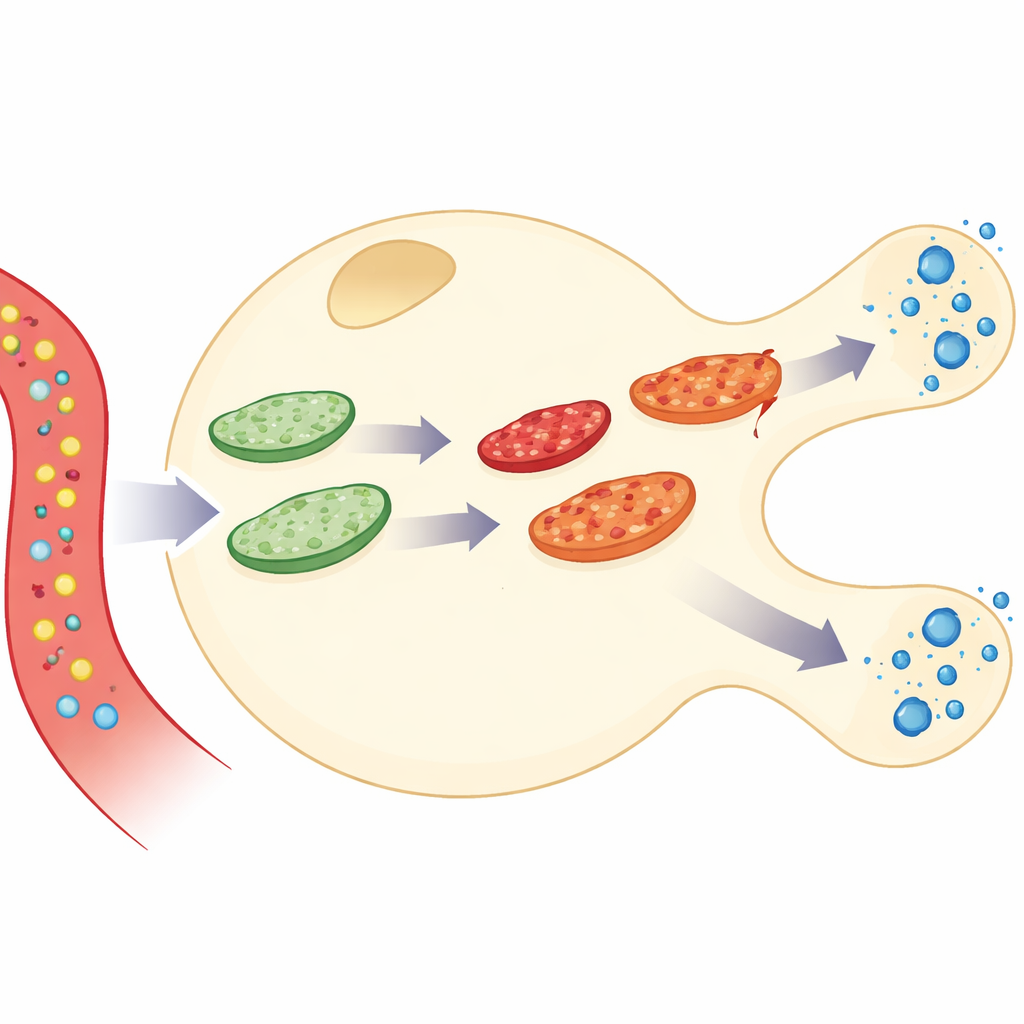
Die Verbindung von Energieverbrauch und Insulinausschüttung
Die Autoren bauten eine detaillierte Simulation einer einzelnen Pankreas‑Beta‑Zelle, des Zelltyps, der Insulin herstellt und ausschüttet. Ihr Modell verknüpft drei Aktivitätsebenen: wie Glukose verbrannt wird, um das Energiemolekül ATP zu erzeugen, wie Calcium im Zellinneren reagiert, und wie Insulinpakete freigesetzt werden. Darüber legten sie ein dynamisches mitochondriales "Netzwerk", das ständig miteinander verschmilzt und sich wieder aufteilt. Durch die Kombination dieser Teile kann das Modell verfolgen, was passiert, wenn Glukose in die Zelle gelangt, ATP ansteigt, Calcium pulsiert und Insulin ausgeschüttet wird — während die Mitochondrien selbst altern, Schäden anhäufen, repariert und entfernt werden.
Zwei Arten der mitochondrialen Spaltung — und warum eine den Unterschied macht
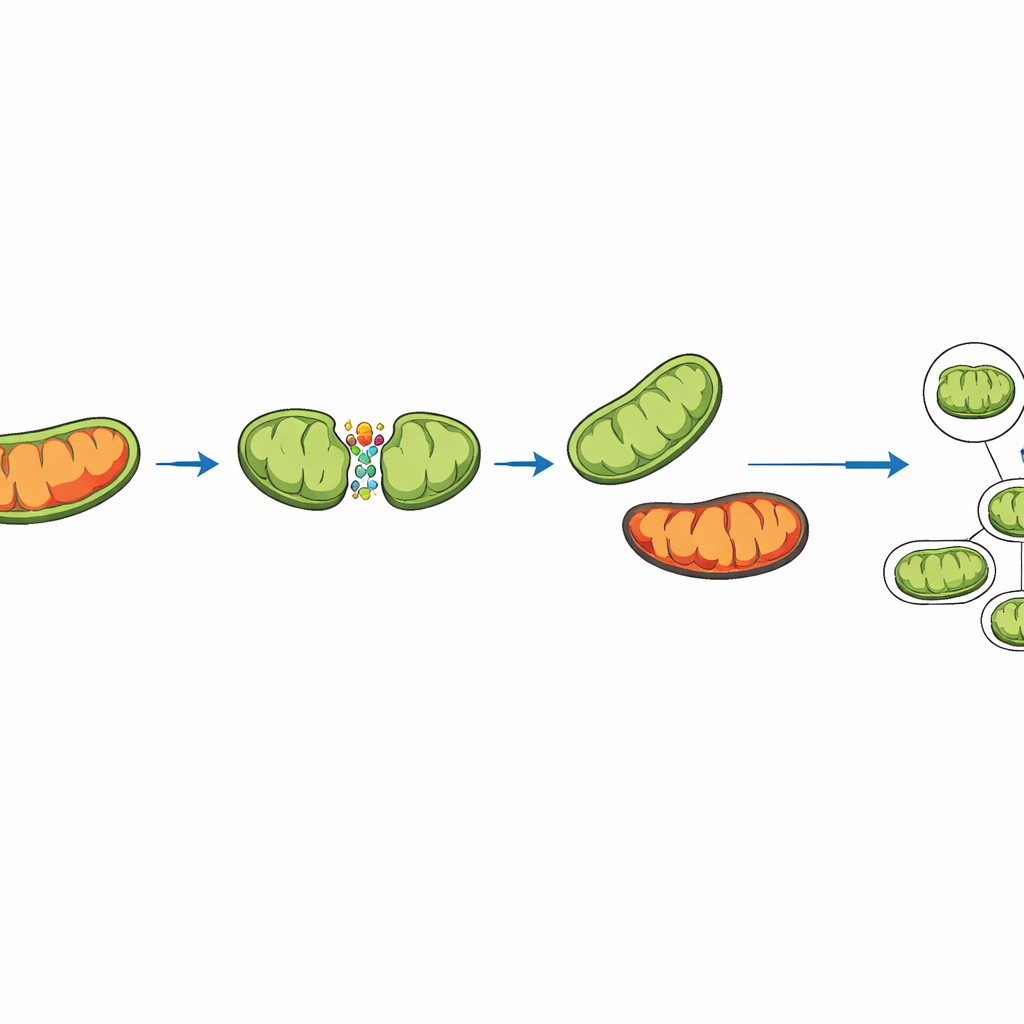
Neuere Experimente zeigen, dass Mitochondrien nicht alle auf dieselbe Weise geteilt werden. Manchmal spalten sie sich in der Mitte und erzeugen zwei ähnliche Tochter‑Mitochondrien. Andere Male schneiden sie ein kleines, stark beschädigtes Ende ab und hinterlassen ein größeres, gesünderes Stück. Die Simulation erfasst beide Spaltungsarten, indem sie Schlüsselproteine darstellt, die die Fissionsmaschinerie an verschiedenen Stellen der mitochondrialen Oberfläche verankern. Im Modell wird für jedes Mitochondrium ein "Schadensscore" verfolgt. Tritt eine periphere Spaltung auf, wird zusätzlicher Schaden absichtlich in das kleine Fragment umgeleitet. Dieses Fragment wird eher von der Zelle verschlungen und recycelt — ein Prozess, der als Mitophagie bezeichnet wird — während das größere, sauberere Fragment im Netzwerk verbleibt.
Wie Schadenssortierung das Netzwerk jung hält
Indem die Forschenden systematisch variierten, wie stark Schaden in das kleine Fragment sortiert wird und wie beschädigt ein Mitochondrium sein darf, bevor es entfernt wird, untersuchten sie Tausende virtueller Szenarien. Wenn die Spaltung den Schaden nicht sortierte, drifteten nahezu alle Mitochondrien auf dasselbe, eher ungesunde Ausmaß an Verschleiß zu. Im Gegensatz dazu senkte bereits eine moderate Verzerrung, die etwas mehr Schaden in das kleine Fragment schob, den durchschnittlichen Schaden im Netzwerk deutlich. Wiederholte Zyklen solcher asymmetrischen Spaltung und selektiven Entfernung schufen ein sich selbst reinigendes System, in dem gesunde Mitochondrien weiterhin effizient ATP produzieren konnten.
Wenn Schlüsselproteine der Spaltung fehlen
Das Team ahmte anschließend gängige experimentelle Manipulationen nach. Ein Verankerungsprotein, Fis1, fördert hauptsächlich periphere Spaltungsvorgänge, die Schäden in kleinen Fragmenten konzentrieren. Eine Reduktion von Fis1 im Modell führte zu weniger peripheren Spaltungen, gleichmäßigeren Schäden in den Mitochondrien und einem Zusammenbruch der Netzwerkgesundheit. Ein anderes Ankerprotein, MFF, begünstigt Mittelzonen‑Spaltungen, die ähnliche Tochterteile hervorbringen. Die Verringerung von MFF verursachte nur geringe Veränderungen im Schadensniveau, führte jedoch zu größeren, stärker verschmolzenen Mitochondrien — im Einklang mit Laborbefunden, dass dieser Weg eher die Zellteilung vorbereitet als Schäden zu beseitigen. Wurde das Kernfissionsprotein Drp1 reduziert, kam die Spaltung nahezu vollständig zum Erliegen. Der Schaden stieg dann nahe an das maximale mögliche Niveau, sodass das Netzwerk stark beeinträchtigt war.
Von müden Mitochondrien zu schwacher Insulinausschüttung
Da das Modell die mitochondriale Gesundheit mit der ATP‑Produktion verknüpft, kann es vorhersagen, wie sich diese strukturellen Veränderungen auf die Insulinausschüttung auswirken. Bei moderatem Verlust von Fis1 schüttete die Zelle weiterhin Insulin bei niedrigem Glukosespiegel aus, reagierte aber abgeschwächt auf hohen Glukosegehalt — ähnlich wie Beta‑Zellen von Menschen mit frühem metabolischem Leiden. Bei starkem Drp1‑Verlust wurde die Zelle nahezu unempfindlich gegenüber Glukose: Die Insulinausschüttung blieb selbst bei hohem Zucker nahe einem niedrigen basalen Niveau. Diese Muster entsprechen berichteten experimentellen Ergebnissen und deuten darauf hin, dass ein ausgewogenes Verhältnis der Fissionsproteine wichtig ist, um Beta‑Zellen sowohl energetisiert als auch reaktionsfähig zu halten.
Was das für das Verständnis von Diabetes bedeutet
Für Laien lautet die Botschaft der Studie, dass die Art und Weise, wie Mitochondrien auseinanderbrechen, ebenso wichtig ist wie ihre Energieproduktion. Ein fein abgestimmtes "gutes Auseinanderbrechen" schneidet beschädigte Stücke ab und hält das Netzwerk jung, was eine starke Insulinausschüttung unterstützt. Wird dieser Trimm‑Mechanismus geschwächt oder abgeschaltet, häufen sich beschädigte Mitochondrien, die ATP‑Produktion versagt und Beta‑Zellen verlieren ihre Fähigkeit, auf steigenden Blutzucker zu reagieren. Indem diese Verknüpfungen in einem flexiblen Computermodell abgebildet werden, bietet die Arbeit ein Prüfbett für künftige Ideen, wie die mitochondriale Qualität bei Diabetes geschützt oder wiederhergestellt werden kann — potenziell mit Blick auf neue Therapien, die Beta‑Zellen länger gesund erhalten.
Zitation: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Schlüsselwörter: Mitochondrien, Insulinausschüttung, Beta‑Zellen, Typ‑2‑Diabetes, Computermodeling