Clear Sky Science · it
Un modello di simulazione basato su regole illumina il ruolo della fissione mitocondriale asimmetrica nella salute delle cellule beta
Perché i piccoli motori contano per la glicemia
All’interno di ciascuna cellula produttrice di insulina del pancreas si trovano dozzine di mitocondri, i piccoli impianti energetici della cellula. Il loro compito è convertire lo zucchero nel segnale energetico che dice a queste cellule di rilasciare insulina e mantenere sotto controllo la glicemia. Nel diabete di tipo 2 questo sistema si guasta, e i mitocondri spesso appaiono danneggiati e frammentati al microscopio. Questo studio utilizza simulazioni al computer avanzate per porre una domanda semplice ma importante: in che modo il modo con cui i mitocondri si dividono e si rinnovano influenza la salute a lungo termine di queste cellule e la loro capacità di rilasciare insulina?
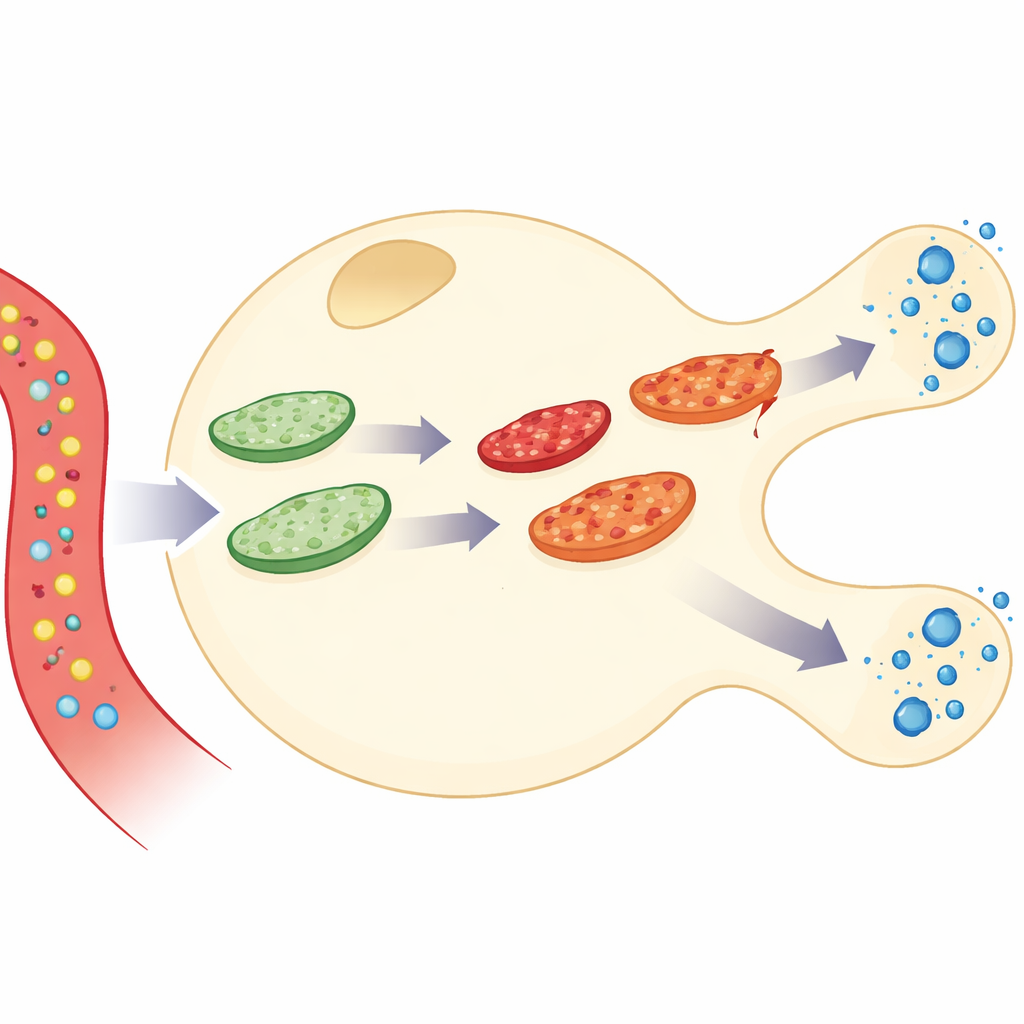
Collegare l’uso di energia al rilascio di insulina
Gli autori hanno costruito una simulazione dettagliata di una singola cellula beta pancreatica, il tipo cellulare che produce e secerne insulina. Il loro modello collega tre livelli di attività: come il glucosio viene ossidato per produrre la molecola energetica ATP, come il calcio intracellulare risponde, e come vengono rilasciati i granuli di insulina. Su questa base hanno aggiunto una “rete” mitocondriale dinamica che si fonde e si divide costantemente. Combinando queste parti, il modello può seguire cosa accade quando il glucosio entra nella cellula, l’ATP aumenta, il calcio pulsa e l’insulina viene secreta—mentre i mitocondri stessi invecchiano, accumulano danni, si riparano e vengono rimossi.
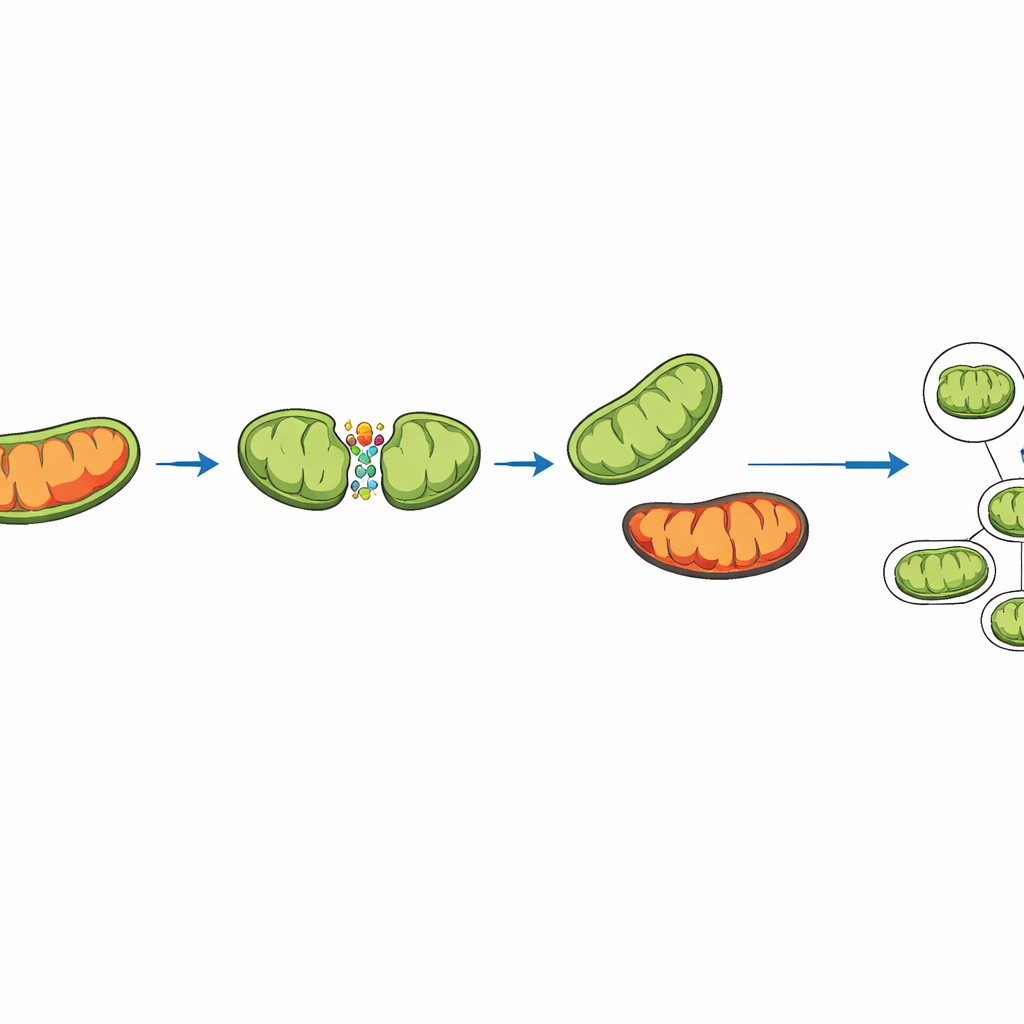
Due modi in cui i mitocondri si dividono—e perché uno fa la differenza
Esperimenti recenti mostrano che i mitocondri non si dividono tutti allo stesso modo. A volte si separano vicino al centro, generando due mitocondri figlie simili. Altre volte si staccano da una piccola estremità molto danneggiata, lasciando indietro un pezzo più grande e più sano. La simulazione cattura entrambi i tipi di fissione rappresentando le proteine chiave che ancorano la macchina di fissione in punti diversi sulla superficie mitocondriale. Nel modello viene monitorato un “punteggio di danno” per ciascun mitocondrio. Quando avviene una fissione periferica, il danno in eccesso viene deliberatamente convogliato nel piccolo frammento. Questo frammento ha maggiore probabilità di essere inghiottito e riciclato dalla cellula, un processo chiamato mitofagia, mentre il frammento più grande e pulito rimane nella rete.
Come l’ordinamento dei danni mantiene la rete giovane
Variando in modo sistematico quanto fortemente il danno venga convogliato nel frammento piccolo e quanto danneggiato un mitocondrio possa essere prima di essere rimosso, i ricercatori hanno esplorato migliaia di scenari virtuali. Quando la fissione non ordinava i danni, quasi tutti i mitocondri tendevano verso lo stesso livello, piuttosto malsano, di usura. Al contrario, anche un bias moderato che spingesse solo un po’ più di danno nel frammento piccolo riduceva notevolmente il danno medio nella rete. Ripetuti cicli di tale fissione asimmetrica e rimozione selettiva crearono un sistema auto-pulente, in cui i mitocondri sani restavano in grado di produrre ATP in modo efficiente.
Quando mancano proteine chiave della fissione
Il gruppo ha quindi simulato manipolazioni sperimentali comuni. Una proteina di ancoraggio, Fis1, promuove soprattutto gli eventi di fissione periferica che concentrano il danno nei piccoli frammenti. Ridurre Fis1 nel modello portò a meno fissioni periferiche, mitocondri più uniformemente danneggiati e al collasso della salute della rete. Un altro ancoraggio, MFF, favorisce le fissioni mediali che producono due figlie simili. Abbassare MFF causò solo cambiamenti lievi nei livelli di danno ma generò mitocondri più grandi e fusi, in accordo con osservazioni di laboratorio secondo cui questa via è più legata alla preparazione della divisione cellulare che alla rimozione dei danni. Quando la proteina centrale della fissione Drp1 fu ridotta, la divisione quasi si arrestò del tutto. Il danno salì allora vicino al massimo possibile, lasciando la rete gravemente compromessa.
Da mitocondri affaticati a scarso rilascio di insulina
Poiché il modello collega la salute mitocondriale alla produzione di ATP, può prevedere come questi cambiamenti strutturali influenzino la secrezione di insulina. Con una perdita moderata di Fis1, la cellula rilasciava ancora insulina a basso glucosio, ma la sua risposta all’alto glucosio era attenuata—simile alle cellule beta di persone con malattia metabolica in fase iniziale. Con una forte perdita di Drp1, la cellula divenne quasi non responsiva al glucosio: il rilascio di insulina rimaneva vicino a un basso livello basale anche quando lo zucchero era alto. Questi schemi assomigliano a risultati sperimentali riportati e suggeriscono che un’espressione bilanciata delle proteine di fissione è essenziale per mantenere le cellule beta sia energizzate sia reattive.
Che cosa significa per la comprensione del diabete
Per un pubblico non specialista, il messaggio dello studio è che il modo in cui i mitocondri si spezzano è altrettanto importante quanto il modo in cui producono energia. Una “buona rottura” ben calibrata elimina i pezzi danneggiati e mantiene la rete giovane, supportando un robusto rilascio di insulina. Quando questo meccanismo di sfoltimento è indebolito o spento, i mitocondri danneggiati si accumulano, la produzione di ATP vacilla e le cellule beta faticano a rispondere all’aumento della glicemia. Catturando questi legami in un modello al computer flessibile, il lavoro offre un banco di prova per idee future su come proteggere o ripristinare la qualità mitocondriale nel diabete, guidando potenzialmente nuovi trattamenti che aiutino le cellule beta a rimanere sane più a lungo.
Citazione: Henning, P., Schultz, J., Baltrusch, S. et al. A rule-based simulation model illuminates the role of asymmetric mitochondrial fission on beta-cell health. npj Syst Biol Appl 12, 64 (2026). https://doi.org/10.1038/s41540-026-00732-0
Parole chiave: mitocondri, secrezione di insulina, cellule beta, diabete di tipo 2, modellazione al computer