Clear Sky Science · sv
Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes
Varför denna forskning är viktig för framtida batterier
Litiumjonbatterier driver allt från bärbara datorer till elbilar, och tillverkare pressar dem för att lagra mer energi och laddas snabbare. För att nå dessa mål införs nya elektrolytrecept och högenergielektroder. En lovande elektrolytkomponent, kallad LiFSI, förbättrar stabilitet och prestanda, men den har en dold nackdel: den kan långsamt fräta på rostfria ståldelar inuti cellen. Denna artikel visar exakt hur den skadan uppstår och presenterar ett praktiskt sätt att stoppa den, vilket banar väg för säkrare och mer långlivade högenergibatterier.
Gömd skada inne i batterihöljet
Många kommersiella batteriformat, inklusive cylindriska och knappcellsformat, använder rostfritt stål för höljen och interna komponenter. Under normala förhållanden skyddar rostfritt stål sig självt med en tunn, stabil oxidskikt. Författarna visar att i LiFSI-baserade elektrolyter kan detta skydd svikta, särskilt vid de högre spänningar som används med moderna nickelrika katoder. Mycket små mängder klorid, ofta kvar från saltsframställning, och FSI-anjonen från LiFSI samverkar för att angripa stålet. Klorid startar processen genom att skapa mikroskopiska gropbildningar i ytan. När dessa gropar bildas löses järn från det rostfria stålet upp, och FSI-baserade arter hjälper till att hålla det järnet i lösning istället för att låta det återbilda ett skyddande oxidlager, så metallen fortsätter att lösas upp och groparna fördjupas.
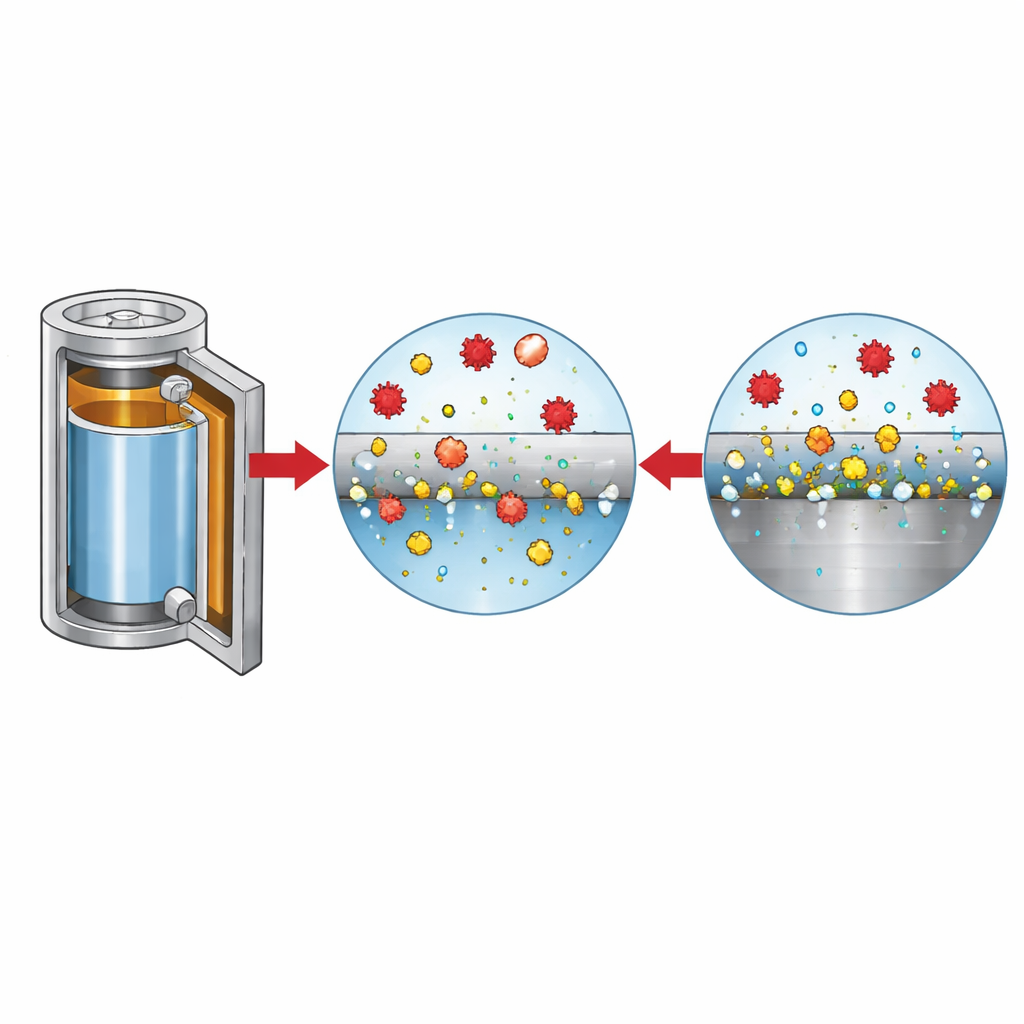
Hur aggressiva joner äter sig in i metallen
För att reda ut de olika jonernas roller varierade forskarna systematiskt kloridnivån och saltkompositionen, samtidigt som de övervakade ström, ytmorfologi och gasutveckling. Vid låga kloridnivåer passiverar stålytan igen efter en inledande störning, men när klorid överstiger någonstans runt tiotals delar per miljon läker inte groparna längre och upplösningen fortsätter. Avbildning och kemisk analys visar att i kloridrika lösningar blir ytan prickig av järnoxider och gropar, medan i rena LiFSI-elektrolyter är groparna färre men mycket djupare, där upplöst järn bildar lösliga komplex istället för att fälla ut. Dessa lösta metalljoner migrerar genom cellen och avsätts på den negativa elektroden, vilket ruggar upp litiumytan och bidrar till gasbildning som väte och koldioxid — båda oönskade för batterisäkerhet och livslängd.
En skyddande hjälpsalt som förändrar gränsytan
Teamet undersökte sedan om tillsats av ett andra salt, LiDFOB, kunde skydda stålet utan att offra LiFSI:s fördelar. Elektrokemiska tester visade att även måttliga mängder LiDFOB skjöt upp början av rostfritt ståls upplösning till högre spänningar och drastiskt minskade korrosionsströmmen. Mikroskopi bekräftade att gropar nästan försvann när LiDFOB fanns närvarande. Ytkänslig spektroskopi visade att i elektrolyter med enbart LiFSI kombineras oxiderat järn och krom med FSI-relaterade fragment, vilket stämmer med pågående upplösning. I kontrast lämnade LiDFOB-innehållande elektrolyter mer metalliskt järn och krom på ytan och introducerade bor- och fluor-rika föreningar kopplade till LiDFOB:s nedbrytning.
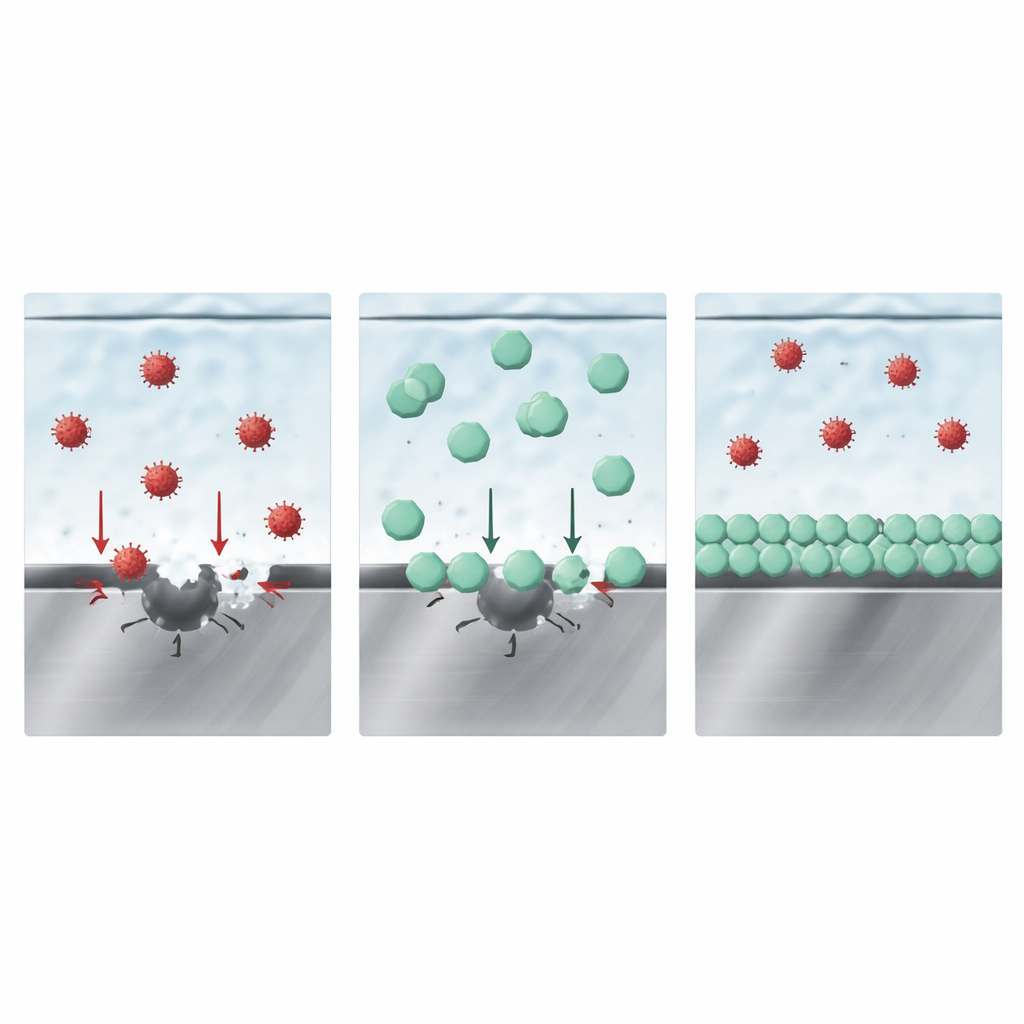
Hur det skyddande lagret vinner konkurrensen
Vid första anblick kan det verka som att en solid borhaltig film ensam skärmar av stålet. Ytterligare nedsänkningsförsök och modellering föreslog dock en mer subtil bild. Författarna föreslår att nyckeln är konkurrens mellan olika anjoner om utrymme direkt vid metallytan. Mätningar av ytladdningsbeteende, tillsammans med datorsimuleringar, visar att anjonen från LiDFOB binder starkare till järnoxidyta än vare sig klorid eller FSI. I praktiska termer tränger LiDFOB:s anjoner in i det innersta vätskeskiktet vid stålets gränsyta och ockuperar de platser där de aggressiva jonerna annars skulle initiera angrepp. Genom att blockera åtkomsten undertrycker de både den initiala kloriddrivna gropbildningen och den FSI-drivna djupa upplösning som följer, vilket i sin tur minskar gasutveckling och metallavsättning på andra ställen i cellen.
Från mekanism till bättre presterande batterier
För att testa om detta kemiska skydd överförs till verkliga fördelar cyklade forskarna grafit||NMC811- och kisel-grafit||NMC811-celler med olika elektrolyter och rostfria stålsorter. Celler med enbart LiFSI gav tidig haveri på grund av metallupplösning, medan de som använde en blandning LiFSI–LiDFOB visade kraftigt förlängd livslängd. När mer korrosionsbeständigt rostfritt stål (SUS316L) kombinerades med den optimerade tvåsalts-elektrolyten nådde kisel-grafitceller runt 300 cykler till 80 procent kvarvarande kapacitet. Pouchceller utan rostfritt ståls hårdvara men med samma elektrolyt varade också ungefär dubbelt så länge som med en konventionell LiPF6-baserad formulering, vilket belyser LiDFOB:s bredare stabiliserande effekt på batterigränsytor.
Vad detta betyder för vardagsteknik
Enkelt uttryckt visar studien att ett lovande högpresterande salt, LiFSI, tyst kan korrodera de ståldelar som håller ett batteri ihop — särskilt när spår av klorid finns närvarande. Författarna visar att klorid öppnar små hål i det skyddande skiktet, och att LiFSI sedan förhindrar att dessa hål läker genom att hålla upplöst järn i vätskan, så skadan sprider sig. Genom att tillsätta LiDFOB, vars joner föredrar att rada upp sig på stålytan och hålla de skadliga jonerna på avstånd, stoppas korrosionen till stor del, gasbildningen minskar och både knappcells- och pouchceller får avsevärt längre livslängd. Denna kombination av ett kraftfullt men frätande salt med ett genomtänkt "bodyguard"-salt erbjuder ett praktiskt recept för säkrare, längre livade högenergilitiumjonbatterier som kan komma att användas i framtida elfordon och storskaliga celler.
Citering: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Nyckelord: litiumjonbatterier, elektrolytprodukter, korrosion av rostfritt stål, LiFSI, LiDFOB