Clear Sky Science · nl
Mechanisme en mitigatie van roestvrijstalen oplossing in LiFSI-gebaseerde elektrolyten voor lithium-ionbatterijen
Waarom dit onderzoek belangrijk is voor toekomstige batterijen
Lithium-ionbatterijen voeden alles, van laptops tot elektrische auto’s, en fabrikanten streven ernaar ze meer energie te laten opslaan en sneller te laten opladen. Om die doelen te bereiken worden nieuwe elektrolytformules en hoogenergetische elektroden toegepast. Een veelbelovend elektrolytzout, LiFSI, verbetert stabiliteit en prestaties, maar heeft een verborgen nadeel: het kan langzaam roestvrijstalen onderdelen in de cel aantasten. Dit artikel legt precies bloot hoe die schade ontstaat en presenteert een praktische manier om dat proces te stoppen, wat de weg vrijmaakt voor veiligere en langer meegaande hoogenergetische batterijen.
Verborgen schade binnen de batterijkast
Veel commerciële batterijformaten, waaronder cilindrische en knoopcellen, gebruiken roestvrij staal voor behuizing en interne componenten. Onder normale omstandigheden beschermt roestvrij staal zichzelf met een dun, stabiel oxidefilm. De auteurs tonen aan dat in LiFSI-gebaseerde elektrolyten deze bescherming kan falen, vooral bij de hogere spanningen die gebruikt worden met moderne nikkelrijke kathodes. Sporen chloride, vaak achtergebleven bij zouthandelingsprocessen, en het FSI-anion uit LiFSI werken samen om het staal aan te vallen. Chloride begint het proces door microscopische putjes in het oppervlak te creëren. Zodra die putjes gevormd zijn, lost ijzer van het roestvrij staal op, en FSI-gerelateerde soortgenoten helpen dat ijzer in oplossing te houden in plaats van dat het een beschermend oxide hervormt, waardoor het metaal blijft oplossen en de putjes dieper groeien.
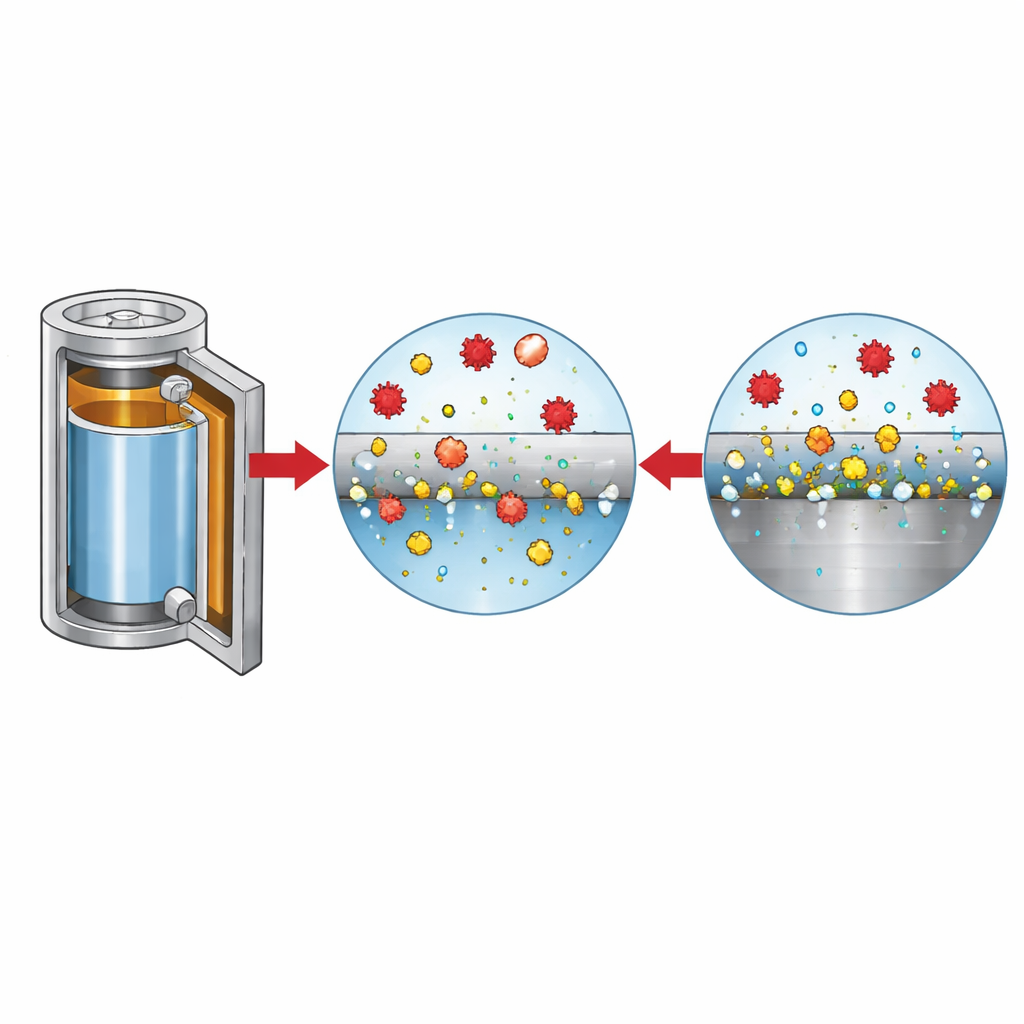
Hoe agressieve ionen het metaal wegvreten
Om de rollen van de verschillende ionen te ontrafelen varieerden de onderzoekers systematisch het chloridegehalte en de zoutsamenstelling, terwijl ze stroom, oppervlaktemorfologie en gasontwikkeling volgden. Bij lage chlorideconcentraties passeert het staaloppervlak na een aanvankelijke verstoring weer naar passivering, maar zodra chloride ongeveer enkele tientallen delen per miljoen overschrijdt, herstellen de putjes niet langer en gaat oplossing door. Beeldvorming en chemische analyse laten zien dat in chloride-rijke oplossingen het oppervlak bezaaid raakt met ijzeroxiden en putjes, terwijl in zuivere LiFSI-elektrolyten de putjes minder talrijk maar veel dieper zijn, waarbij opgelost ijzer oplosbare complexen vormt in plaats van uit te slaan. Deze opgeloste metaalionen migreren door de cel en slaan neer op de negatieve elektrode, ruw maken van het lithiumoppervlak en bijdragen aan gasvorming zoals waterstof en kooldioxide — beide onwenselijk voor batterijveiligheid en levensduur.
Een beschermend hulpszout dat de interface hervormt
Het team onderzocht vervolgens of het toevoegen van een tweede zout, LiDFOB, het staal kon beschermen zonder de voordelen van LiFSI op te geven. Elektrochemische tests toonden aan dat zelfs bescheiden hoeveelheden LiDFOB het begin van roestvrijstalen oplossing naar hogere spanningen verschoven en de corrosiestroom drastisch verminderden. Microscopy bevestigde dat putjes vrijwel verdwenen wanneer LiDFOB aanwezig was. Oppervlaktegevoelige spectroscopie toonde dat in uitsluitend LiFSI-elektrolyten geoxideerde ijzer- en chroomsoorten combineren met FSI-gerelateerde fragmenten, wat overeenkomt met aanhoudende oplossing. Ter vergelijking lieten elektrolyten met LiDFOB meer metallisch ijzer en chroom aan het oppervlak achter en introduceerden ze boron- en fluor-rijke verbindingen die gekoppeld zijn aan de afbraak van LiDFOB.
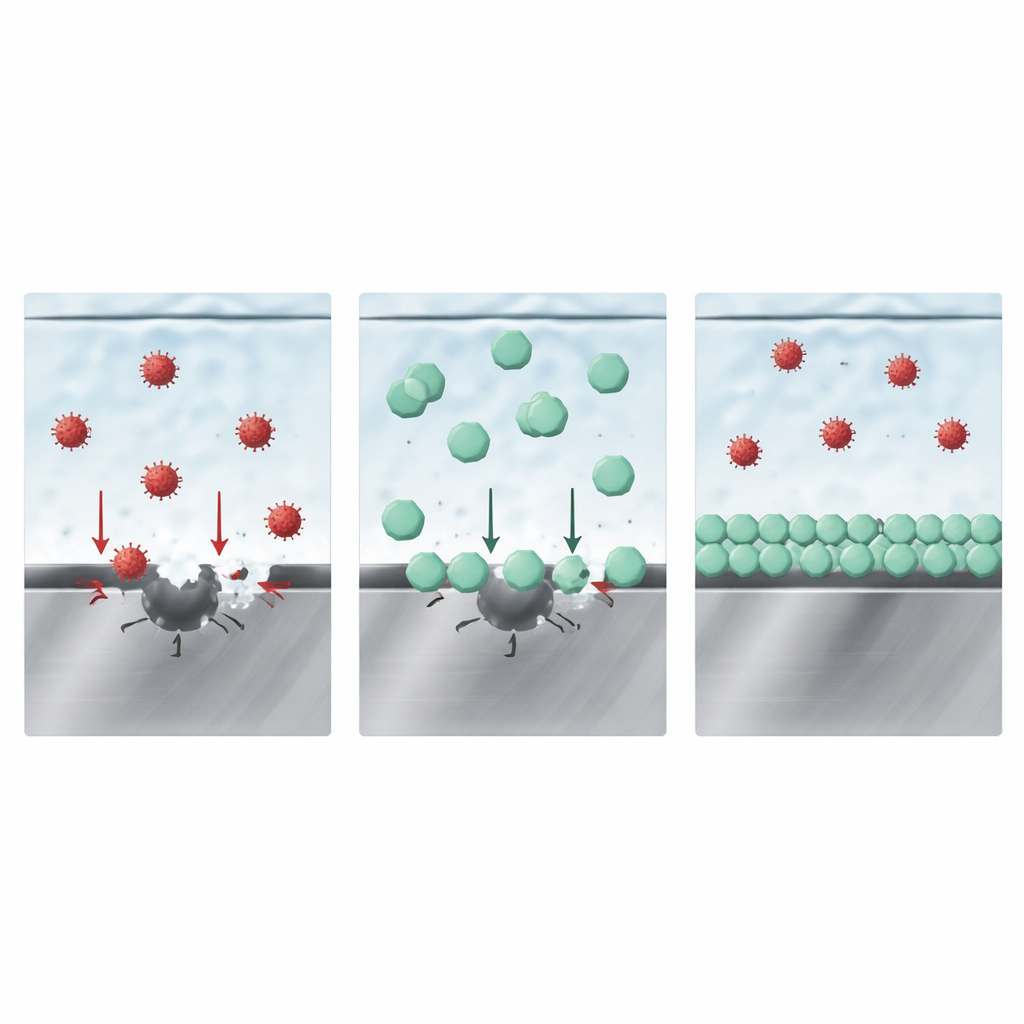
Hoe de beschermende laag de concurrentie wint
Op het eerste gezicht lijkt het misschien dat een solide boorhoudende film het staal uitsluitend afschermt. Extra dompelproeven en modellering suggereerden echter een subtieler beeld. De auteurs stellen dat de sleutel de competitie is tussen verschillende anionen om ruimte direct aan het metaaloppervlak. Metingen van het oppervlakte-laadgedrag, samen met computersimulaties, tonen aan dat het anion van LiDFOB sterker bindt aan het ijzeroxide-oppervlak dan zowel chloride als FSI. In praktische termen dringen de anionen van LiDFOB door tot de binnenste laag van de vloeistof aan de staalinterface en bezetten juist die plekken waar de agressieve ionen anders de aanval zouden inzetten. Door de toegang te blokkeren onderdrukken ze zowel de initiële chloride-gedreven pitting als de door FSI gedreven diepe oplossing die daarop volgt, wat op zijn beurt gasontwikkeling en metaalneerslag elders in de cel vermindert.
Van mechanisme naar beter presterende batterijen
Om te testen of deze chemische bescherming zich vertaalt naar praktische voordelen, cyclisten de onderzoekers graphite||NMC811 en sillicium-grafiet||NMC811 cellen met verschillende elektrolyten en roestvrijstalen kwaliteiten. Cellen met alleen LiFSI faalden vroeg door metaaloplossing, terwijl cellen met gemengde LiFSI–LiDFOB-elektrolyten een sterk verlengde levensduur lieten zien. Wanneer corrosiebestendiger roestvrij staal (SUS316L) werd gecombineerd met het geoptimaliseerde dubbelzout-elektrolyt, bereikten sillicium-grafietcellen ongeveer 300 cycli tot 80% resterende capaciteit. Pouchcellen zonder roestvrijstalen hardware maar met hetzelfde elektrolyt hielden ook ruwweg twee keer zo lang vol als met een conventionele LiPF6-gebaseerde formulering, wat het bredere stabiliserende effect van LiDFOB op batterijinterfaces benadrukt.
Wat dit betekent voor alledaagse technologie
Eenvoudig gezegd laat de studie zien dat een veelbelovend hoogpresterend zout, LiFSI, stilletjes de stalen onderdelen kan corroderen die een batterij bij elkaar houden — vooral als sporadisch chloride aanwezig is. De auteurs onthullen dat chloride kleine gaten in de beschermende film opent, en dat LiFSI die gaten vervolgens verhindert te helen door opgelost ijzer in de vloeistof te houden, waardoor de schade zich uitbreidt. Door LiDFOB toe te voegen, waarvan de ionen zich bij voorkeur op het staaloppervlak schikken en de schadelijke ionen op afstand houden, wordt de corrosie grotendeels gestopt, neemt gasvorming af en gaan zowel knoop- als pouchcellen veel langer mee. Deze combinatie van een krachtig maar corrosief zout met een doordacht gekozen "bodyguard"-zout biedt een praktische formule voor veiligere, langer houdende hoogenergetische lithium-ionbatterijen die hun weg kunnen vinden naar toekomstige elektrische voertuigen en grote cellen.
Bronvermelding: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Trefwoorden: lithium-ion batterijen, elektrolytadditieven, corrosie van roestvrij staal, LiFSI, LiDFOB