Clear Sky Science · it
Meccanismo e mitigazione della dissoluzione dell'acciaio inossidabile negli elettroliti per batterie agli ioni di litio a base di LiFSI
Perché questa ricerca conta per le batterie del futuro
Le batterie agli ioni di litio alimentano tutto, dai portatili alle auto elettriche, e i produttori cercano continuamente di aumentare la capacità e accelerare la ricarica. Per raggiungere questi obiettivi si adottano nuove formulazioni di elettrolita e elettrodi ad alta energia. Un ingrediente elettrolitico promettente, chiamato LiFSI, migliora stabilità e prestazioni, ma presenta un problema nascosto: può corrodere lentamente i componenti in acciaio inossidabile all’interno della cella. Questo articolo svela esattamente come avviene il danno e propone un metodo pratico per prevenirlo, aprendo la strada a celle ad alta energia più sicure e durature.
Danno nascosto all’interno del guscio della batteria
Molti formati commerciali di batterie, incluse celle cilindriche e a bottone, usano acciaio inossidabile per gli involucri e i componenti interni. In condizioni normali l’acciaio si protegge con un sottile film di ossido stabile. Gli autori dimostrano che negli elettroliti a base LiFSI questa protezione può venire meno, soprattutto alle tensioni più alte usate con catodi ricchi di nichel moderni. Piccole quantità di cloruro, spesso residue dalla produzione dei sali, e l’anione FSI proveniente da LiFSI agiscono insieme per attaccare l’acciaio. Il cloruro avvia il processo creando micropitting sulla superficie. Una volta che questi pit si formano, il ferro dell’acciaio si dissolve, e le specie derivanti da FSI mantengono il ferro in soluzione invece che permetterne la ricostituzione come ossido protettivo, così il metallo continua a dissolversi e i pit si approfondiscono.
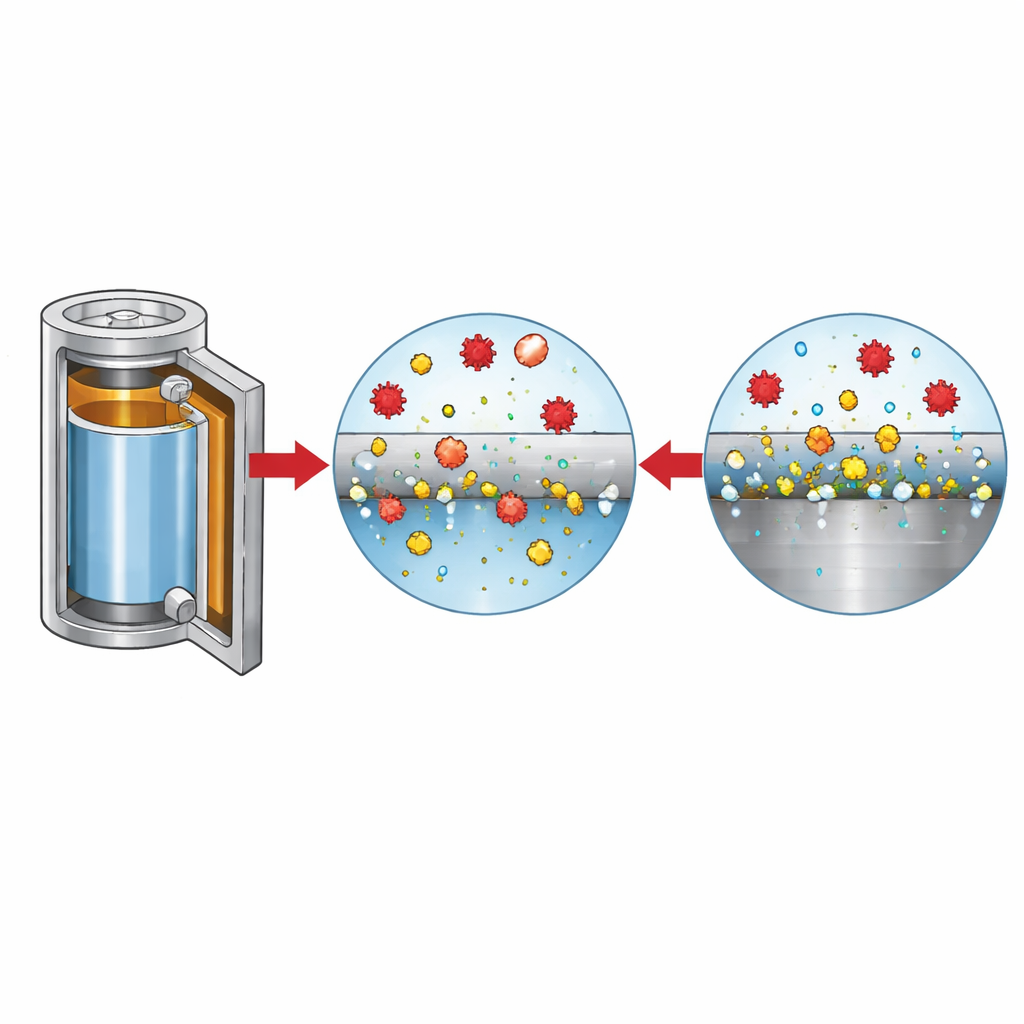
Come gli ioni aggressivi consumano il metallo
Per chiarire i ruoli dei diversi ioni, i ricercatori hanno variato sistematicamente il contenuto di cloruro e la composizione del sale, monitorando corrente, morfologia superficiale ed evoluzione gassosa. A bassi livelli di cloruro, la superficie dell’acciaio si ripassa dopo un disturbo iniziale, ma quando il cloruro supera poche decine di parti per milione i pit non si rimarginano più e la dissoluzione prosegue. Imaging e analisi chimiche rivelano che in soluzioni ricche di cloruro la superficie si riempie di ossidi di ferro e di pit, mentre negli elettroliti puri a base LiFSI i pit sono meno numerosi ma molto più profondi, con il ferro disciolto che forma complessi solubili invece di precipitare. Questi ioni metallici disciolti migrano attraverso la cella e si depositano sull’elettrodo negativo, irruvidendo la superficie del litio e contribuendo alla formazione di gas come idrogeno e anidride carbonica — entrambi indesiderabili per la sicurezza e la durata della batteria.
Un sale protettivo che rimodella l’interfaccia
Il team ha quindi esplorato se l’aggiunta di un secondo sale, LiDFOB, potesse proteggere l’acciaio senza compromettere i vantaggi di LiFSI. I test elettrochimici hanno mostrato che anche quantità modeste di LiDFOB spostano l’inizio della dissoluzione dell’acciaio verso tensioni più alte e riducono drasticamente la corrente di corrosione. La microscopia ha confermato che i pit quasi scompaiono in presenza di LiDFOB. Spettroscopie sensibili alla superficie hanno rivelato che, negli elettroliti solo LiFSI, specie ossidate di ferro e cromo si combinano con frammenti legati a FSI, coerente con una dissoluzione in corso. Al contrario, negli elettroliti contenenti LiDFOB la superficie mantiene più ferro e cromo metallici e compaiono composti ricchi di boro e fluoro associati alla degradazione di LiDFOB.
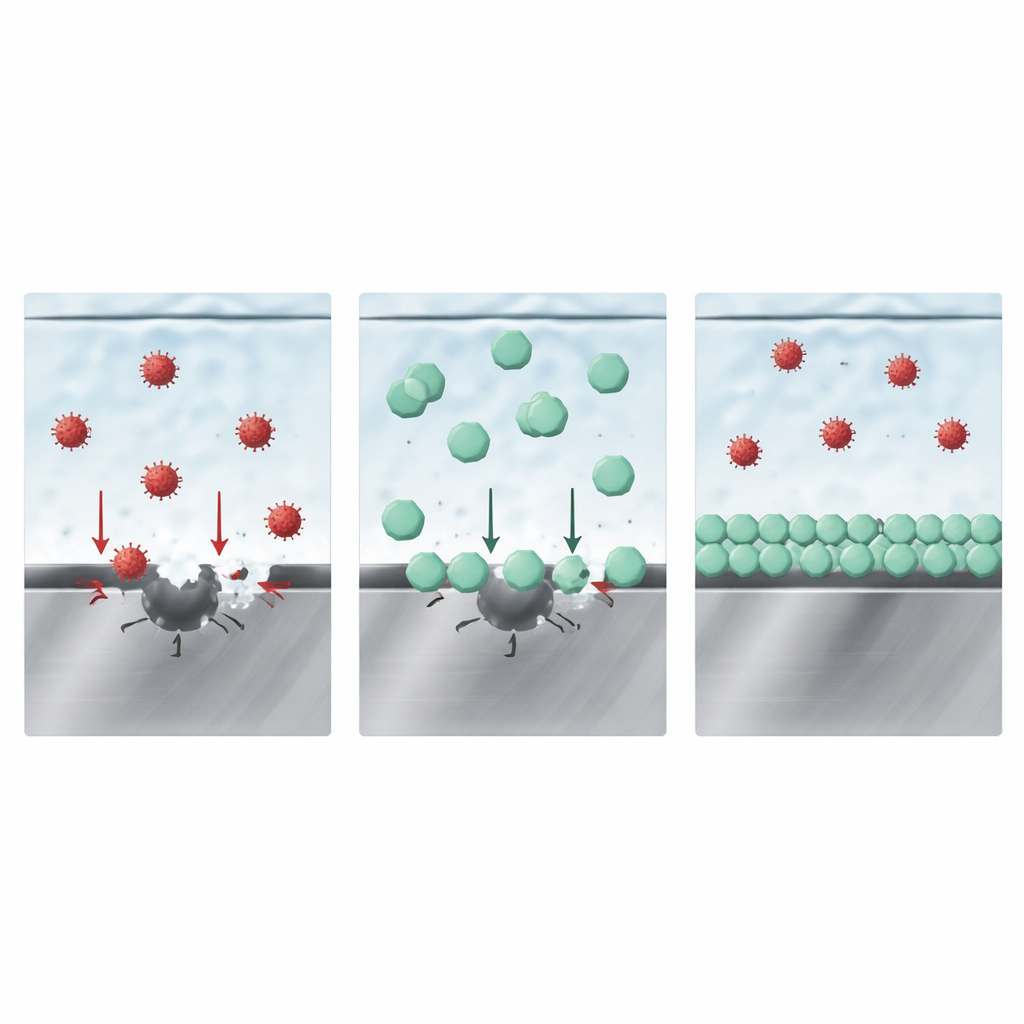
Come lo strato protettivo prevale nella competizione
A prima vista potrebbe sembrare che un film solido contenente boro sia l’unica barriera che protegge l’acciaio. Tuttavia esperimenti di immersione aggiuntivi e modellizzazione suggeriscono un quadro più sottile. Gli autori propongono che la chiave sia la competizione tra diversi anioni per lo spazio immediatamente sulla superficie metallica. Misure del comportamento della carica superficiale, insieme a simulazioni al computer, mostrano che l’anione derivato da LiDFOB si lega più fortemente alla superficie di ossido di ferro rispetto al cloruro o all’FSI. In termini pratici, gli anioni di LiDFOB si accumulano nello strato più interno del liquido sull’interfaccia con l’acciaio, occupando i punti dove gli ioni aggressivi altrimenti inizierebbero l’attacco. Bloccando l’accesso, sopprimono sia il pitting iniziale guidato dal cloruro sia la dissoluzione profonda indotta da FSI che segue, riducendo di conseguenza l’evoluzione gassosa e il deposito di metallo in altre parti della cella.
Dal meccanismo a batterie con prestazioni migliori
Per verificare se questa protezione chimica si traduce in benefici reali, i ricercatori hanno testato cicli su celle grafite||NMC811 e silicio‑grafite||NMC811 usando elettroliti e gradi di acciaio inossidabile diversi. Le celle con solo LiFSI sono fallite precocemente a causa della dissoluzione del metallo, mentre quelle con elettroliti misti LiFSI–LiDFOB hanno mostrato durate molto più estese. Quando un acciaio inossidabile più resistente alla corrosione (SUS316L) è stato combinato con l’elettrolita dual‑salt ottimizzato, le celle silicio‑grafite hanno raggiunto circa 300 cicli fino all’80% di capacità residua. Anche le pouch cell senza componenti in acciaio inossidabile ma con lo stesso elettrolita sono durate circa il doppio rispetto a una formulazione convenzionale a base di LiPF6, evidenziando l’effetto stabilizzante più ampio di LiDFOB sulle interfacce della batteria.
Cosa significa per la tecnologia di tutti i giorni
In termini accessibili, lo studio mostra che un sale ad alte prestazioni, LiFSI, può corrodere silenziosamente le parti in acciaio che tengono insieme una batteria — specialmente quando è presente cloruro in tracce. Gli autori rivelano che il cloruro apre piccoli fori nel film protettivo, e LiFSI impedisce a quei fori di rimarginarsi mantenendo il ferro disciolto in fase liquida, così il danno si propaga. Aggiungendo LiDFOB, i cui ioni si dispongono preferenzialmente sulla superficie dell’acciaio e tengono lontani gli ioni nocivi, la corrosione viene in gran parte arrestata, la generazione di gas diminuisce e sia le celle a bottone sia le pouch durano molto più a lungo. Questa combinazione di un sale potente ma corrosivo con un “corpo di guardia” scelto con criterio offre una ricetta pratica per batterie agli ioni di litio ad alta energia più sicure e con vita utile maggiore, pronte per l’uso in futuri veicoli elettrici e in celle di grande formato.
Citazione: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Parole chiave: batterie agli ioni di litio, additivi per elettroliti, corrosione dell'acciaio inossidabile, LiFSI, LiDFOB