Clear Sky Science · de
Mechanismus und Minderung der Auflösung von Edelstahl in LiFSI-basierten Elektrolyten für Lithium-Ionen-Batterien
Warum diese Forschung für zukünftige Batterien wichtig ist
Lithium-Ionen-Batterien treiben alles an, von Laptops bis hin zu Elektroautos. Hersteller versuchen, ihre Energiespeicherkapazität zu erhöhen und die Ladezeiten zu verkürzen. Um diese Ziele zu erreichen, werden neue Elektrolyt‑Formulierungen und hochenergetische Elektroden eingesetzt. Ein vielversprechender Elektrolytbestandteil, LiFSI, verbessert Stabilität und Leistung, hat jedoch einen versteckten Nachteil: Er kann Edelstahlteile im Inneren der Zelle langsam angreifen. Diese Studie zeigt genau, wie dieser Schaden entsteht, und präsentiert eine praktikable Methode, ihn zu verhindern — ein Schritt hin zu sichereren und langlebigeren Hochenergiebatterien.
Versteckte Schäden im Batteriegehäuse
Viele kommerzielle Batterieformate, etwa zylindrische Zellen und Knopfzellen, verwenden Edelstahl für Gehäuse und interne Komponenten. Unter normalen Bedingungen schützt sich Edelstahl durch eine dünne, stabile Oxidschicht. Die Autoren zeigen, dass dieser Schutz in LiFSI‑basierten Elektrolyten versagen kann, besonders bei den höheren Spannungen, die bei modernen Nickel‑reichen Kathoden verwendet werden. Winzige Chloridmengen, die oft als Verunreinigung aus der Salzproduktion zurückbleiben, und das FSI‑Anion aus LiFSI wirken zusammen und greifen den Stahl an. Chlorid initiiert den Prozess, indem es mikroskopische Grübchen (Pitting) in der Oberfläche erzeugt. Sobald diese Grübchen entstehen, löst sich Eisen aus dem Edelstahl, und FSI‑basierte Spezies halten das Eisen in Lösung, statt dass es wieder eine schützende Oxidschicht bildet — dadurch löst sich weiter Metall und die Grübchen vertiefen sich.
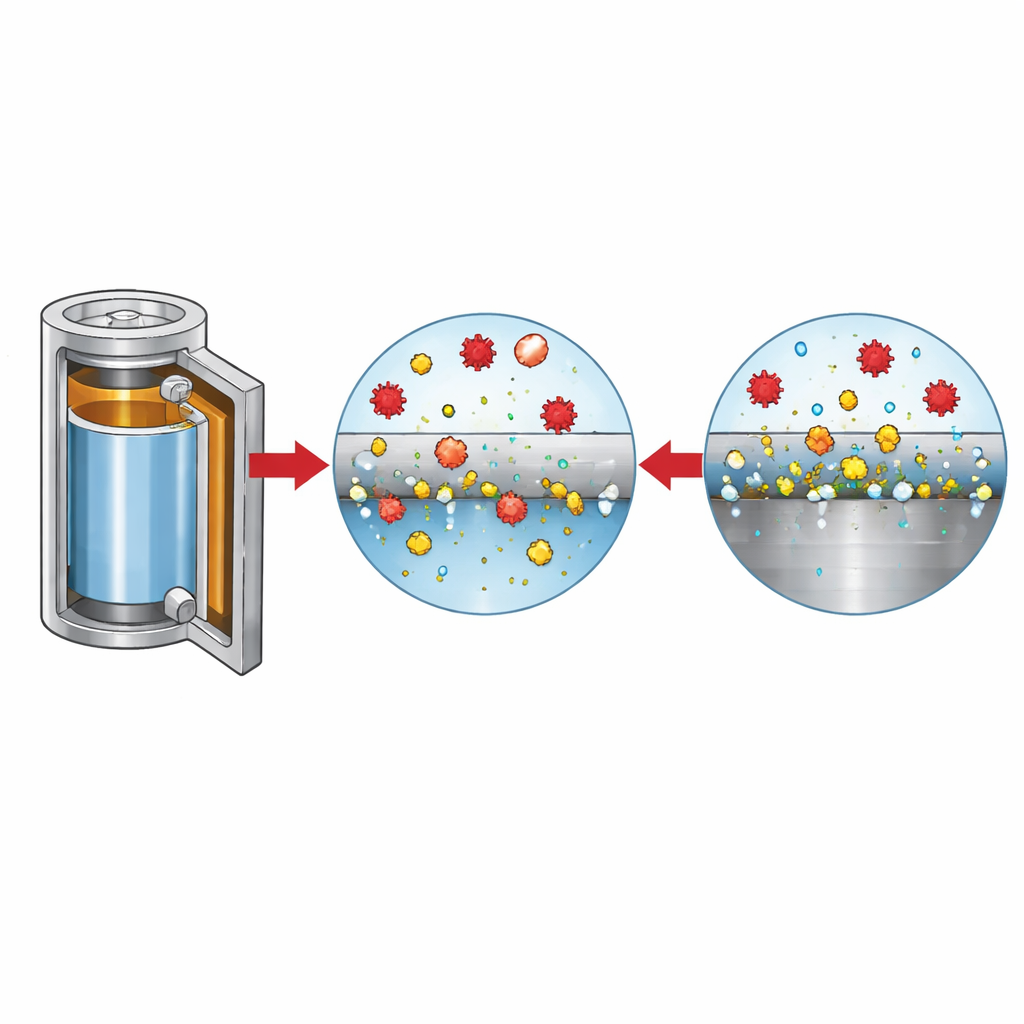
Wie aggressive Ionen das Metall angreifen
Um die Rollen der unterschiedlichen Ionen zu entwirren, variierten die Forschenden systematisch den Chloridgehalt und die Salzkomposition und überwachten dabei Strom, Oberflächenmorphologie und Gasentwicklung. Bei geringen Chloridkonzentrationen passiviert die Stahloberfläche nach einer anfänglichen Störung wieder, aber sobald Chlorid einige Dutzend Teile pro Million überschreitet, heilen die Grübchen nicht mehr und die Auflösung setzt sich fort. Bildgebende Verfahren und chemische Analysen zeigen, dass die Oberfläche in chloridreichen Lösungen mit Eisenoxiden und Grübchen übersät ist, während in reinen LiFSI‑Elektrolyten die Grübchen seltener, dafür aber deutlich tiefer sind; das gelöste Eisen bildet lösliche Komplexe statt zu fällen. Diese gelösten Metallionen wandern durch die Zelle und lagern sich an der negativen Elektrode ab, machen die Lithiumoberfläche rauer und tragen zur Gasbildung wie Wasserstoff und Kohlendioxid bei — beides unerwünscht für Sicherheit und Lebensdauer der Batterie.
Ein schützendes Hilfssalz, das die Grenzfläche umgestaltet
Das Team untersuchte anschließend, ob die Zugabe eines zweiten Salzes, LiDFOB, den Stahl schützen kann, ohne die Vorteile von LiFSI zu verlieren. Elektrochemische Tests zeigten, dass bereits moderate Mengen LiDFOB den Beginn der Edelstahlauslösung auf höhere Spannungen verschieben und den Korrosionsstrom drastisch reduzieren. Mikroskopische Untersuchungen bestätigten, dass Grübchen bei Anwesenheit von LiDFOB nahezu verschwanden. Oberflächenempfindliche Spektroskopie zeigte, dass in reinen LiFSI‑Elektrolyten oxidiertes Eisen- und Chrom‑Spezies zusammen mit FSI‑verwandten Fragmenten auftreten, was zur fortlaufenden Auflösung passt. Im Gegensatz dazu hinterließen LiDFOB‑haltige Elektrolyte mehr metallisches Eisen und Chrom an der Oberfläche und führten zu bor‑ und fluorreichen Verbindungen, die mit dem Abbau von LiDFOB in Verbindung stehen.
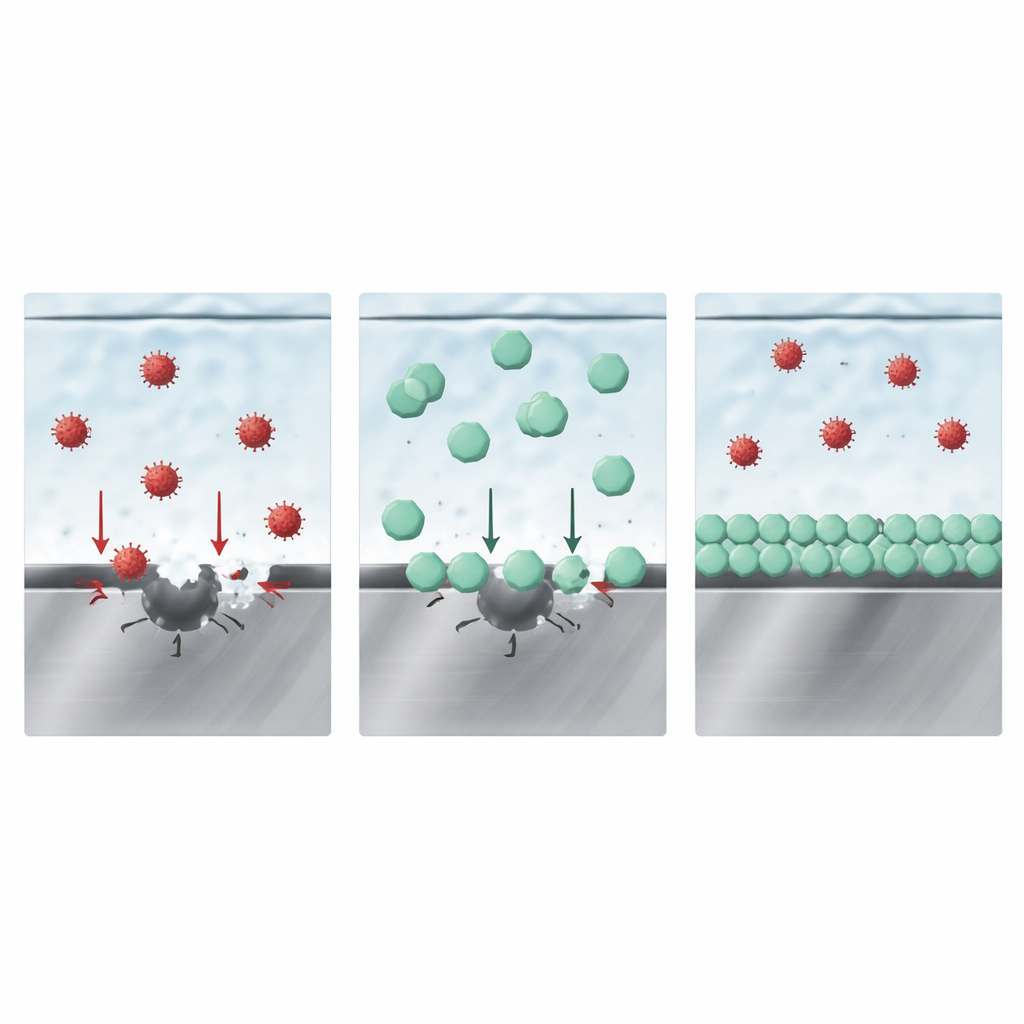
Wie die schützende Schicht den Wettstreit gewinnt
Auf den ersten Blick könnte man annehmen, dass allein ein festes borhaltiges Filmchen den Stahl abschirmt. Zusätzliche Eintauchexperimente und Modellierungen legen jedoch ein subtileres Bild nahe. Die Autoren schlagen vor, dass der Schlüssel im Wettbewerb verschiedener Anionen um die Plätze unmittelbar an der Metalloberfläche liegt. Messungen des Oberflächenladungsverhaltens zusammen mit Computersimulationen zeigen, dass das Anion von LiDFOB stärker an der Eisenoxidschicht bindet als Chlorid oder FSI. Praktisch bedeutet das: Die Anionen von LiDFOB drängen sich in die innerste Schicht der Flüssigkeit an der Stahlgrenzfläche und besetzen genau jene Orte, an denen sonst die aggressiven Ionen den Angriff einleiten würden. Indem sie den Zugang blockieren, unterdrücken sie sowohl das initiale chloridgetriebene Pitting als auch die darauf folgende, von FSI angetriebene tiefe Auflösung — was wiederum die Gasentwicklung und Metallabscheidung an anderen Stellen der Zelle reduziert.
Vom Mechanismus zu besser funktionierenden Batterien
Um zu prüfen, ob dieser chemische Schutz in der Praxis Nutzen bringt, haben die Forschenden Graphit||NMC811‑ und Silizium‑Graphit||NMC811‑Zellen mit unterschiedlichen Elektrolyten und Edelstahlsorten zyklisiert. Zellen mit nur LiFSI versagten früh aufgrund der Metallauflösung, während Zellen mit gemischten LiFSI–LiDFOB‑Elektrolyten deutlich längere Lebensdauern zeigten. In Kombination mit einem korrosionsbeständigeren Edelstahl (SUS316L) und dem optimierten Dual‑Salz‑Elektrolyten erreichten Silizium‑Graphit‑Zellen etwa 300 Zyklen bis 80 % verbleibender Kapazität. Pouch‑Zellen ohne Edelstahl‑Hardware, aber mit demselben Elektrolyten, hielten ebenfalls etwa doppelt so lange wie mit einer konventionellen LiPF6‑Formulierung, was die allgemein stabilisierende Wirkung von LiDFOB an Batteriegrenzflächen unterstreicht.
Was das für alltägliche Technologie bedeutet
Eindringlich gezeigt: Das vielversprechende Hochleistungs‑Salz LiFSI kann unbemerkt die Stahlteile angreifen, die eine Batterie zusammenhalten — besonders wenn Spuren von Chlorid vorhanden sind. Die Autoren legen offen, dass Chlorid winzige Löcher in der schützenden Oxidschicht öffnet, und LiFSI verhindert dann die Heilung dieser Löcher, indem es gelöstes Eisen in der Elektrolytphase hält, sodass sich der Schaden ausbreitet. Durch die Zugabe von LiDFOB, dessen Ionen sich bevorzugt an der Stahloberfläche anlagern und die schädlichen Ionen fernhalten, wird die Korrosion weitgehend gestoppt, die Gasentwicklung verringert und sowohl Knopf- als auch Pouch‑Zellen erreichen deutlich längere Lebensdauern. Die Kombination aus einem leistungsfähigen, aber korrosiven Salz und einem intelligent gewählten „Bodyguard“-Salz bietet somit eine praktische Rezeptur für sicherere, langlebigere Hochenergie‑Lithium‑Ionen‑Batterien, die in künftigen Elektrofahrzeugen und großformatigen Zellen Anwendung finden könnten.
Zitation: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Schlüsselwörter: Lithium-Ionen-Batterien, Elektrolyt‑Additive, Edelstahlkorrosion, LiFSI, LiDFOB