Clear Sky Science · pt
Mecanismo e mitigação da dissolução do aço inoxidável em eletrólitos de baterias de íon-lítio à base de LiFSI
Por que esta pesquisa importa para as baterias do futuro
Baterias de íon-lítio alimentam tudo, desde laptops até carros elétricos, e os fabricantes buscam aumentar sua capacidade de armazenar energia e acelerar o carregamento. Para atingir esses objetivos, estão sendo adotadas novas fórmulas de eletrólitos e eletrodos de alta energia. Um ingrediente promissor no eletrólito, chamado LiFSI, melhora a estabilidade e o desempenho, mas traz uma desvantagem oculta: pode corroer lentamente peças de aço inoxidável dentro da célula. Este artigo revela exatamente como esse dano ocorre e apresenta uma forma prática de interrompê-lo, abrindo caminho para baterias de alta energia mais seguras e duráveis.
Dano oculto dentro da carcaça da bateria
Muitos formatos comerciais de bateria, incluindo cilíndricos e tipo moeda, usam aço inoxidável em invólucros e componentes internos. Em condições normais, o aço inoxidável se protege com uma fina película de óxido estável. Os autores mostram que, em eletrólitos à base de LiFSI, essa proteção pode falhar, especialmente nas tensões mais altas usadas com cátodos ricos em níquel. Quantidades minúsculas de cloreto, frequentemente residuais do processo de produção de sais, e o ânion FSI do LiFSI agem em conjunto para atacar o aço. O cloreto inicia o processo criando micro-pites na superfície. Uma vez formados esses pontos, o ferro do aço inoxidável se dissolve, e espécies derivadas do FSI ajudam a manter esse ferro em solução em vez de permitir que ele reconstituía um óxido protetor, de modo que o metal continua a dissolver-se e as pites ficam mais profundas.
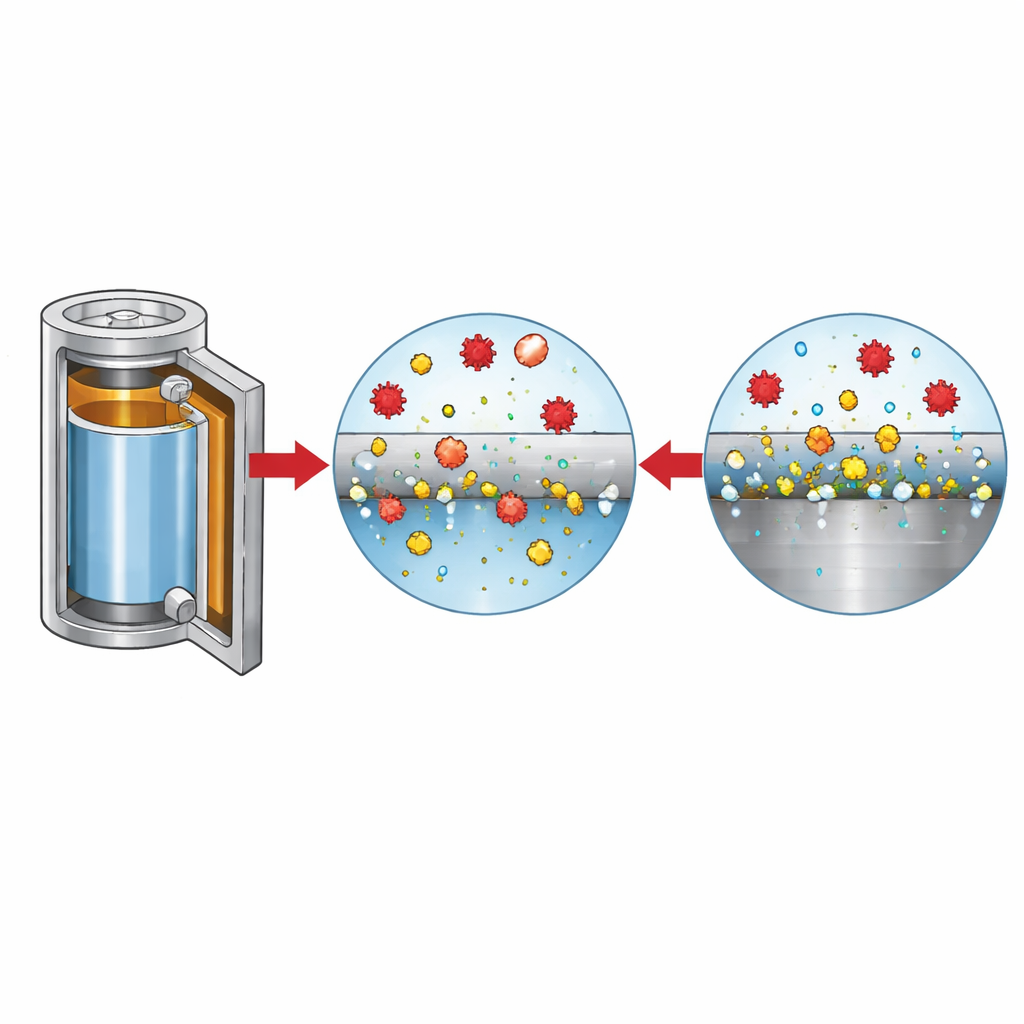
Como íons agressivos corroem o metal
Para separar os papéis dos diferentes íons, os pesquisadores variaram sistematicamente o nível de cloreto e a composição do sal, enquanto monitoravam corrente, morfologia de superfície e evolução de gases. Em níveis baixos de cloreto, a superfície do aço volta a passivar-se após uma perturbação inicial, mas quando o cloreto excede algumas dezenas de partes por milhão, as pites não se cicatrizam e a dissolução continua. Imagens e análises químicas revelam que, em soluções ricas em cloreto, a superfície fica pontilhada de óxidos de ferro e pites, enquanto em eletrólitos de LiFSI puro as pites são menos numerosas, porém muito mais profundas, com ferro dissolvido formando complexos solúveis em vez de precipitar. Esses íons metálicos dissolvidos migram através da célula e se depositam no eletrodo negativo, tornando a superfície do lítio áspera e contribuindo para a formação de gases como hidrogênio e dióxido de carbono — ambos indesejáveis para a segurança e vida útil da bateria.
Um sal auxiliar protetor que remodela a interface
A equipe então explorou se a adição de um segundo sal, LiDFOB, poderia proteger o aço sem sacrificar os benefícios do LiFSI. Testes eletroquímicos mostraram que mesmo quantidades modestas de LiDFOB deslocaram o início da dissolução do aço inoxidável para tensões mais altas e reduziram drasticamente a corrente de corrosão. A microscopia confirmou que as pites praticamente desapareceram quando o LiDFOB estava presente. Técnicas espectroscópicas sensíveis à superfície revelaram que, em eletrólitos somente com LiFSI, espécies oxidada de ferro e cromo se combinam com fragmentos relacionados ao FSI, consistente com dissolução contínua. Em contraste, eletrólitos contendo LiDFOB deixaram mais ferro e cromo metálicos na superfície e introduziram compostos ricos em boro e flúor ligados à degradação do LiDFOB.
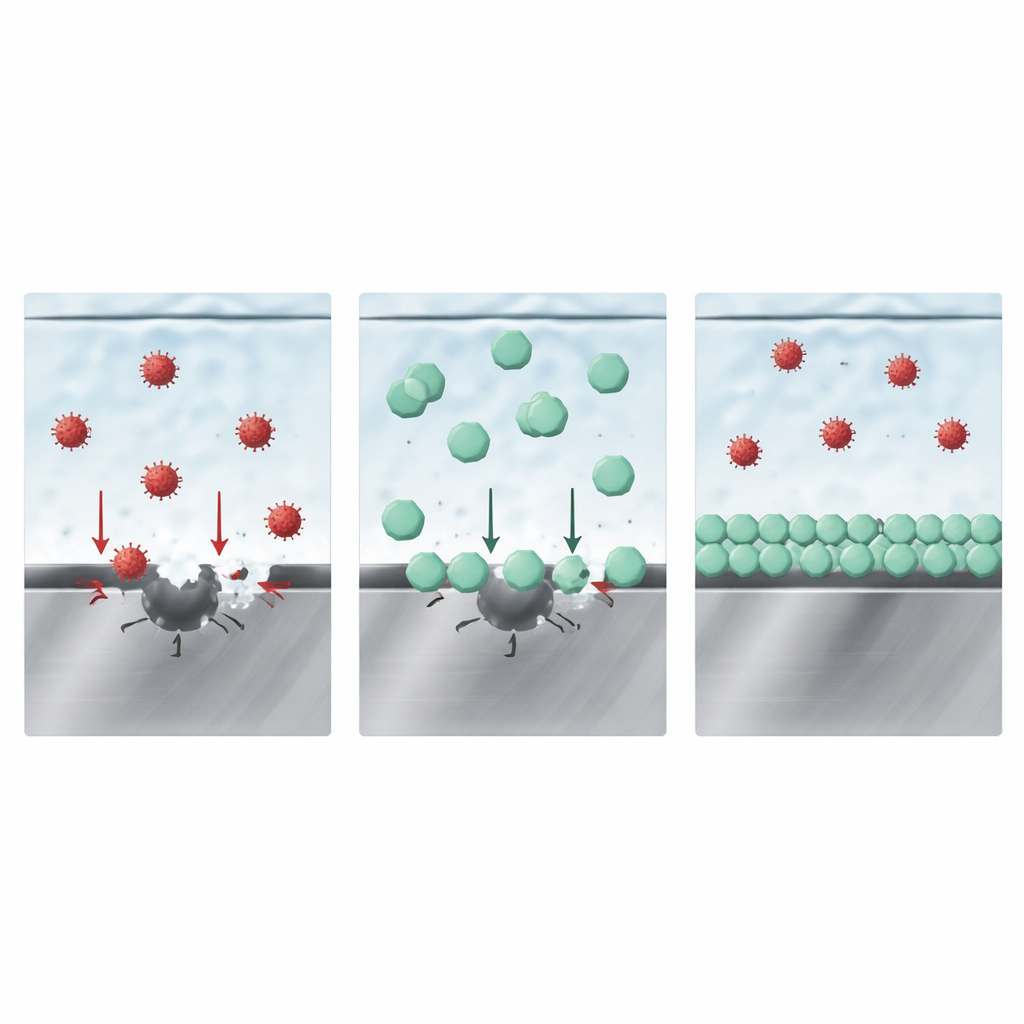
Como a camada protetora vence a competição
À primeira vista, pode parecer que uma película sólida contendo boro sozinha protege o aço. No entanto, experimentos adicionais de imersão e modelagem sugerem um quadro mais sutil. Os autores propõem que a chave é a competição entre diferentes ânions pelo espaço diretamente na superfície do metal. Medições do comportamento da carga de superfície, juntamente com simulações computacionais, mostram que o ânion do LiDFOB se liga mais fortemente à superfície de óxido de ferro do que tanto o cloreto quanto o FSI. Em termos práticos, os ânions do LiDFOB ocupam a camada mais interna do líquido na interface com o aço, tomando os próprios locais onde os íons agressivos iniciariam o ataque. Ao bloquear o acesso, eles suprimem tanto a pitagem inicial induzida por cloreto quanto a dissolução profunda dirigida pelo FSI que segue, o que por sua vez reduz a evolução de gases e o depósito de metal em outras partes da célula.
Do mecanismo a baterias com melhor desempenho
Para testar se essa proteção química se traduz em benefícios no mundo real, os pesquisadores ciclaram células grafite||NMC811 e silício-grafite||NMC811 usando diferentes eletrólitos e graus de aço inoxidável. Células com apenas LiFSI falharam precocemente devido à dissolução do metal, enquanto aquelas usando eletrólitos mistos LiFSI–LiDFOB mostraram vidas úteis muito mais longas. Quando um aço inoxidável mais resistente à corrosão (SUS316L) foi combinado com o eletrólito otimizado de sal duplo, células de silício-grafite alcançaram cerca de 300 ciclos até 80% da capacidade remanescente. Células pouch sem componentes de aço inoxidável, mas usando o mesmo eletrólito, também duraram aproximadamente o dobro em comparação com uma formulação convencional à base de LiPF6, destacando o efeito estabilizador mais amplo do LiDFOB nas interfaces da bateria.
O que isso significa para a tecnologia do dia a dia
Em termos acessíveis, o estudo mostra que um sal promissor de alto desempenho, o LiFSI, pode corroer silenciosamente as peças de aço que mantêm uma bateria unida — especialmente quando traços de cloreto estão presentes. Os autores revelam que o cloreto abre pequenos buracos na película protetora, e o LiFSI então impede que esses buracos se fechem ao manter o ferro dissolvido no líquido, de modo que o dano se espalha. Ao adicionar LiDFOB, cujos íons preferencialmente se alinham na superfície do aço e mantêm os íons nocivos afastados, a corrosão é em grande parte interrompida, a geração de gases é reduzida e tanto células tipo moeda quanto pouch duram muito mais. Essa combinação de um sal poderoso, porém corrosivo, com um sal “guarda-costas” escolhido de forma inteligente oferece uma receita prática para baterias de íon-lítio de alta energia, mais seguras e com vida útil prolongada, que podem chegar a veículos elétricos futuros e a células de grande formato.
Citação: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Palavras-chave: baterias de íon-lítio, aditivos para eletrólitos, corrosão do aço inoxidável, LiFSI, LiDFOB