Clear Sky Science · fr
Mécanisme et atténuation de la dissolution de l’acier inoxydable dans les électrolytes de batteries lithium-ion à base de LiFSI
Pourquoi cette recherche compte pour les batteries du futur
Les batteries lithium-ion alimentent tout, des ordinateurs portables aux voitures électriques, et les fabricants cherchent à augmenter leur capacité de stockage et leur vitesse de charge. Pour atteindre ces objectifs, de nouvelles recettes d’électrolytes et des électrodes à haute énergie sont adoptées. Un ingrédient prometteur d’électrolyte, nommé LiFSI, améliore la stabilité et les performances, mais présente un inconvénient caché : il peut corroder lentement les pièces en acier inoxydable à l’intérieur de la cellule. Cet article révèle précisément comment ce dommage se produit et propose une solution pratique pour l’empêcher, ouvrant la voie à des batteries haute énergie plus sûres et durables.
Dommages cachés à l’intérieur de l’enveloppe de la batterie
De nombreux formats commerciaux de batteries, y compris les cellules cylindriques et bouton, utilisent l’acier inoxydable pour les boîtiers et les composants internes. Dans des conditions normales, l’acier inoxydable se protège par un film d’oxyde fin et stable. Les auteurs montrent que, dans des électrolytes à base de LiFSI, cette protection peut échouer, notamment aux tensions plus élevées utilisées avec les cathodes riches en nickel modernes. De très faibles quantités de chlorure, souvent résiduelles après la production des sels, et l’anion FSI issu du LiFSI agissent de concert pour attaquer l’acier. Le chlorure initie le processus en créant des piqûres microscopiques à la surface. Une fois ces piqûres formées, du fer issu de l’acier inoxydable se dissout, et des espèces dérivées du FSI contribuent à maintenir ce fer en solution au lieu de laisser se reformer un oxyde protecteur, de sorte que le métal continue à se dissoudre et que les piqûres s’approfondissent.
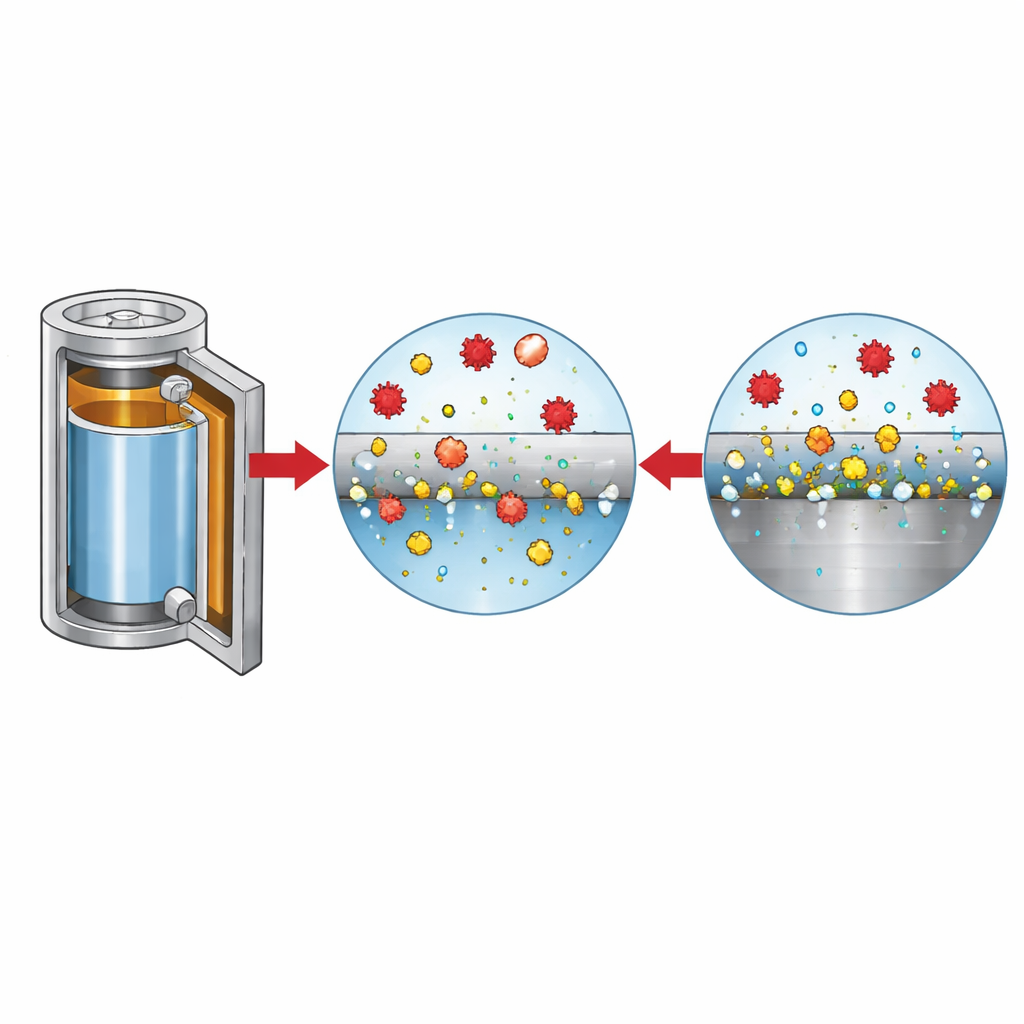
Comment des ions agressifs rongent le métal
Pour démêler les rôles des différents ions, les chercheurs ont fait varier systématiquement le niveau de chlorure et la composition des sels, tout en surveillant le courant, la morphologie de surface et l’évolution des gaz. À faibles teneurs en chlorure, la surface de l’acier se repasseive après une perturbation initiale, mais dès que le chlorure dépasse quelques dizaines de parties par million environ, les piqûres ne guérissent plus et la dissolution se poursuit. L’imagerie et l’analyse chimique révèlent que dans des solutions riches en chlorure, la surface devient parsemée d’oxydes de fer et de piqûres, tandis que dans des électrolytes purement à base de LiFSI, les piqûres sont moins nombreuses mais beaucoup plus profondes, le fer dissous formant des complexes solubles au lieu de précipiter. Ces ions métalliques dissous migrent à travers la cellule et se déposent sur l’électrode négative, rugosifiant la surface du lithium et contribuant à la formation de gaz tels que l’hydrogène et le dioxyde de carbone — deux phénomènes indésirables pour la sécurité et la durée de vie de la batterie.
Un sel protecteur qui reconfigure l’interface
L’équipe a ensuite exploré si l’ajout d’un second sel, le LiDFOB, pouvait protéger l’acier sans sacrifier les avantages du LiFSI. Les tests électrochimiques ont montré que même des quantités modestes de LiDFOB repoussaient le début de la dissolution de l’acier inoxydable vers des tensions plus élevées et réduisaient drastiquement le courant de corrosion. La microscopie a confirmé que les piqûres disparaissaient presque en présence de LiDFOB. La spectroscopie sensible à la surface a révélé que, dans les électrolytes contenant uniquement du LiFSI, des espèces d’oxyde de fer et de chrome oxydées se combinent avec des fragments liés au FSI, en accord avec une dissolution en cours. En revanche, les électrolytes contenant du LiDFOB laissaient plus de fer et de chrome métalliques en surface et introduisaient des composés riches en bore et en fluor associés à la décomposition du LiDFOB.
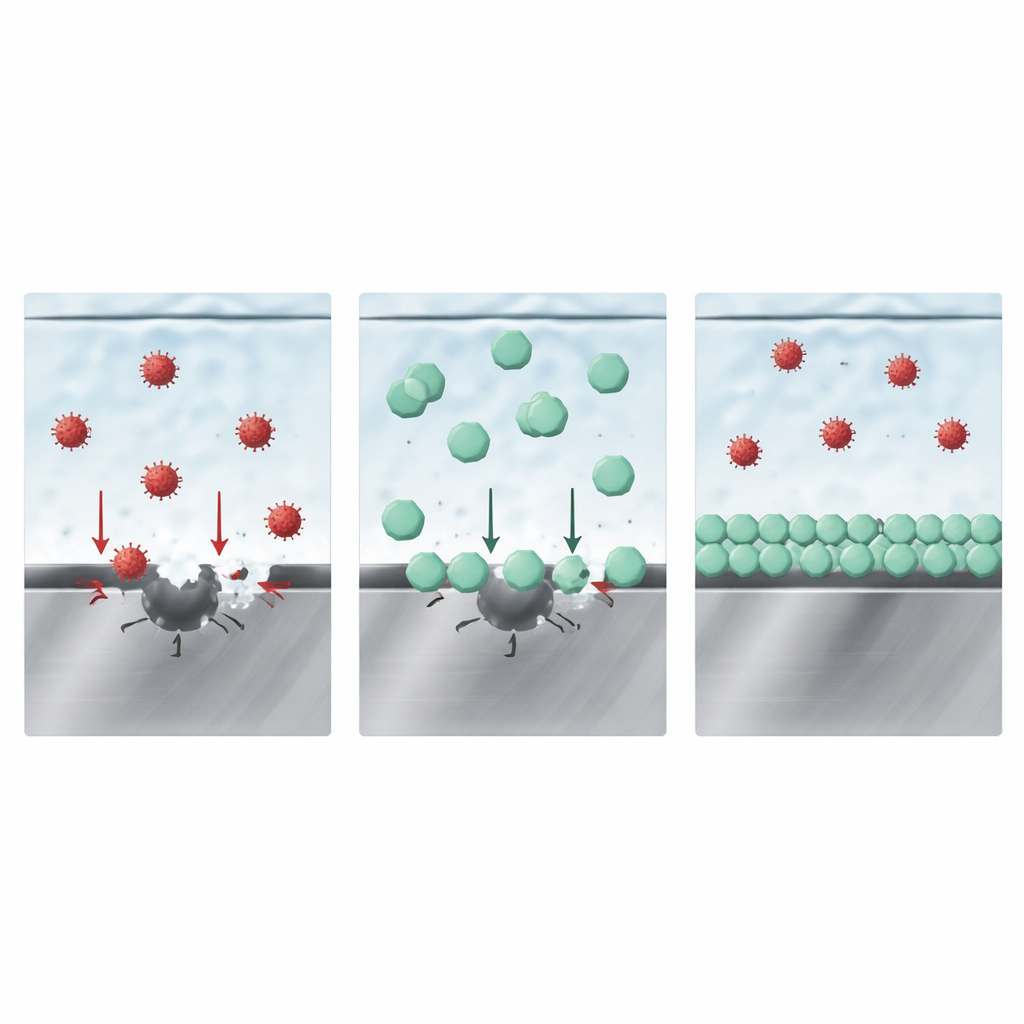
Comment la couche protectrice l’emporte dans la compétition
À première vue, on pourrait penser qu’un film solide contenant du bore suffit à protéger l’acier. Cependant, des expériences d’immersion supplémentaires et des modélisations suggèrent un tableau plus subtil. Les auteurs proposent que la clé soit la compétition entre différents anions pour l’espace directement à la surface du métal. Des mesures du comportement de la charge de surface, ainsi que des simulations informatiques, montrent que l’anion du LiDFOB se lie plus fortement à la surface d’oxyde de fer que le chlorure ou le FSI. Concrètement, les anions du LiDFOB s’entassent dans la couche la plus interne du liquide à l’interface avec l’acier, occupant précisément les emplacements où les ions agressifs initiqueraient autrement l’attaque. En bloquant l’accès, ils suppriment à la fois la piqûration initiale provoquée par le chlorure et la dissolution profonde induite par le FSI qui suit, ce qui réduit à son tour l’évolution des gaz et le dépôt de métal ailleurs dans la cellule.
Du mécanisme à de meilleures batteries
Pour vérifier si cette protection chimique se traduit par des avantages réels, les chercheurs ont cyclé des cellules graphite||NMC811 et silicium-graphite||NMC811 en utilisant différents électrolytes et nuances d’acier inoxydable. Les cellules avec seulement du LiFSI échouaient tôt en raison de la dissolution du métal, tandis que celles utilisant des électrolytes mixtes LiFSI–LiDFOB montraient une durée de vie grandement prolongée. Lorsque de l’acier inoxydable plus résistant à la corrosion (SUS316L) a été combiné avec l’électrolyte à double sel optimisé, les cellules silicium-graphite ont atteint environ 300 cycles avant d’atteindre 80 % de capacité restante. Les cellules pouch dépourvues de pièces en acier inoxydable mais utilisant le même électrolyte ont également duré environ deux fois plus longtemps qu’avec une formulation conventionnelle à base de LiPF6, soulignant l’effet stabilisant plus large du LiDFOB sur les interfaces de batterie.
Ce que cela signifie pour la technologie du quotidien
En termes accessibles, l’étude montre qu’un sel performant, le LiFSI, peut corroder en silence les pièces en acier qui maintiennent une batterie — surtout quand des traces de chlorure sont présentes. Les auteurs révèlent que le chlorure ouvre de minuscules trous dans le film protecteur, et que le LiFSI empêche ensuite ces trous de se refermer en maintenant le fer dissous dans le liquide, de sorte que les dégâts se propagent. En ajoutant du LiDFOB, dont les anions se positionnent préférentiellement à la surface de l’acier et maintiennent les ions nuisibles à distance, la corrosion est largement arrêtée, la génération de gaz est réduite et les cellules bouton comme les pouch durent beaucoup plus longtemps. Cette combinaison d’un sel puissant mais corrosif avec un « garde du corps » salin judicieusement choisi offre une recette pratique pour des batteries lithium-ion haute énergie, plus sûres et plus durables, susceptibles d’équiper les véhicules électriques et les cellules grand format du futur.
Citation: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Mots-clés: batteries lithium-ion, additifs d’électrolyte, corrosion de l’acier inoxydable, LiFSI, LiDFOB