Clear Sky Science · ar
آلية وتخفيف ذوبان الفولاذ المقاوم للصدأ في إلكتروليتات بطاريات أيونات الليثيوم المبنية على LiFSI
لماذا يهم هذا البحث للبطاريات المستقبلية
تشغّل بطاريات أيونات الليثيوم كل شيء من الحواسيب المحمولة إلى السيارات الكهربائية، وتدفعها الشركات لتخزين طاقة أكبر والشحن بسرعة أكبر. للوصول إلى هذه الأهداف، يتم تبني تركيبات إلكتروليت جديدة وأقطاب عالية الطاقة. مكوّن إلكتروليت واعد يسمى LiFSI يحسّن الاستقرار والأداء، لكنه يأتي مع عيب خفي: يمكنه تآكل أجزاء الفولاذ المقاوم للصدأ داخل الخلية ببطء. تكشف هذه الورقة عن الكيفية التي يحدث بها ذلك الضرر بالضبط وتعرض وسيلة عملية لوقفه، مما يمهّد الطريق لبطاريات عالية الطاقة أكثر أمانًا وطويلة العمر.
ضرر خفي داخل غلاف البطارية
تستخدم العديد من أشكال البطاريات التجارية، بما في ذلك الخلايا الأسطوانية والعملات، الفولاذ المقاوم للصدأ للأغلفة والمكونات الداخلية. في الظروف العادية، يحمي الفولاذ المقاوم للصدأ نفسه بطبقة أكسيد رقيقة ومستقرة. يوضح المؤلفون أنه في الإلكتروليتات المعتمدة على LiFSI يمكن أن يفشل هذا الحاجز، خصوصًا عند الجهود الأعلى المستخدمة مع الكاثودات الغنية بالنيكل الحديثة. كميات ضئيلة من كلوريد الصوديوم، المتبقية غالبًا من إنتاج الملح، وأيون FSI من LiFSI تعملان معًا لمهاجمة الفولاذ. يبدأ الكلوريد العملية بإنشاء حفر مجهرية في السطح. بمجرد تشكّل هذه الحفر، يذوب الحديد من الفولاذ المقاوم للصدأ، وتساعد مركبات مشتقة من FSI في إبقاء ذلك الحديد في المحلول بدلًا من أن يعيد تكوين أكسيد واقٍ، فتستمر عملية الذوبان وتزداد عمق الحفر.
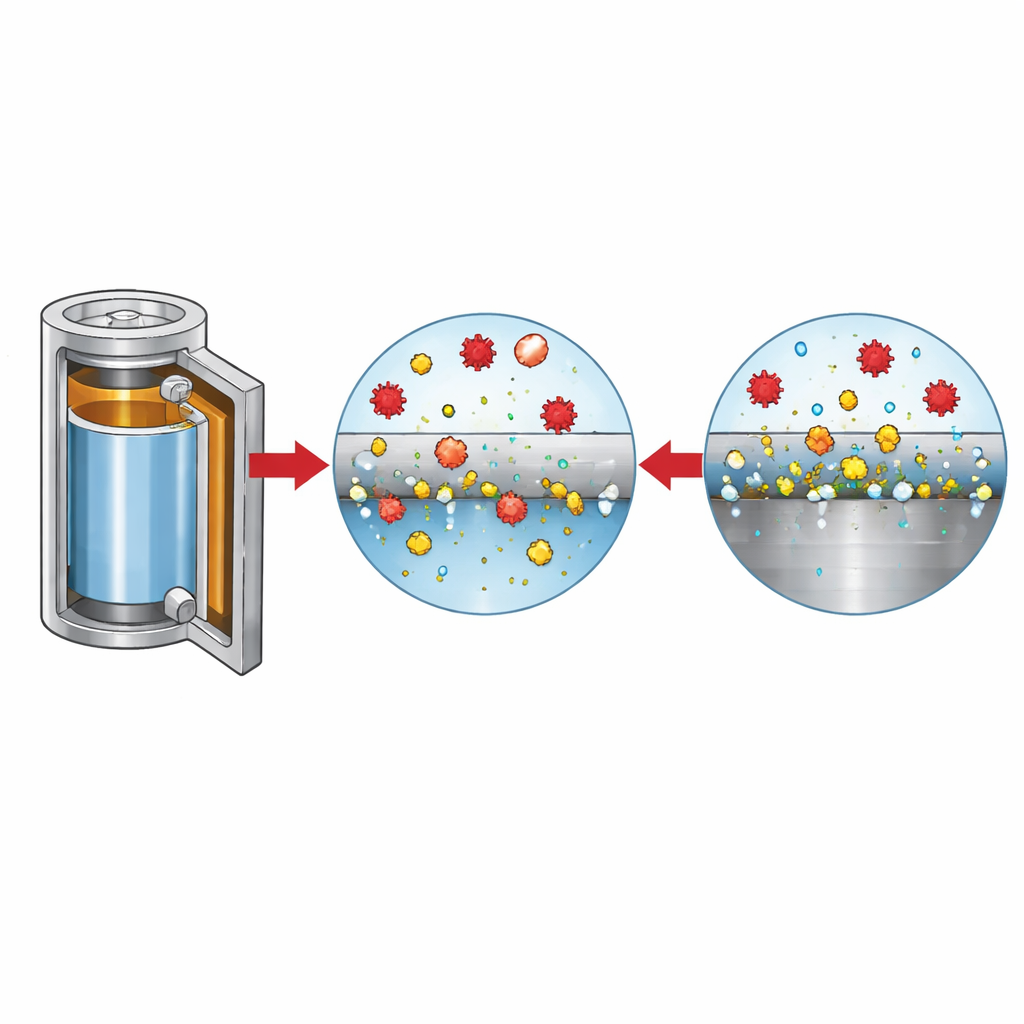
كيف تأكل الأيونات العدوانية المعدن
لفك أدوار الأيونات المختلفة، غيّر الباحثون مستوى الكلوريد وتركيبة الملح بشكل ممنهج بينما راقبوا التيار وبنية السطح وتطور الغازات. عند مستويات كلوريد منخفضة، يعيد السطح التمرٌّد بعد اضطرابٍ أولي، لكن بمجرد أن يتجاوز الكلوريد بضع عشرات من أجزاء في المليون تقريبًا، لا تلتئم الحفر ويستمر الذوبان. تُظهر الصور والتحليلات الكيميائية أن السطح في محاليل غنية بالكلوريد يصبح متنقّطًا بأكاسيد الحديد وحفر، بينما في إلكتروليتات LiFSI النقية تكون الحفر أقل عددًا ولكنها أعمق بكثير، مع تكوّن معقّ-dات ذائبة للحديد بدلًا من ترسّبها. تنتقل هذه الأيونات المعدنية المذابة عبر الخلية وتترسّب على القطب السالب، مسببة خشونة على سطح الليثيوم والمساهمة في تكوّن غازات مثل الهيدروجين وثاني أكسيد الكربون—وهما أمران غير مرغوبين لسلامة البطارية وعمرها.
ملح مساعد واقٍ يعيد تشكيل الواجهة
استكشف الفريق بعد ذلك ما إذا كان إضافة ملح ثانٍ، LiDFOB، يمكن أن يحمي الفولاذ دون التضحية بفوائد LiFSI. أظهرت الاختبارات الكهروكيميائية أن كميات متواضعة من LiDFOB دفعت عتبة بدء ذوبان الفولاذ المقاوم للصدأ إلى جهود أعلى وقلّلت بشكل كبير من تيار التآكل. أكدت الميكروسكوبات أن الحفر كادت تختفي بوجود LiDFOB. كشفت الطيفيات الحساسة للسطح أنه في الإلكتروليتات القائمة على LiFSI فقط، تتحد أنواع مؤكسدة من الحديد والكروم مع شظايا مرتبطة بـFSI، ما يتوافق مع استمرار الذوبان. بالمقابل، تركت الإلكتروليتات المحتوية على LiDFOB مزيدًا من الحديد والكروم المعدنيين على السطح وقدّمت مركبات غنية بالبورون والفلور مرتبطة بتحلل LiDFOB.
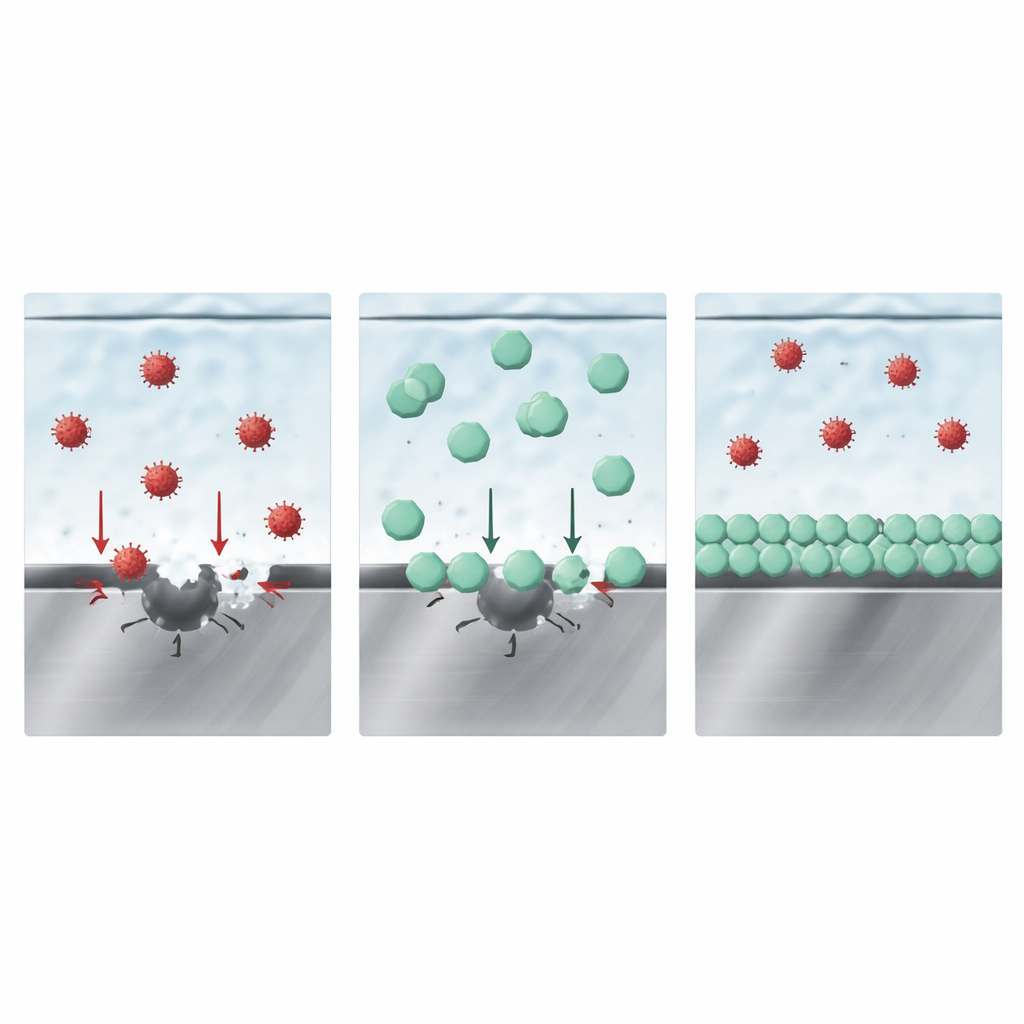
كيف يفوز الطبقة الواقية في المنافسة
قد يبدو للوهلة الأولى أن فيلمًا صلبًا يحتوي على البورون وحده يحمي الفولاذ. مع ذلك، أشارت تجارب انغماس إضافية ونمذجات إلى صورة أكثر دقّة. يقترح المؤلفون أن المفتاح هو التنافس بين الأنيونات المختلفة على المساحة مباشرةً على سطح المعدن. تُظهر قياسات سلوك الشحنة السطحية، جنبًا إلى جنب مع محاكاة حاسوبية، أن أنيون LiDFOB يرتبط بقوة أكبر بسطح أكسيد الحديد مقارنة بالكلوريد أو FSI. عمليًا، تتكدّس أنيونات LiDFOB في الطبقة الأقرب إلى السطح عند واجهة الفولاذ، فتحتل المواضع التي كان يمكن أن تبدأ فيها الأيونات العدوانية الهجوم. من خلال حجب الوصول، فإنها تكبح كلًا من حفر الكلوريد الأولية وذوبان FSI العميق التالي، مما يقلل بدوره من تطور الغازات وترسّب المعادن في أجزاء أخرى من الخلية.
من الآلية إلى بطاريات ذات أداء أفضل
لاختبار ما إذا كان هذا الحماية الكيميائية تترجم إلى فوائد واقعية، مرّن الباحثون خلايا جرافيت||NMC811 وخلايا سيليكون-جرافيت||NMC811 باستخدام إلكتروليتات ودرجات مختلفة من الفولاذ المقاوم للصدأ. فشلت الخلايا التي تحتوي على LiFSI وحده مبكرًا بسبب ذوبان المعدن، بينما أظهرت الخلايا التي استخدمت إلكتروليتات مختلطة LiFSI–LiDFOB أعمارًا أطول بكثير. عندما تم الجمع بين فولاذ مقاوم للتآكل أكثر (SUS316L) والإلكتروليت ثنائي الأملاح المحسّن، بلغت خلايا السيليكون-جرافيت حوالى 300 دورة حتى تصل السعة المتبقية إلى 80%. كذلك، استمرت خلايا الحقيبة التي لا تحتوي على أجهزة من الفولاذ المقاوم ولكنها استخدمت نفس الإلكتروليت تقريبًا ضعف المدة مقارنة بصيغة تقليدية معتمدة على LiPF6، مما يبرز التأثير الموثّب الأوسع لـLiDFOB على واجهات البطارية.
ماذا يعني هذا للتكنولوجيا اليومية
بعبارات مبسطة، تُظهر الدراسة أن ملحًا واعدًا عالي الأداء، LiFSI، يمكن أن يضعف بصمت أجزاء الفولاذ التي تربط البطارية معًا—وخاصة عند وجود أثر من الكلوريد. يكشف المؤلفون أن الكلوريد يفتح ثقوبًا صغيرة في الطبقة الواقية، ثم يمنع LiFSI التئام تلك الثقوب عبر إبقاء الحديد المذاب في السائل، فتنتشر الأضرار. بإضافة LiDFOB، الذي تصطف أيوناته تفضيليًا على سطح الفولاذ وتبعد الأيونات الضارة، يتوقف التآكل إلى حد كبير، وتقلّ توليد الغازات، وتدوم كل من خلايا العملة والحقيبة لفترة أطول بكثير. يقدم هذا المزيج من ملح قوي لكنه مؤكسد مع «ملح حارس» مختار بذكاء وصفة عملية لبطاريات أيونات الليثيوم عالية الطاقة أكثر أمانًا وطول عمر، قد تُستخدم في المركبات الكهربائية المستقبلية والخلايا ذات الحجم الكبير.
الاستشهاد: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
الكلمات المفتاحية: بطاريات أيونات الليثيوم, إضافات الإلكتروليت, تآكل الفولاذ المقاوم للصدأ, LiFSI, LiDFOB