Clear Sky Science · es
Mecanismo y mitigación de la disolución del acero inoxidable en electrolitos de baterías de ion-litio a base de LiFSI
Por qué esta investigación importa para las baterías del futuro
Las baterías de ion-litio alimentan desde portátiles hasta coches eléctricos, y los fabricantes las presionan para almacenar más energía y cargarse más rápido. Para alcanzar esos objetivos se están adoptando nuevas fórmulas de electrolito y electrodos de alta energía. Un componente prometedor del electrolito, llamado LiFSI, mejora la estabilidad y el rendimiento, pero tiene un inconveniente oculto: puede corroer lentamente las piezas de acero inoxidable dentro de la celda. Este artículo descubre exactamente cómo ocurre ese daño y presenta una forma práctica de detenerlo, allanando el camino para baterías de alta energía más seguras y duraderas.
Daño oculto dentro de la carcasa de la batería
Muchos formatos comerciales de baterías, incluidas las cilíndricas y de botón, usan acero inoxidable para las carcazas y componentes internos. En condiciones normales, el acero inoxidable se protege con una película de óxido delgada y estable. Los autores muestran que en electrolitos a base de LiFSI esta protección puede fallar, especialmente a los voltajes más altos que se usan con cátodos modernos ricos en níquel. Pequeñas cantidades de cloruro, a menudo residuales de la producción de la sal, y el anión FSI procedente del LiFSI actúan conjuntamente para atacar el acero. El cloruro inicia el proceso creando picaduras microscópicas en la superficie. Una vez que se forman estas picaduras, el hierro del acero inoxidable se disuelve, y las especies derivadas del FSI ayudan a mantener ese hierro en solución en lugar de permitir que vuelva a formar un óxido protector, de modo que el metal sigue disolviéndose y las picaduras se profundizan.
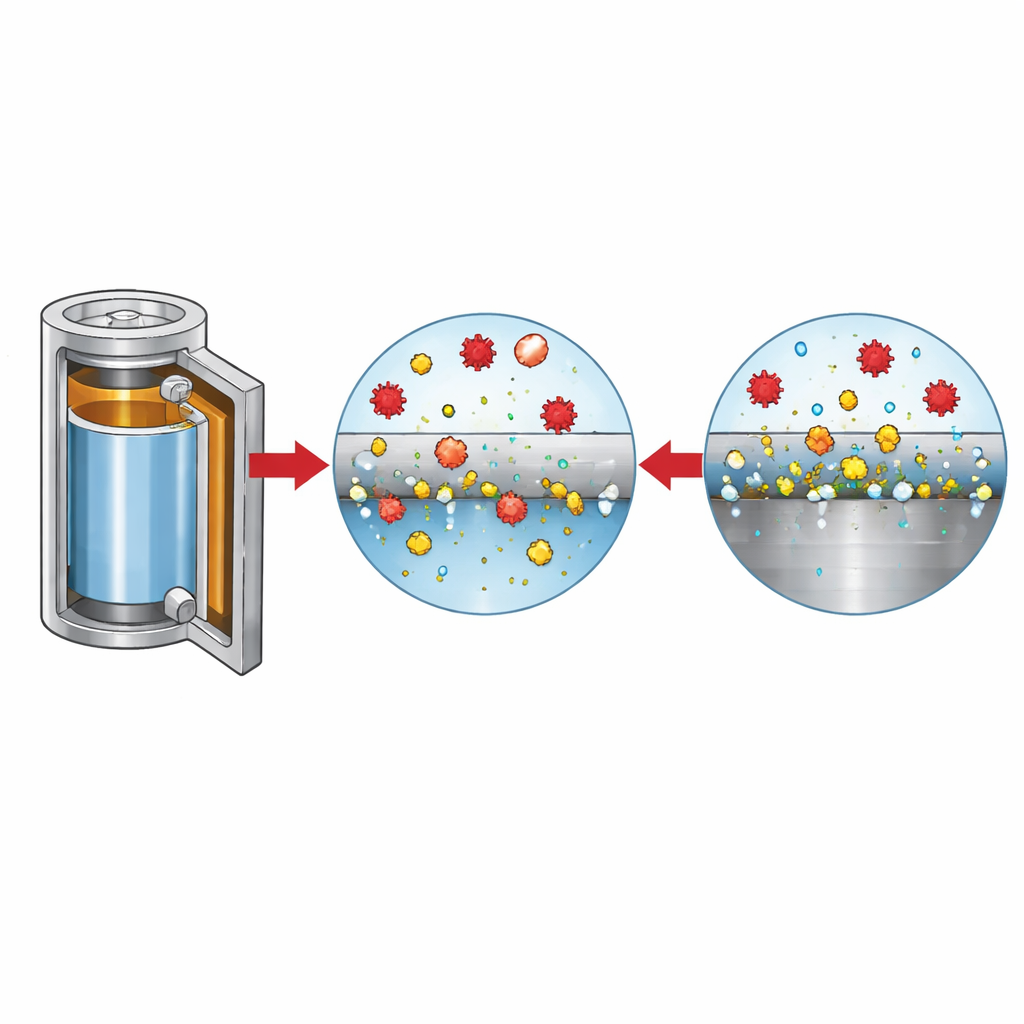
Cómo los iones agresivos devoran el metal
Para desenredar los roles de los distintos iones, los investigadores variaron sistemáticamente el nivel de cloruro y la composición de la sal, mientras monitorizaban la corriente, la morfología superficial y la evolución de gases. A niveles bajos de cloruro, la superficie de acero vuelve a pasivarse tras una perturbación inicial, pero una vez que el cloruro supera unas pocas decenas de partes por millón, las picaduras ya no se curan y la disolución continúa. Las imágenes y el análisis químico revelan que en soluciones ricas en cloruro la superficie queda salpicada de óxidos de hierro y picaduras, mientras que en electrolitos de LiFSI puro las picaduras son menos numerosas pero mucho más profundas, con hierro disuelto que forma complejos solubles en lugar de precipitar. Estos iones metálicos disueltos migran a través de la celda y se depositan en el electrodo negativo, rugosizando la superficie del litio y contribuyendo a la formación de gases como hidrógeno y dióxido de carbono, ambos indeseables para la seguridad y la vida útil de la batería.
Una sal auxiliar protectora que remodela la interfaz
El equipo exploró si añadir una segunda sal, LiDFOB, podría proteger el acero sin sacrificar los beneficios del LiFSI. Las pruebas electroquímicas mostraron que incluso cantidades modestas de LiDFOB desplazaron el inicio de la disolución del acero inoxidable a voltajes más altos y redujeron drásticamente la corriente de corrosión. La microscopía confirmó que las picaduras prácticamente desaparecían cuando estaba presente LiDFOB. La espectroscopía sensible a la superficie reveló que, en electrolitos solo con LiFSI, el hierro y el cromo oxidados se combinan con fragmentos relacionados con FSI, coherente con una disolución continua. En cambio, los electrolitos que contenían LiDFOB dejaron más hierro y cromo metálicos en la superficie e introdujeron compuestos ricos en boro y flúor vinculados a la descomposición de LiDFOB.
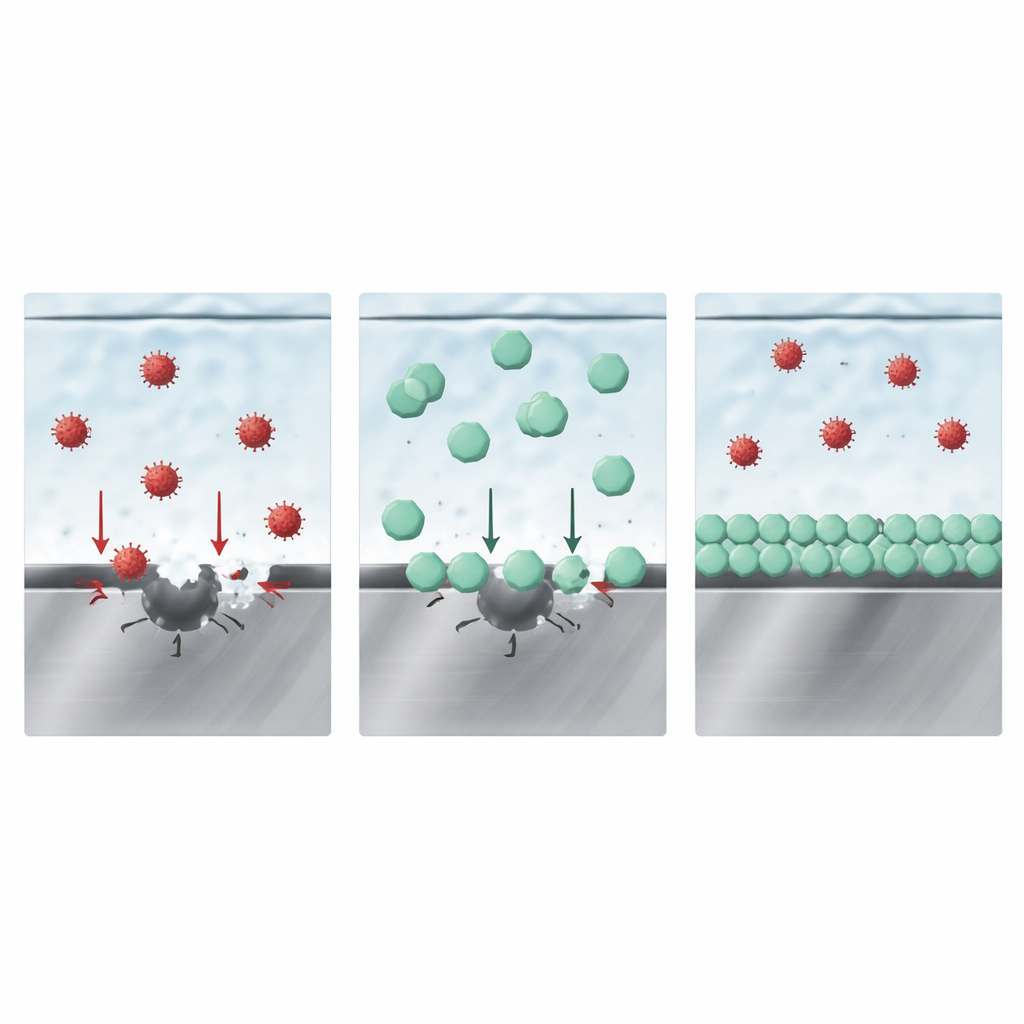
Cómo la capa protectora gana la competición
A primera vista podría parecer que una película sólida que contiene boro por sí sola protege el acero. Sin embargo, experimentos adicionales de inmersión y modelado sugirieron un panorama más sutil. Los autores proponen que la clave es la competencia entre diferentes aniones por el espacio justo en la superficie del metal. Medidas del comportamiento de la carga superficial, junto con simulaciones por ordenador, muestran que el anión del LiDFOB se une con más fuerza a la superficie de óxido de hierro que el cloruro o el FSI. En términos prácticos, los aniones de LiDFOB se agolpan en la capa más íntima del líquido en la interfaz con el acero, ocupando los mismos lugares donde los iones agresivos iniciarían el ataque. Al bloquear el acceso, suprimen tanto la pitting inicial impulsada por cloruros como la disolución profunda impulsada por FSI que le sigue, lo que a su vez reduce la evolución de gases y la deposición de metal en otras partes de la celda.
Del mecanismo a baterías con mejor rendimiento
Para comprobar si esta protección química se traduce en beneficios en el mundo real, los investigadores ciclaron celdas graphite||NMC811 y silicio-graphite||NMC811 usando distintos electrolitos y grados de acero inoxidable. Las celdas con solo LiFSI fallaron pronto por la disolución del metal, mientras que las que usaron electrolitos mixtos LiFSI–LiDFOB mostraron vidas mucho más largas. Cuando un acero inoxidable más resistente a la corrosión (SUS316L) se combinó con el electrolito de doble sal optimizado, las celdas de silicio-graphite alcanzaron alrededor de 300 ciclos hasta un 80% de capacidad restante. Las celdas pouch sin componentes de acero inoxidable pero usando el mismo electrolito también duraron aproximadamente el doble que con una formulación convencional basada en LiPF6, destacando el efecto estabilizador más amplio de LiDFOB en las interfaces de la batería.
Qué significa esto para la tecnología cotidiana
En términos accesibles, el estudio demuestra que una sal prometedora de alto rendimiento, LiFSI, puede corroer silenciosamente las piezas de acero que sujetan una batería, especialmente cuando hay trazas de cloruro. Los autores revelan que el cloruro abre pequeños agujeros en la película protectora, y LiFSI impide que esos agujeros se cierren al mantener el hierro disuelto en el líquido, de modo que el daño se propaga. Al añadir LiDFOB, cuyos iones se alinean preferentemente en la superficie del acero y mantienen a raya a los iones dañinos, la corrosión se detiene en gran medida, se reduce la generación de gases y tanto las celdas de botón como las pouch duran mucho más. Esta combinación de una sal poderosa pero corrosiva con una “sal guardaespaldas” escogida inteligentemente ofrece una receta práctica para baterías de ion-litio de alta energía más seguras y de mayor vida útil que podrían emplearse en futuros vehículos eléctricos y celdas de gran formato.
Cita: Yan, P., Stan, M.C., Zhour, K. et al. Mechanism and mitigation of stainless steel dissolution in LiFSI-based lithium-ion battery electrolytes. Nat Commun 17, 3866 (2026). https://doi.org/10.1038/s41467-026-72530-5
Palabras clave: baterías de ion-litio, aditivos de electrolito, corrosión del acero inoxidable, LiFSI, LiDFOB