Clear Sky Science · sv
Kontinentomfattande genomisk övervakning av Plasmodium falciparum-malaria i hela Afrika söder om Sahara med snabb nanopore-sekvensering
Varför malariagen är viktiga i vardagen
Malaria dödar fortfarande hundratusentals människor varje år i Afrika söder om Sahara, och parasiten lär sig nya sätt att undkomma våra tester och läkemedel. Denna studie visar hur forskare och lokala vårdteam snabbt kan läsa parasitens genetiska kod i vanliga laboratorier i Afrika, så att länder kan se i nästan realtid var malaria blir svårare att diagnosticera och behandla.
Växande problem för tester och behandlingar
Den dödligaste malariaparasiten, Plasmodium falciparum, slår tillbaka mot två av våra huvudverktyg. Vissa stammar har förlorat gener som kallas hrp2 och hrp3, vilket gör att standard-snabbtester kan missa infektioner. Andra bär förändringar i en gen som kallas kelch13, vilka är kopplade till långsammare rensning av parasiter efter behandling med dagens första linjens läkemedel. Dessa oroande varianter har spridit sig över östra, centrala och södra Afrika. Hälsomyndigheter överväger att byta typ av tester eller rotera läkemedelskombinationer, men de behöver detaljerad och aktuell information om vilka parasitstammar som cirkulerar var.
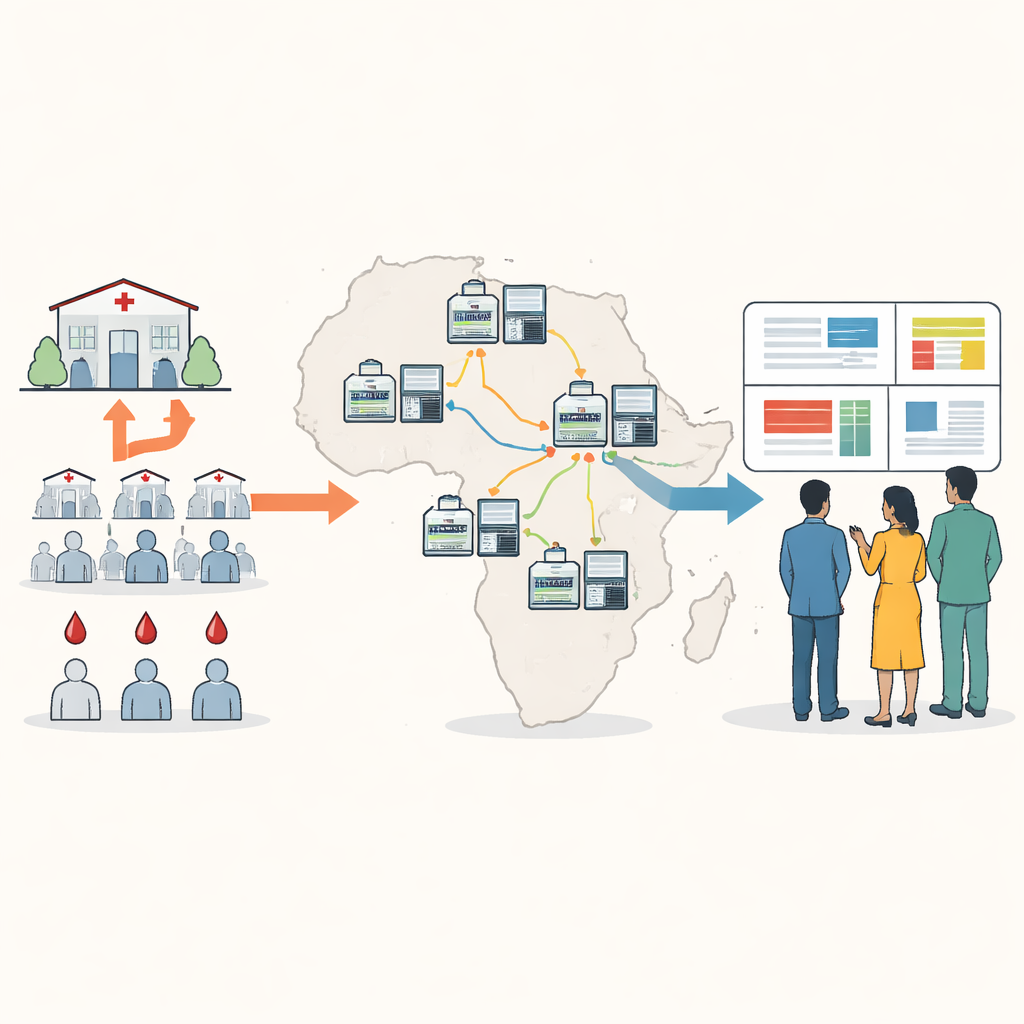
Att föra genetisk övervakning närmare patienterna
Traditionell DNA-sekvensering för malaria kräver ofta att blodprover skickas utomlands eller till några stora regionala centra, vilket kan vara långsamt, dyrt och avskilt från lokalt beslutsfattande. Författarna utformade en ny metod byggd kring en liten bärbar enhet känd som en nanopore-sekvenserare. Med hjälp av torkade blodfläckar tagna vid rutinmässig malariatestning kan lokal personal förstärka och sekvensera nyckelgener från parasiten på ungefär fem timmar, till en kostnad under tjugofem dollar per prov. Den nya "minimalt livskraftiga panelen" fokuserar på tio genetiska regioner som avslöjar läkemedelsresistens, närvaro eller frånvaro av hrp2 och hrp3, vaccinrelevanta förändringar och hur många olika parasitstammar som blandas i en enda infektion.
Enkel programvara på en vanlig laptop
För att göra metoden användbar på platser med begränsad internet- och datorkapacitet skapade teamet ett programpaket kallat Nomadic. Det körs på samma laptop som styr sekvenseraren och fungerar helt offline. Under sekvenseringen kartlägger programmet varje läsning mot parasitgenomet, kontrollerar kvalitet och flaggar viktiga mutationer, samtidigt som det visar intuitiva diagram i en lokal instrumentpanel. Programvaran producerar också kompakta sammanfattningsfiler som är lätta att dela via e-post eller långsamma uppkopplingar, vilket gör det möjligt för partner att kombinera resultat från många platser utan att flytta stora rådatafiler.
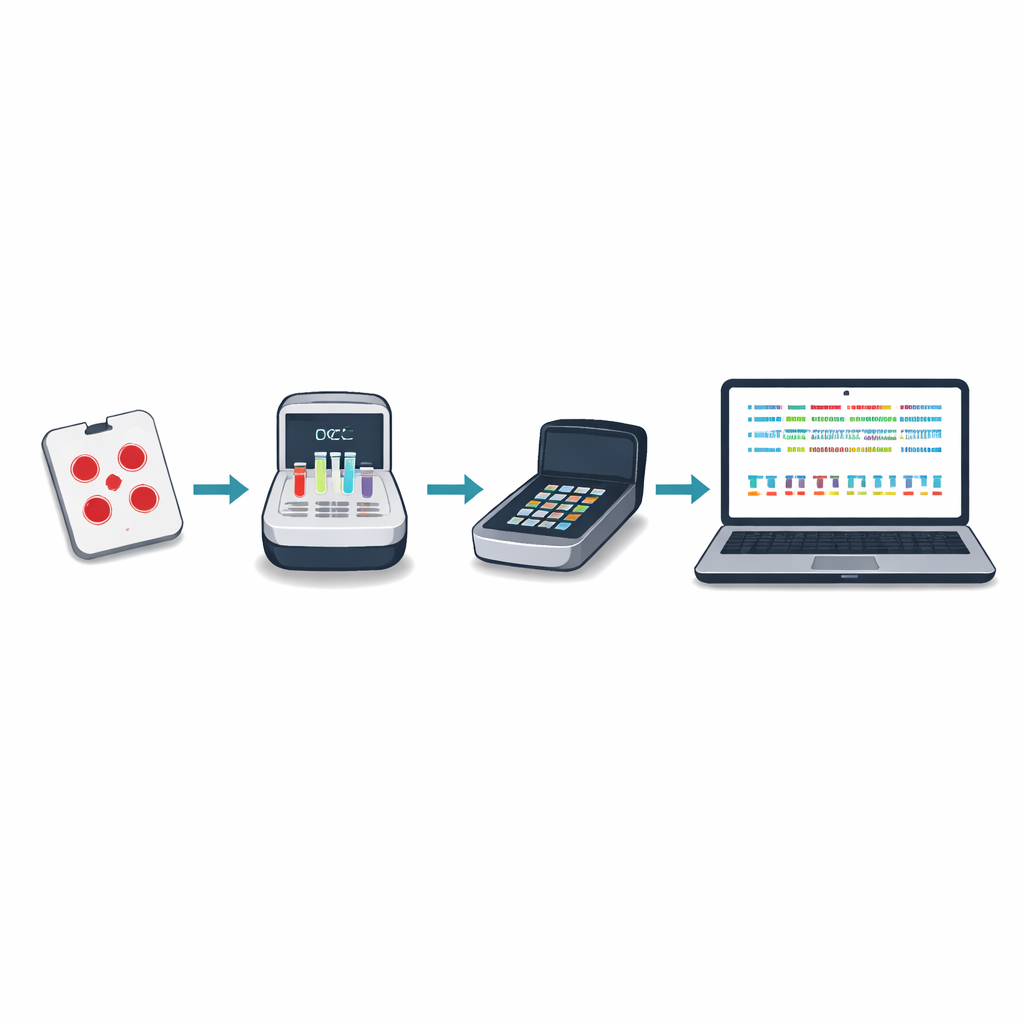
Test av systemet över Afrika
Mellan 2024 och 2025 använde laboratorier i sex afrikanska länder protokollet för att sekvensera och analysera över tusen malariaprover, de flesta bearbetade lokalt av 13 forskare med varierande grad av tidigare erfarenhet. Metoden gav stark och konsekvent täckning av målgenerna över ett brett spektrum av parasitnivåer i blodet. Ett nytt variantavkallningsverktyg, kallat Delve, kunde tillförlitligt upptäcka genetiska förändringar som bars av minoritetsparasiter som utgjorde så lite som fem till tio procent av en infektion — en nivå som standardverktyg ofta missar. Samma sekvenseringskörningar identifierade också korrekt nästan alla deletioner i hrp2- och hrp3-generna jämfört med konventionella laboratoriemetoder, och i vissa blandade infektioner upptäckte de deletioner som standardtester missade.
Vad detta betyder för kampen mot malaria
Detta arbete visar att högkvalitativ genetisk övervakning av malaria inte behöver begränsas till avlägsna högteknologiska centra. Genom att kombinera ett prisvärt, strömlinjeformat laboratorieprotokoll med laptopbaserad analys kan vanliga folkhälsolaboratorier spåra markörer för läkemedelsresistens och svårupptäckta diagnostik-undvikande parasiter i nästan realtid. Medan andra metoder fortfarande är bättre lämpade för vissa specialuppgifter, passar detta tillvägagångssätt väl för det akuta behovet av snabb, praktisk information för att styra val av tester och behandlingspolicyer i hela Afrika söder om Sahara.
Citering: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Nyckelord: malaria, genomisk övervakning, läkemedelsresistens, nanopore-sekvensering, Afrika söder om Sahara