Clear Sky Science · fr
Surveillance génomique à l'échelle continentale du paludisme à Plasmodium falciparum en Afrique subsaharienne par séquençage nanopore rapide
Pourquoi les gènes du paludisme comptent dans la vie quotidienne
Le paludisme tue encore des centaines de milliers de personnes chaque année en Afrique subsaharienne, et le parasite apprend de nouvelles stratégies pour échapper à nos tests et médicaments. Cette étude montre comment des scientifiques et des équipes de santé locales peuvent lire rapidement le code génétique du parasite dans des laboratoires africains ordinaires, afin que les pays puissent voir en quasi-temps réel où le paludisme devient plus difficile à diagnostiquer et à traiter.
Des problèmes grandissants pour les tests et les traitements
Le parasite le plus mortel, Plasmodium falciparum, fait front contre deux de nos principaux outils. Certaines souches ont perdu des gènes appelés hrp2 et hrp3, ce qui fait que les tests rapides standard peuvent manquer des infections. D'autres portent des modifications dans un gène connu sous le nom de kelch13, liées à une élimination plus lente des parasites après traitement par les médicaments de première ligne actuels. Ces variants préoccupants se sont propagés à travers l'Afrique orientale, centrale et australe. Les agences de santé envisagent de changer de type de tests ou de faire tourner les combinaisons de médicaments, mais elles ont besoin d'informations détaillées et actualisées sur les souches de parasites en circulation et leur répartition géographique.
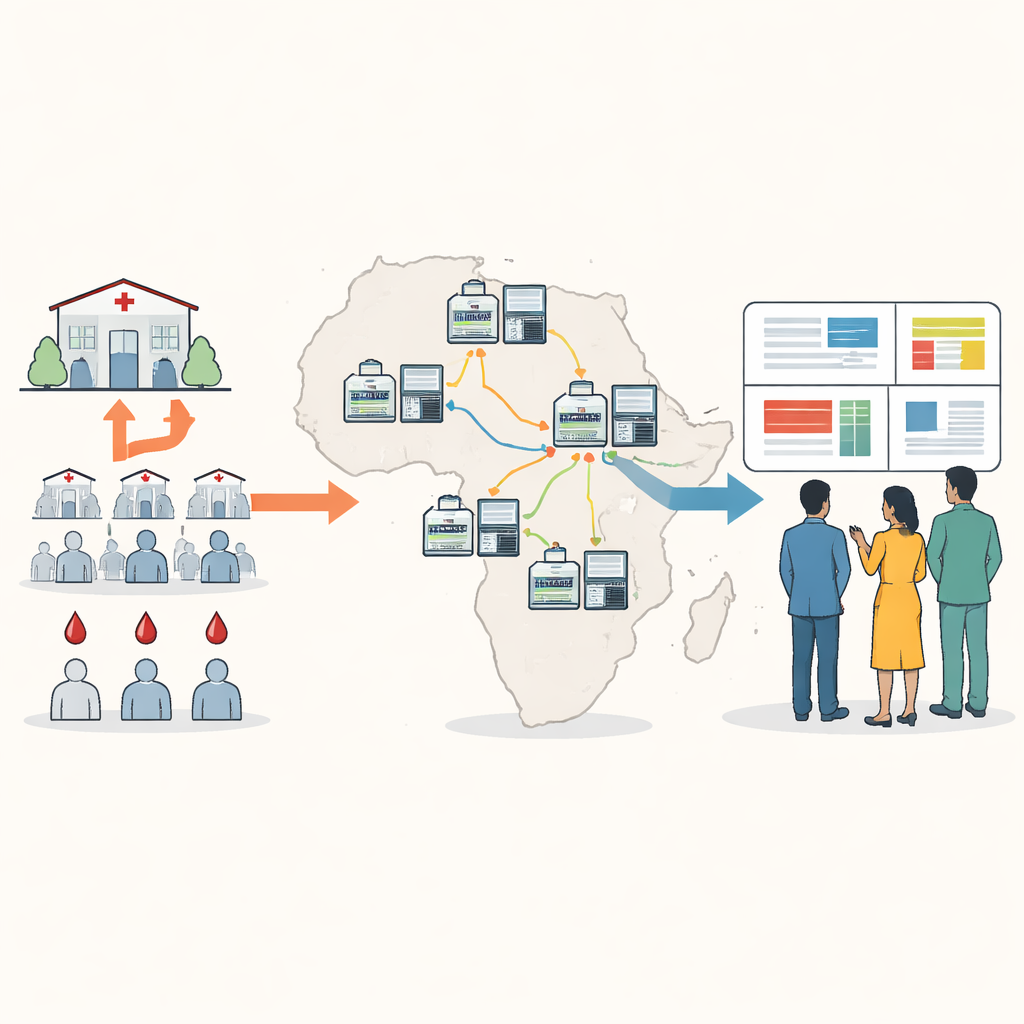
Rapprocher le suivi génétique des patients
Le séquençage génétique traditionnel du paludisme nécessite souvent l'envoi d'échantillons de sang à l'étranger ou à quelques grands centres régionaux, ce qui peut être lent, coûteux et déconnecté de la prise de décision locale. Les auteurs ont conçu une nouvelle approche centrée sur un petit appareil portable connu sous le nom de séquenceur nanopore. À partir de points de sang séchés prélevés lors du dépistage routinier, le personnel local peut amplifier et séquencer des gènes clés du parasite en environ cinq heures, à un coût inférieur à vingt-cinq dollars par échantillon. Le nouveau « panel minimal viable » se concentre sur dix régions génétiques qui révèlent la résistance aux médicaments, la présence ou l'absence de hrp2 et hrp3, des modifications d'intérêt pour les vaccins, et le nombre de souches parasitaires différentes présentes dans une même infection.
Un logiciel simple sur un ordinateur portable ordinaire
Pour rendre la méthode utilisable dans des lieux à connectivité internet et puissance de calcul limitées, l'équipe a créé un package logiciel appelé Nomadic. Il s'exécute sur le même ordinateur portable qui contrôle le séquenceur et fonctionne entièrement hors ligne. Pendant le séquençage, le programme aligne chaque lecture sur le génome du parasite, vérifie la qualité et signale les mutations importantes, tout en affichant des graphiques intuitifs dans un tableau de bord local. Le logiciel produit également des fichiers de synthèse compacts faciles à partager par e-mail ou via des connexions lentes, permettant aux partenaires de combiner des résultats provenant de nombreux sites sans transférer de gros fichiers de données brutes.
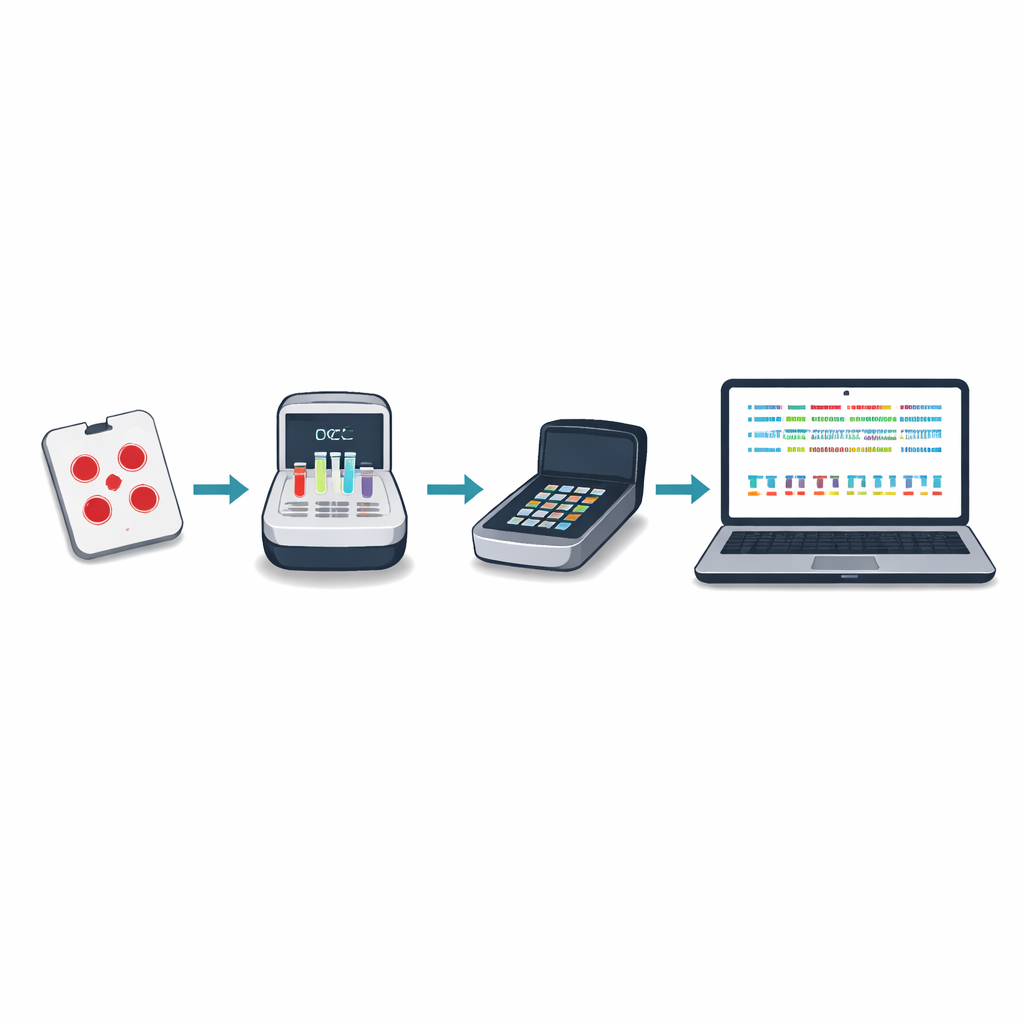
Tester le système à travers l'Afrique
Entre 2024 et 2025, des laboratoires de six pays africains ont utilisé le protocole pour séquencer et analyser plus de mille échantillons de paludisme, la plupart traités localement par 13 scientifiques ayant des niveaux d'expérience variés. La méthode a produit une couverture solide et cohérente des gènes ciblés sur une large gamme de charges parasitaires dans le sang. Un nouvel outil d'appel de variants, nommé Delve, a pu détecter de manière fiable des modifications génétiques portées par des souches minoritaires constituant seulement cinq à dix pour cent d'une infection, un niveau que les outils standard manquent souvent. Les mêmes séries de séquençage ont aussi identifié correctement presque toutes les délétions dans les gènes hrp2 et hrp3 comparé aux méthodes de laboratoire conventionnelles, et, dans certaines infections mixtes, ont détecté des délétions que les tests standard avaient négligées.
Ce que cela signifie pour la lutte contre le paludisme
Ce travail montre que la surveillance génétique de haute qualité du paludisme n'a pas à être confinée à des centres high-tech lointains. En associant un protocole de laboratoire abordable et simplifié à une analyse sur ordinateur portable, des laboratoires de santé publique ordinaires peuvent suivre en quasi-temps réel les marqueurs de résistance aux médicaments et les parasites furtifs qui échappent au diagnostic. Bien que d'autres méthodes restent mieux adaptées à certaines tâches spécialisées, cette approche répond bien au besoin urgent d'informations rapides et pratiques pour orienter le choix des tests et les politiques de traitement à travers l'Afrique subsaharienne.
Citation: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Mots-clés: paludisme, surveillance génomique, résistance aux médicaments, séquençage nanopore, Afrique subsaharienne