Clear Sky Science · nl
Genomische surveillance op continentaal niveau van Plasmodium falciparum-malaria in sub-Sahara Afrika met snelle nanopore-sequencing
Waarom malariagenen van belang zijn voor het dagelijks leven
Malaria veroorzaakt nog steeds honderden duizenden doden per jaar in sub-Sahara Afrika, en de parasiet leert nieuwe trucs om onze testen en medicijnen te omzeilen. Deze studie laat zien hoe wetenschappers en lokale gezondheids teams in gewone Afrikaanse laboratoria snel de genetische code van de parasiet kunnen lezen, zodat landen bijna in realtime kunnen zien waar malaria moeilijker te diagnosticeren en te behandelen wordt.
Toenemende problemen voor testen en behandelingen
De dodelijkste malariaparasiet, Plasmodium falciparum, verzet zich tegen twee van onze belangrijkste instrumenten. Sommige stammen hebben de genen hrp2 en hrp3 verloren, waardoor standaard snelle tests infecties kunnen missen. Andere dragen veranderingen in een gen dat bekendstaat als kelch13, die worden gelinkt aan vertraagde klaring van parasieten na behandeling met de huidige eerstelijnsgeneesmiddelen. Deze verontrustende varianten verspreiden zich over Oost-, Centraal- en Zuid-Afrika. Gezondheidsinstanties overwegen het type test te veranderen of combinaties van geneesmiddelen te rouleren, maar zij hebben gedetailleerde en tijdige informatie nodig over welke parasietstammen waar circuleren.
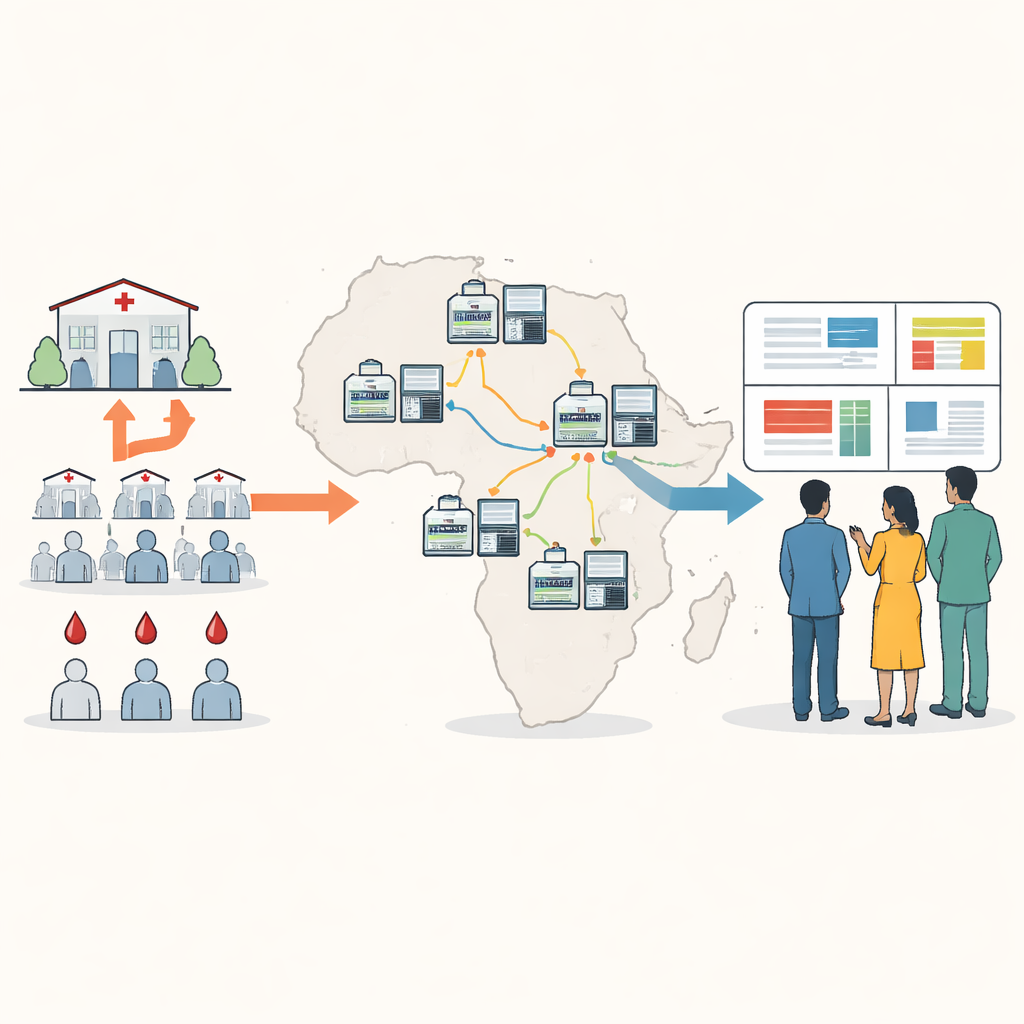
Genetische tracking dichter bij de patiënten brengen
Traditionele DNA-sequencing voor malaria vereist vaak het opsturen van bloedmonsters naar het buitenland of naar enkele grote regionale centra, wat traag, duur en losgekoppeld van lokale besluitvorming kan zijn. De auteurs ontwierpen een nieuwe benadering rond een klein draagbaar apparaat, bekend als een nanopore-sequencer. Met behulp van gedroogde bloedvlekken afkomstig van routinematige malariatesten kunnen lokale medewerkers sleutelgenen van de parasiet in ongeveer vijf uur amplificeren en sequencen, tegen een kostprijs van minder dan vijfentwintig dollar per monster. Het nieuwe “minimal viable panel” richt zich op tien genetische regio’s die resistentie tegen geneesmiddelen onthullen, de aanwezigheid of afwezigheid van hrp2 en hrp3, vaccingerelateerde veranderingen en hoeveel verschillende parasietstammen in één infectie gemengd zijn.
Eenvoudige software op een gewone laptop
Om de methode bruikbaar te maken op locaties met beperkte internet- en rekenkracht, ontwikkelde het team een softwarepakket genaamd Nomadic. Het draait op dezelfde laptop die de sequencer aanstuurt en werkt volledig offline. Terwijl het sequencen vordert, mappt het programma elke read naar het parasietgenoom, controleert de kwaliteit en markeert belangrijke mutaties, terwijl het intuïtieve grafieken toont in een lokaal dashboard. De software genereert ook compacte samenvattingsbestanden die gemakkelijk per e-mail of via trage verbindingen gedeeld kunnen worden, waardoor partners resultaten van veel locaties kunnen combineren zonder grote ruwe data te verplaatsen.
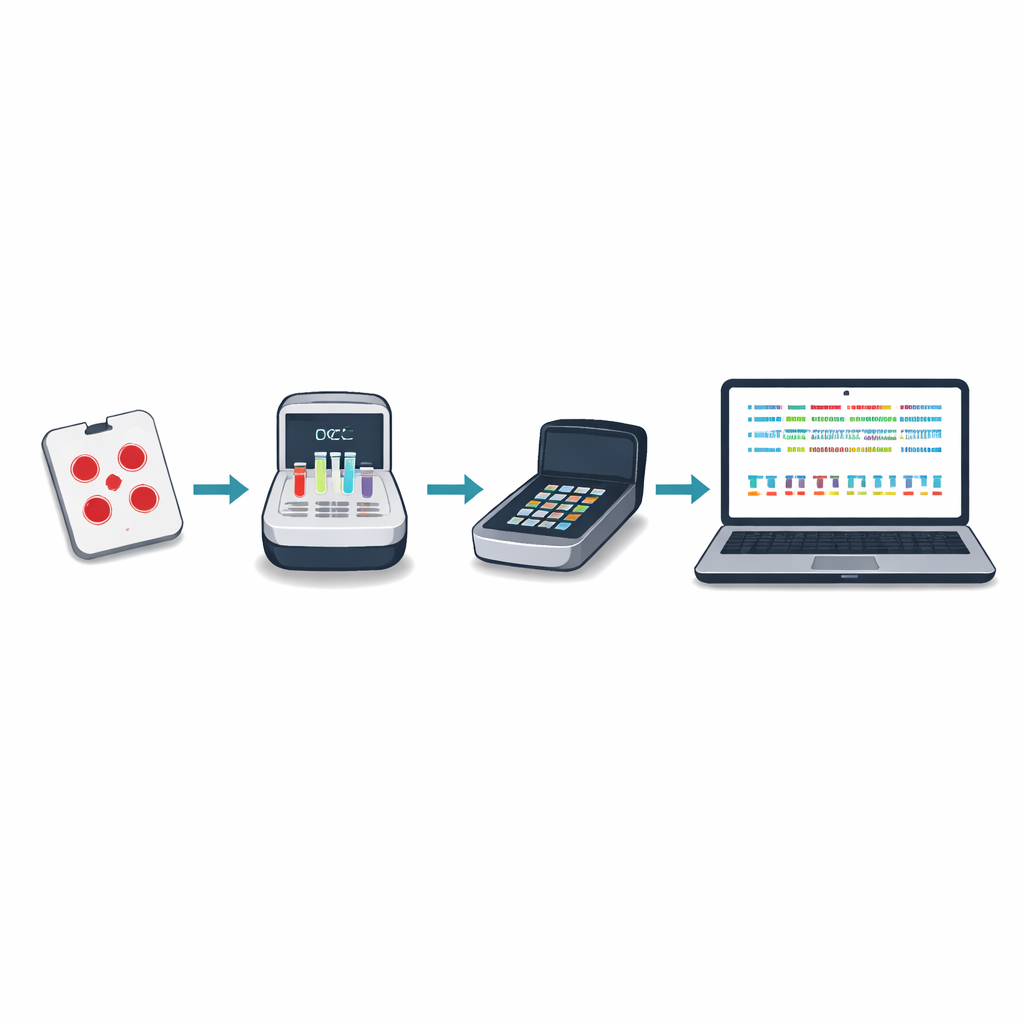
Het systeem testen in heel Afrika
Tussen 2024 en 2025 gebruikten laboratoria in zes Afrikaanse landen het protocol om meer dan duizend malariamonsters te sequencen en te analyseren, waarvan de meeste lokaal werden verwerkt door 13 onderzoekers met uiteenlopende ervaring. De methode leverde sterke en consistente dekking van de targetgenen over een breed scala aan parasietniveaus in bloed. Een nieuwe variant-detectietool, genaamd Delve, kon betrouwbaar genetische veranderingen detecteren die werden gedragen door minoritaire parasietstammen die slechts vijf tot tien procent van een infectie uitmaakten, een niveau dat standaardtools vaak missen. Dezelfde sequencelopen identificeerden ook vrijwel alle deleties in de hrp2- en hrp3-genen correct in vergelijking met conventionele laboratoriummethoden, en in sommige gemengde infecties ontdekte het deleties die standaardtests over het hoofd zagen.
Wat dit betekent voor de strijd tegen malaria
Deze studie toont aan dat hoogwaardige genetische surveillance van malaria niet beperkt hoeft te blijven tot verre hightechcentra. Door een betaalbaar, gestroomlijnd laboratoriumprotocol te koppelen aan laptopgebaseerde analyse, kunnen gewone volksgezondheidslaboratoria markers voor medicijnresistentie en sluipende diagnostiek-ontwijkende parasieten bijna in realtime volgen. Hoewel andere methoden voor sommige specialistische taken beter geschikt blijven, sluit deze benadering goed aan bij de dringende behoefte aan snelle, praktische informatie om testkeuzes en behandelrichtlijnen in sub-Sahara Afrika te sturen.
Bronvermelding: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Trefwoorden: malaria, genomische surveillance, medicijnresistentie, nanopore-sequencing, sub-Sahara Afrika