Clear Sky Science · pt
Vigilância genômica em escala continental do Plasmodium falciparum na África Subsaariana com sequenciamento rápido por nanopore
Por que os genes da malária importam no dia a dia
A malária ainda mata centenas de milhares de pessoas a cada ano na África Subsaariana, e o parasita vem aprendendo novas estratégias para escapar dos nossos testes e medicamentos. Este estudo mostra como cientistas e equipes de saúde locais podem ler rapidamente o código genético do parasita em laboratórios africanos comuns, permitindo que os países identifiquem quase em tempo real onde a malária está se tornando mais difícil de diagnosticar e tratar.
Problemas crescentes para testes e tratamentos
O parasita mais letal, Plasmodium falciparum, está reagindo contra duas de nossas principais ferramentas. Algumas linhagens perderam genes chamados hrp2 e hrp3, o que faz com que testes rápidos padrão deixem de detectar infecções. Outras apresentam alterações em um gene conhecido como kelch13, associadas à eliminação mais lenta dos parasitas após o tratamento com os medicamentos de primeira linha atuais. Essas variantes preocupantes têm se espalhado pelo leste, centro e sul da África. Agências de saúde consideram mudar os tipos de testes ou alternar combinações de medicamentos, mas precisam de informações detalhadas e oportunas sobre quais linhagens do parasita circulam em cada região.
Levando o rastreamento genético para mais perto dos pacientes
O sequenciamento tradicional de DNA para malária frequentemente exige o envio de amostras de sangue para o exterior ou para alguns grandes centros regionais, o que pode ser lento, caro e desconectado da tomada de decisão local. Os autores desenvolveram uma nova abordagem centrada em um pequeno dispositivo portátil conhecido como sequenciador por nanopore. Usando manchas de sangue seco coletadas em testes de rotina, a equipe local pode amplificar e sequenciar genes-chave do parasita em cerca de cinco horas, a um custo inferior a vinte e cinco dólares por amostra. O novo “painel viável mínimo” concentra-se em dez regiões genéticas que revelam resistência a medicamentos, presença ou ausência de hrp2 e hrp3, alterações relevantes para vacinas e quantas linhagens parasitárias diferentes estão misturadas em uma única infecção.
Software simples em um laptop comum
Para tornar o método utilizável em locais com internet e capacidade computacional limitadas, a equipe criou um pacote de software chamado Nomadic. Ele roda no mesmo laptop que controla o sequenciador e funciona inteiramente offline. À medida que o sequenciamento avança, o programa mapeia cada leitura para o genoma do parasita, verifica a qualidade e sinaliza mutações importantes, tudo isso exibindo gráficos intuitivos em um painel local. O software também produz arquivos de resumo compactos que são fáceis de compartilhar por e-mail ou conexões lentas, permitindo que parceiros combinem resultados de muitos locais sem transferir grandes arquivos brutos.
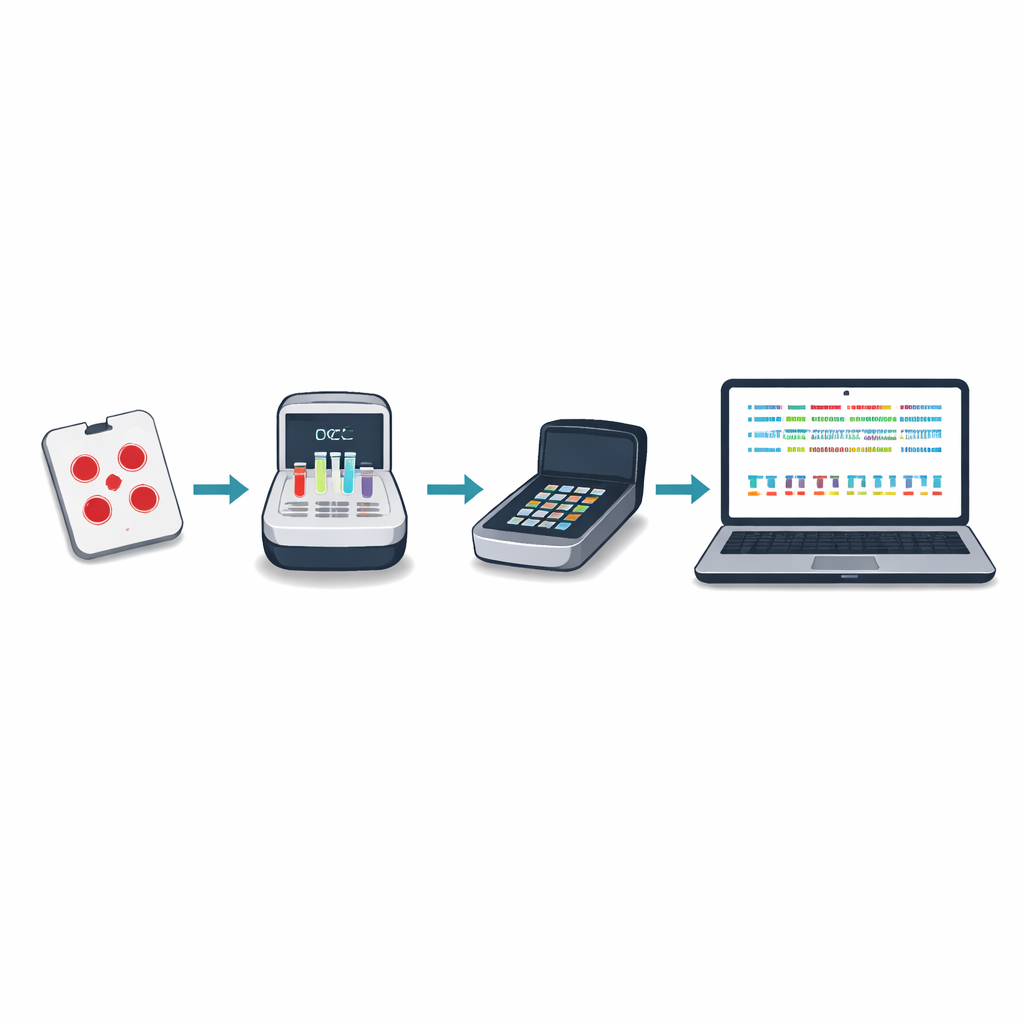
Testando o sistema por toda a África
Entre 2024 e 2025, laboratórios em seis países africanos usaram o protocolo para sequenciar e analisar mais de mil amostras de malária, a maioria processada localmente por 13 cientistas com níveis variados de experiência prévia. O método produziu cobertura forte e consistente dos genes-alvo em uma ampla gama de níveis parasitários no sangue. Uma nova ferramenta de chamada de variantes, chamada Delve, conseguiu detectar de forma confiável alterações genéticas presentes em linhagens minoritárias que representavam apenas cinco a dez por cento de uma infecção, níveis que ferramentas padrão frequentemente deixam passar. As mesmas corridas de sequenciamento também identificaram corretamente quase todas as deleções nos genes hrp2 e hrp3 quando comparadas com métodos laboratoriais convencionais e, em algumas infecções mistas, detectaram deleções que testes padrão haviam deixado passar.
O que isso significa para a luta contra a malária
Este trabalho mostra que vigilância genética de alta qualidade da malária não precisa ficar limitada a centros de alta tecnologia distantes. Ao combinar um protocolo de laboratório acessível e simplificado com análise em laptops, laboratórios de saúde pública comuns podem monitorar marcadores de resistência a medicamentos e parasitas que driblam os diagnósticos quase em tempo real. Embora outros métodos continuem mais indicados para algumas tarefas especializadas, essa abordagem se ajusta bem à necessidade urgente de informações rápidas e práticas para orientar escolhas de testes e políticas de tratamento em toda a África Subsaariana.
Citação: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Palavras-chave: malária, vigilância genômica, resistência a medicamentos, sequenciamento por nanopore, África Subsaariana