Clear Sky Science · de
Genomische Überwachung von Plasmodium falciparum über Kontinente hinweg in Subsahara-Afrika mittels schneller Nanopore-Sequenzierung
Warum Malariagene für den Alltag wichtig sind
Malaria tötet in Subsahara-Afrika weiterhin Hunderttausende Menschen pro Jahr, und der Parasit lernt ständig neue Wege, unseren Tests und Medikamenten zu entgehen. Diese Studie zeigt, wie Wissenschaftler und lokale Gesundheitsteams den genetischen Code des Parasiten schnell in normalen afrikanischen Laboren lesen können, sodass Länder nahezu in Echtzeit erkennen, wo Malaria schwerer zu diagnostizieren und zu behandeln wird.
Zunehmende Probleme für Tests und Behandlungen
Der tödlichste Malariaparasit, Plasmodium falciparum, wehrt sich gegen zwei unserer Hauptwerkzeuge. Einige Stämme haben die Gene hrp2 und hrp3 verloren, wodurch Standard-Schnelltests Infektionen übersehen können. Andere tragen Veränderungen in einem Gen namens kelch13, die mit einer verlangsamten Parasitenelimination nach Behandlung mit den derzeitigen Erstlinienmedikamenten verbunden sind. Diese besorgniserregenden Varianten breiten sich in Ost-, Zentral- und Südafrika aus. Gesundheitsbehörden erwägen, Testtypen zu wechseln oder Wirkstoffkombinationen zu rotieren, benötigen dafür jedoch detaillierte und aktuelle Informationen darüber, welche Parasitenstämme wo zirkulieren.
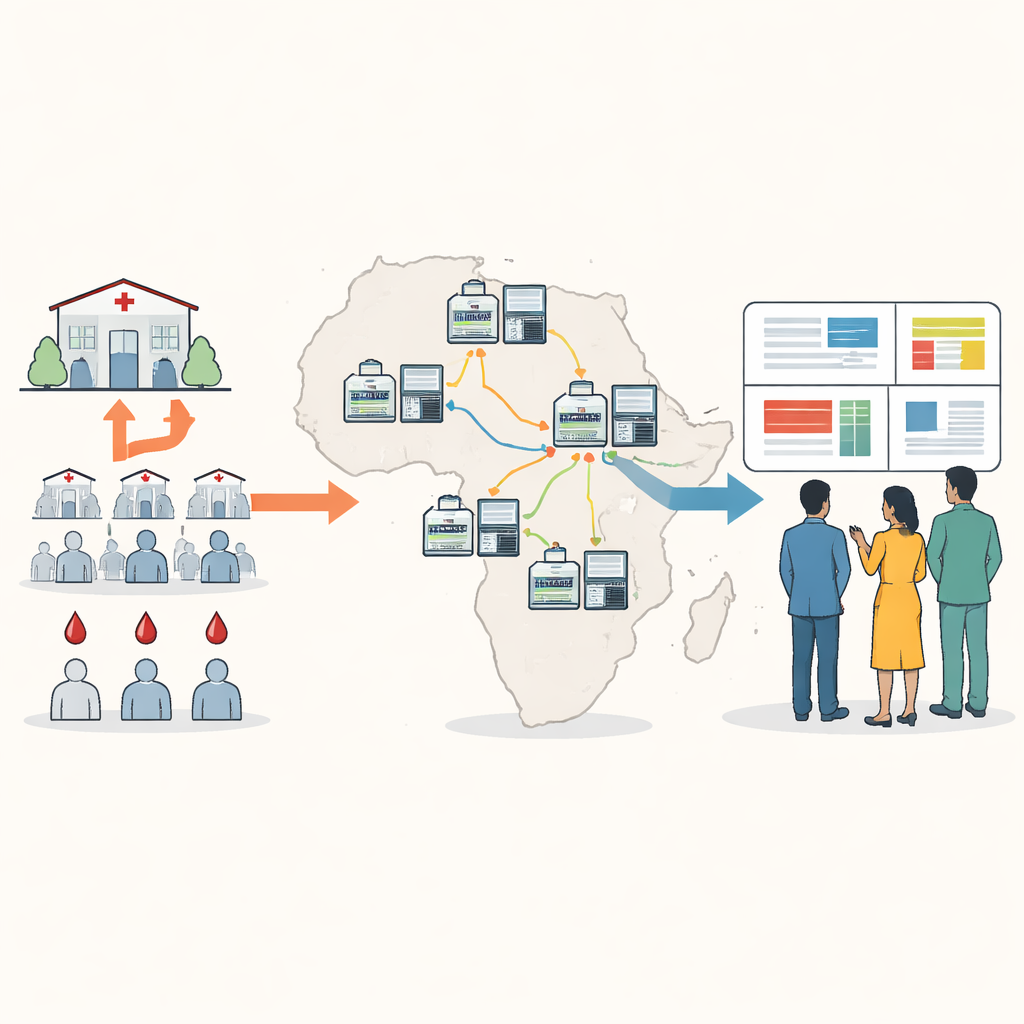
Genetisches Monitoring näher an die Patienten bringen
Die herkömmliche DNA-Sequenzierung von Malariaproben erfordert oft, dass Blutproben ins Ausland oder an wenige große regionale Zentren geschickt werden, was langsam, teuer und von lokalen Entscheidungsprozessen getrennt sein kann. Die Autoren entwickelten einen neuen Ansatz rund um ein kleines tragbares Gerät, bekannt als Nanopore-Sequenzer. Mit getrockneten Blutstropfen aus routinemäßigen Malariatests können lokale Mitarbeiter Schlüsselparasiten-Gene in etwa fünf Stunden vervielfältigen und sequenzieren, zu Kosten von unter 25 US-Dollar pro Probe. Das neue ‚Minimal Viable Panel‘ konzentriert sich auf zehn genetische Regionen, die Arzneimittelresistenz, das Vorhandensein oder Fehlen von hrp2 und hrp3, impfrelevante Veränderungen und die Anzahl verschiedener Parasitenstämme in einer einzelnen Infektion aufdecken.
Einfach nutzbare Software auf einem gewöhnlichen Laptop
Um die Methode an Orte mit begrenztem Internet und Rechenressourcen anzupassen, entwickelte das Team ein Softwarepaket namens Nomadic. Es läuft auf demselben Laptop, der auch den Sequenzer steuert, und arbeitet vollständig offline. Während der Sequenzierung ordnet das Programm jeden Leseabschnitt dem Parasiten-Genom zu, prüft die Qualität und markiert wichtige Mutationen, während es zugleich intuitive Diagramme in einem lokalen Dashboard anzeigt. Die Software erzeugt außerdem kompakte Zusammenfassungsdateien, die sich leicht per E-Mail oder über langsame Verbindungen teilen lassen, sodass Partner Ergebnisse vieler Standorte kombinieren können, ohne große Rohdatendateien zu verschieben.
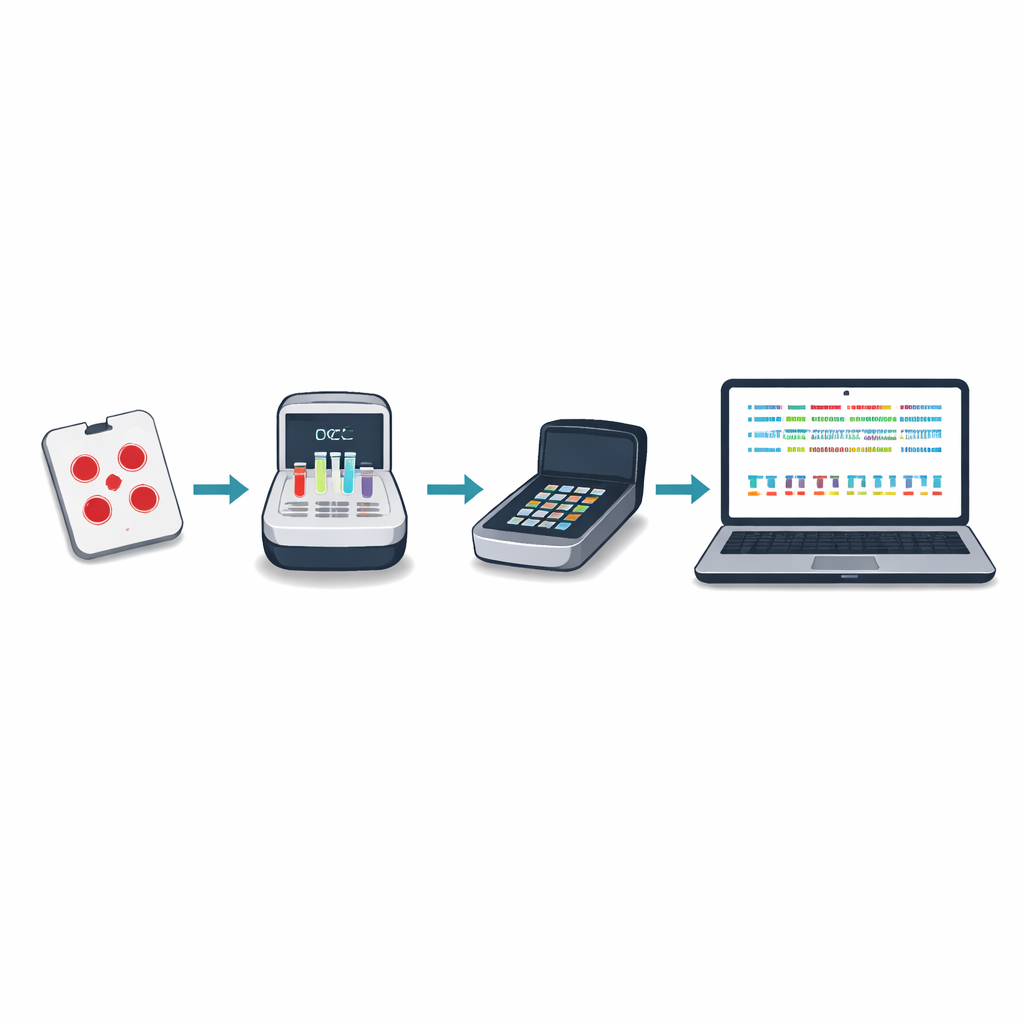
Systemtests in ganz Afrika
Zwischen 2024 und 2025 nutzten Labore in sechs afrikanischen Ländern das Protokoll, um über tausend Malariaproben zu sequenzieren und zu analysieren, die meisten lokal verarbeitet von 13 Wissenschaftlern mit unterschiedlicher Vorerfahrung. Die Methode lieferte eine starke und konsistente Abdeckung der Zielgene über ein breites Spektrum an Parasitenkonzentrationen im Blut. Ein neues Werkzeug zur Variantenbestimmung, Delve genannt, konnte genetische Veränderungen zuverlässig erkennen, die von Minoritätsparasiten getragen wurden und nur fünf bis zehn Prozent einer Infektion ausmachten — ein Bereich, den Standardwerkzeuge oft übersehen. Dieselben Sequenzierläufe identifizierten zudem nahezu alle Deletionen in den Genes hrp2 und hrp3 im Vergleich zu konventionellen Laborverfahren und erkannten in einigen Mischinfektionen Deletionen, die Standardtests übersehen hatten.
Was das für den Kampf gegen Malaria bedeutet
Diese Arbeit zeigt, dass hochwertige genetische Überwachung von Malaria nicht auf entfernte Hightech-Zentren beschränkt sein muss. Durch die Kombination eines erschwinglichen, schlanken Laborprotokolls mit laptopbasierter Analyse können normale öffentliche Gesundheitslabore Resistenzmarker und diagnostisch versteckte Parasiten nahezu in Echtzeit verfolgen. Während andere Methoden für manche Spezialaufgaben weiterhin besser geeignet bleiben, ist dieser Ansatz gut auf den dringenden Bedarf an schnellen, praktischen Informationen abgestimmt, die Testauswahl und Behandlungspolitik in Subsahara-Afrika leiten können.
Zitation: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Schlüsselwörter: Malaria, genomische Überwachung, Arzneimittelresistenz, Nanopore-Sequenzierung, Subsahara-Afrika