Clear Sky Science · it
Sorveglianza genomica su scala continentale di Plasmodium falciparum in tutta l’Africa subsahariana con sequenziamento rapido nanopore
Perché i geni della malaria contano nella vita di tutti i giorni
La malaria continua a uccidere centinaia di migliaia di persone ogni anno nell’Africa subsahariana, e il parassita impara nuovi stratagemmi per sfuggire ai nostri test e ai nostri farmaci. Questo studio mostra come scienziati e squadre sanitarie locali possano leggere rapidamente il codice genetico del parassita in normali laboratori africani, permettendo ai Paesi di vedere in quasi tempo reale dove la malaria diventa più difficile da diagnosticare e trattare.
Problemi crescenti per test e trattamenti
Il parassita più letale, Plasmodium falciparum, sta opponendo resistenza a due dei nostri strumenti principali. Alcuni ceppi hanno perso geni chiamati hrp2 e hrp3, il che significa che i test rapidi standard possono non rilevare le infezioni. Altri presentano variazioni in un gene noto come kelch13, collegate a una più lenta eliminazione del parassita dopo il trattamento con i farmaci di prima linea attuali. Queste varianti preoccupanti si stanno diffondendo nell’Africa orientale, centrale e meridionale. Le agenzie sanitarie stanno valutando la sostituzione dei tipi di test o la rotazione di combinazioni di farmaci, ma hanno bisogno di informazioni dettagliate e tempestive su quali ceppi del parassita circolano e dove.
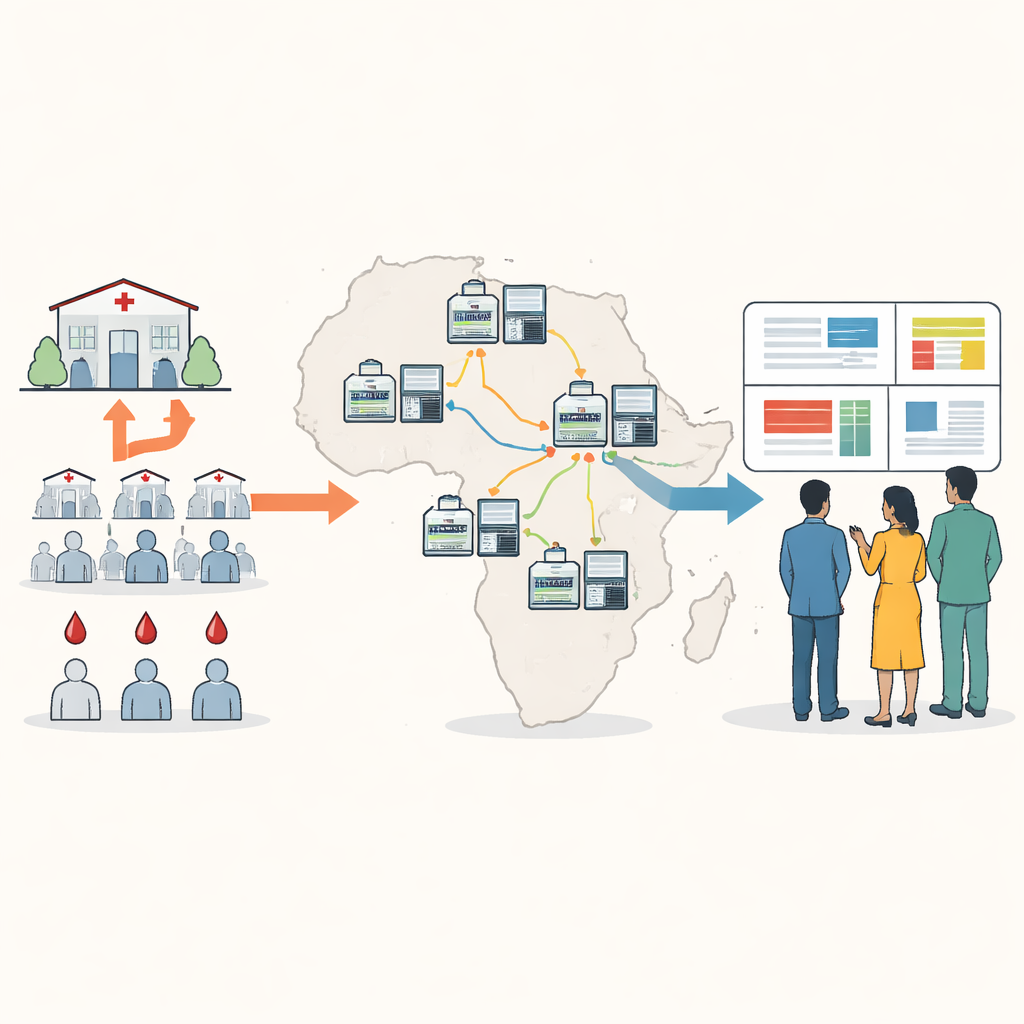
Avvicinare il tracciamento genetico ai pazienti
Il sequenziamento del DNA tradizionale per la malaria spesso richiede l’invio di campioni di sangue all’estero o a pochi grandi centri regionali, operazione che può essere lenta, costosa e scollegata dalle decisioni locali. Gli autori hanno progettato un nuovo approccio basato su un piccolo dispositivo portatile noto come sequenziatore nanopore. Utilizzando spot di sangue essiccato prelevati dai test di routine, il personale locale può amplificare e sequenziare geni chiave del parassita in circa cinque ore, a un costo inferiore a venticinque dollari per campione. Il nuovo “pannello minimo vitale” si concentra su dieci regioni genetiche che rivelano la resistenza ai farmaci, la presenza o assenza di hrp2 e hrp3, cambiamenti rilevanti per i vaccini e il numero di ceppi parassitari diversi miscelati in una singola infezione.
Software semplice su un portatile comune
Per rendere il metodo utilizzabile in luoghi con internet e potenza di calcolo limitati, il team ha creato un pacchetto software chiamato Nomadic. Funziona sullo stesso portatile che controlla il sequenziatore e opera completamente offline. Durante il sequenziamento, il programma mappa ogni lettura sul genoma del parassita, verifica la qualità e segnala le mutazioni importanti, il tutto visualizzando grafici intuitivi in una dashboard locale. Il software produce anche file di sintesi compatti facili da condividere via email o su connessioni lente, permettendo ai partner di combinare i risultati di molti siti senza trasferire grandi file di dati grezzi.
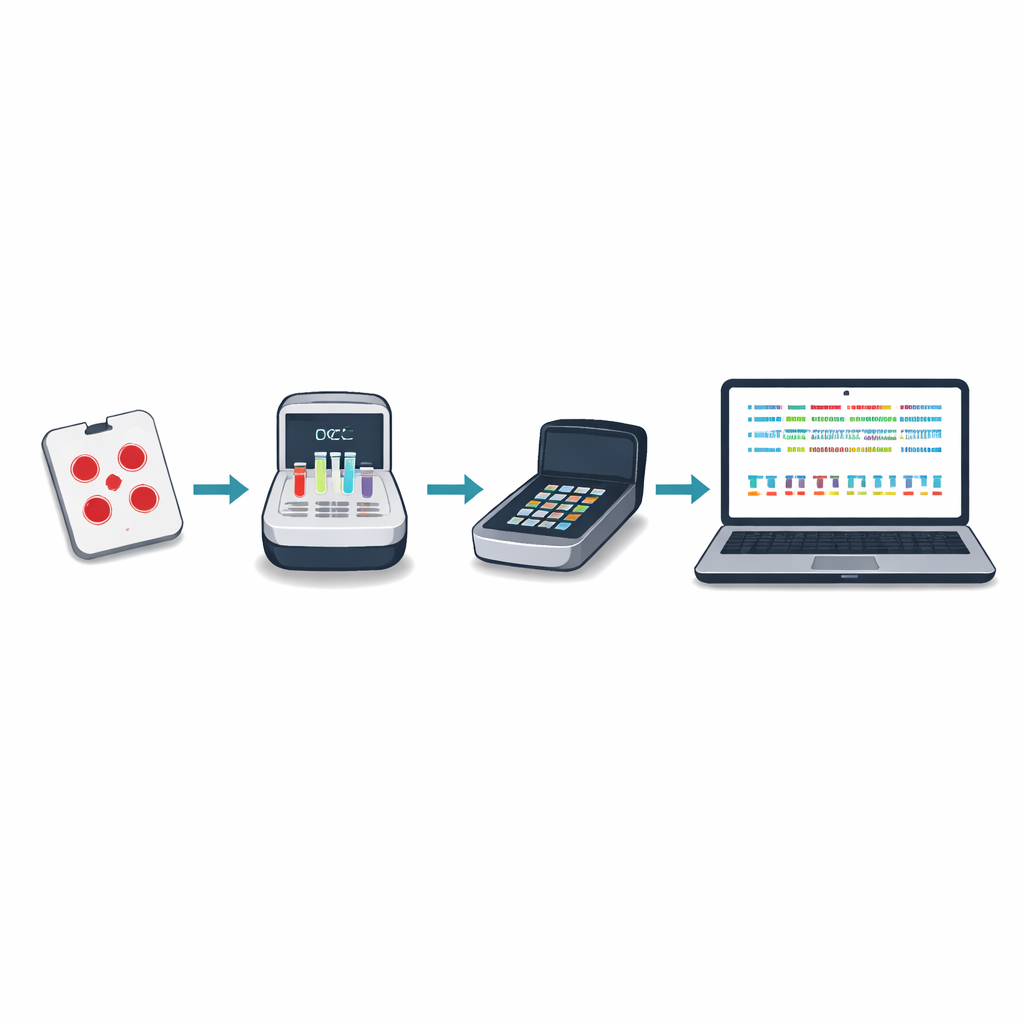
Testare il sistema in tutta l’Africa
Tra il 2024 e il 2025, laboratori in sei Paesi africani hanno usato il protocollo per sequenziare e analizzare oltre mille campioni di malaria, la maggior parte processata localmente da 13 scienziati con diversi livelli di esperienza pregressa. Il metodo ha fornito una copertura solida e consistente dei geni target su un’ampia gamma di livelli di parassiti nel sangue. Un nuovo strumento di chiamata delle varianti, chiamato Delve, è stato in grado di rilevare in modo affidabile cambiamenti genetici presenti in ceppi parassitari minoritari che costituivano solo il cinque-dieci percento di un’infezione, una soglia che gli strumenti standard spesso perdono. Le stesse run di sequenziamento hanno inoltre identificato correttamente quasi tutte le delezioni nei geni hrp2 e hrp3 rispetto ai metodi di laboratorio convenzionali e, in alcune infezioni miste, hanno rilevato delezioni che i test standard avevano trascurato.
Cosa significa per la lotta contro la malaria
Questo lavoro dimostra che una sorveglianza genetica di alta qualità della malaria non deve essere confinata a centri high-tech lontani. Abbinando un protocollo di laboratorio economico e snello all’analisi su portatile, i laboratori di sanità pubblica ordinari possono monitorare marcatori di resistenza ai farmaci e parassiti che sfuggono alla diagnostica in tempi quasi reali. Pur rimanendo altri metodi più adatti per alcuni compiti specialistici, questo approccio è ben calibrato sull’esigenza urgente di informazioni rapide e pratiche per guidare le scelte dei test e le politiche di trattamento in tutta l’Africa subsahariana.
Citazione: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Parole chiave: malaria, sorveglianza genomica, resistenza ai farmaci, sequienziamento nanopore, Africa subsahariana