Clear Sky Science · pl
Genomiczne monitorowanie Plasmodium falciparum w skali kontynentu w Afryce Subsaharyjskiej za pomocą szybkiego sekwencjonowania nanoporowego
Dlaczego geny malarii mają znaczenie w codziennym życiu
Malaria wciąż zabija setki tysięcy osób rocznie w Afryce Subsaharyjskiej, a pasożyt uczy się nowych sposobów, by unikać naszych testów i leków. Badanie pokazuje, jak naukowcy i lokalne zespoły zdrowia publicznego mogą szybko odczytywać kod genetyczny pasożyta w zwykłych afrykańskich laboratoriach, dzięki czemu kraje mogą niemal w czasie rzeczywistym zobaczyć, gdzie malaria staje się trudniejsza do wykrycia i leczenia.
Rosnące problemy z testami i leczeniem
Najbardziej śmiertelny gatunek pasożyta, Plasmodium falciparum, stawia opór dwóm naszym głównym narzędziom. Niektóre szczepy utraciły geny nazywane hrp2 i hrp3, co sprawia, że standardowe szybkie testy mogą nie wykryć zakażeń. Inne niosą zmiany w genie znanym jako kelch13, które wiążą się ze spowolnionym usuwaniem pasożytów po leczeniu obecnymi lekami pierwszego rzutu. Te niepokojące warianty rozprzestrzeniają się po wschodniej, środkowej i południowej Afryce. Agencje zdrowia rozważają zmianę rodzaju testów lub rotację kombinacji leków, ale potrzebują szczegółowych i aktualnych informacji o tym, które szczepy pasożyta krążą w poszczególnych regionach.
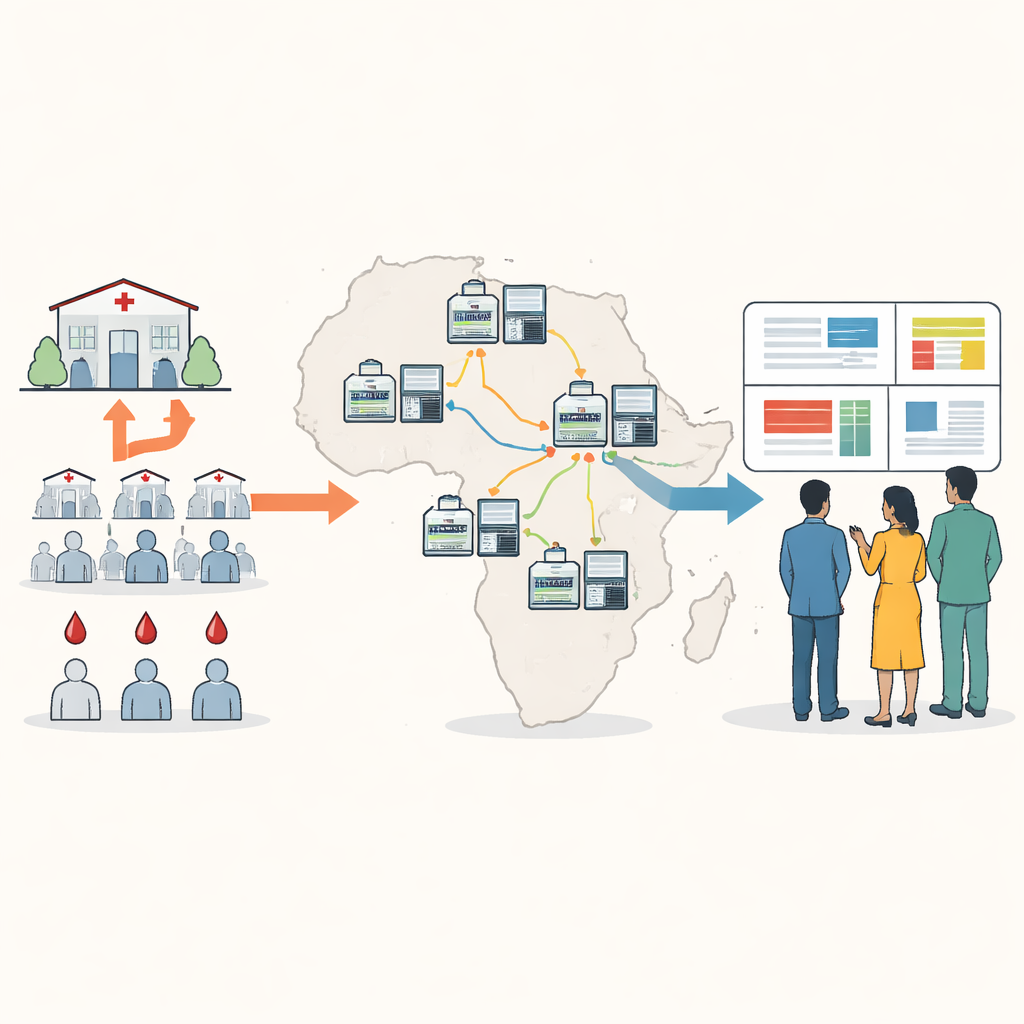
Przybliżenie śledzenia genetycznego do pacjentów
Tradycyjne sekwencjonowanie DNA dla malarii często wymaga wysyłania próbek krwi za granicę lub do kilku dużych regionalnych ośrodków, co może być wolne, kosztowne i odłączać wyniki od lokalnego podejmowania decyzji. Autorzy opracowali nowe podejście oparte na małym przenośnym urządzeniu zwanym sekwencerem nanoporowym. Korzystając z wysuszonych plamek krwi pobranych podczas rutynowych badań na malarię, lokalny personel może namnożyć i zsekwencjonować kluczowe geny pasożyta w około pięć godzin, przy koszcie poniżej dwudziestu pięciu dolarów za próbkę. Nowy „minimalny panel funkcjonalny” koncentruje się na dziesięciu regionach genetycznych, które ujawniają oporność na leki, obecność lub brak hrp2 i hrp3, zmiany istotne dla szczepionek oraz liczbę różnych szczepów pasożyta zmieszanych w jednym zakażeniu.
Proste oprogramowanie na zwykły laptop
Aby metoda była użyteczna w miejscach o ograniczonym internecie i mocy obliczeniowej, zespół stworzył pakiet oprogramowania nazwany Nomadic. Działa na tym samym laptopie, który steruje sekwencerem, i pracuje całkowicie offline. W miarę postępu sekwencjonowania program mapuje każde odczytanie do genomu pasożyta, sprawdza jakość i oznacza ważne mutacje, jednocześnie wyświetlając intuicyjne wykresy w lokalnym panelu sterowania. Oprogramowanie generuje też zwarte pliki podsumowujące, które łatwo wysłać mailem lub przez wolne łącza, umożliwiając partnerom łączenie wyników z wielu miejsc bez przesyłania dużych surowych plików danych.
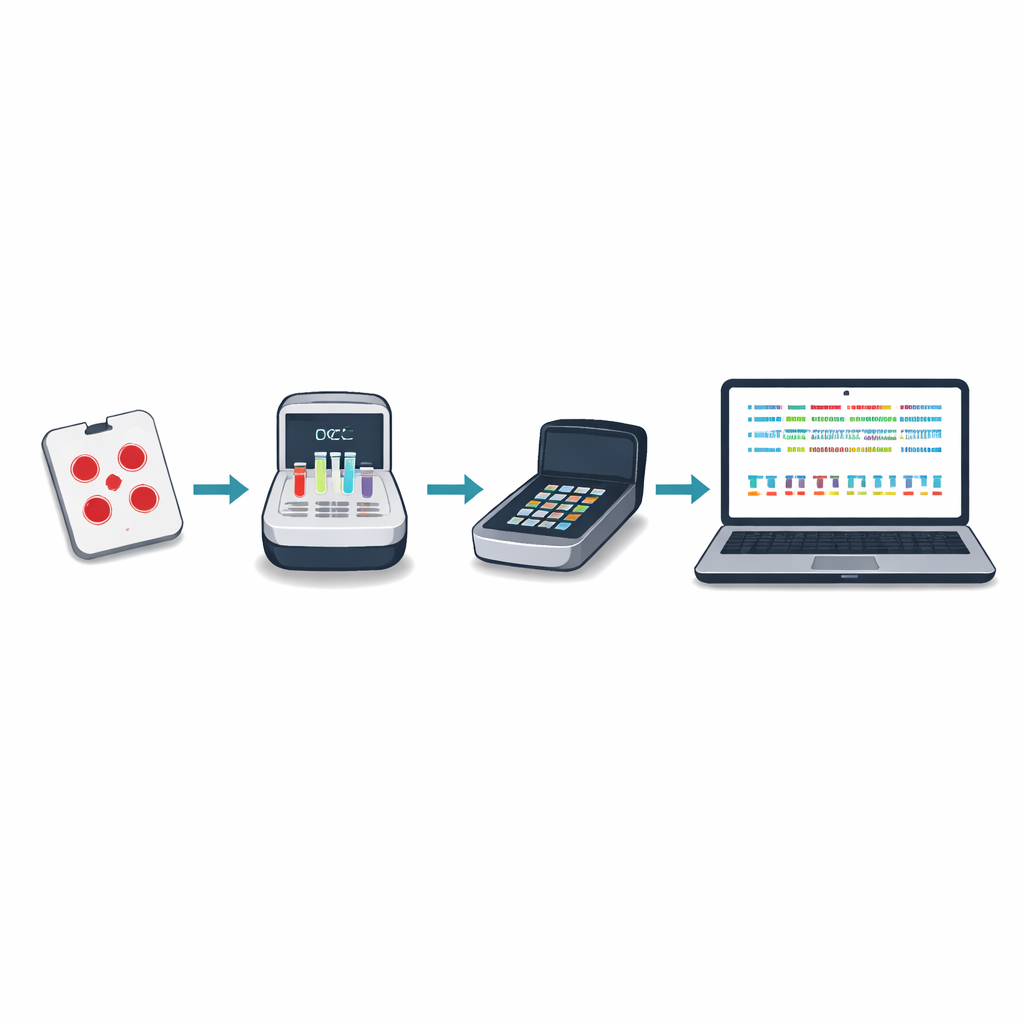
Testowanie systemu w całej Afryce
W latach 2024–2025 laboratoria w sześciu krajach afrykańskich zastosowały protokół do sekwencjonowania i analizy ponad tysiąca próbek malarii, z których większość przetworzono lokalnie przez 13 naukowców o różnym wcześniejszym doświadczeniu. Metoda zapewniła silne i spójne pokrycie docelowych genów w szerokim zakresie poziomów pasożytów we krwi. Nowe narzędzie do wykrywania wariantów, nazwane Delve, mogło niezawodnie wykrywać zmiany genetyczne niosące przez mniejsze szczepy pasożyta stanowiące zaledwie pięć do dziesięciu procent zakażenia — poziom, który standardowe narzędzia często pomijają. Te same serie sekwencjonowania również poprawnie identyfikowały prawie wszystkie delecje w genach hrp2 i hrp3 w porównaniu z konwencjonalnymi metodami laboratoryjnymi, a w niektórych mieszanych zakażeniach wykrywały delecje, które testy standardowe przeoczyły.
Co to oznacza w walce z malarią
Ta praca pokazuje, że wysokiej jakości monitoring genetyczny malarii nie musi być ograniczony do odległych ośrodków wysokich technologii. Łącząc niedrogi, uproszczony protokół laboratoryjny z analizą na laptopie, zwykłe laboratoria zdrowia publicznego mogą śledzić markery oporności na leki i pasożyty unikające diagnostyki niemal w czasie rzeczywistym. Choć inne metody nadal lepiej nadają się do niektórych zadań specjalistycznych, podejście to dobrze odpowiada pilnej potrzebie szybkich, praktycznych informacji do kierowania wyborem testów i polityką leczenia w Afryce Subsaharyjskiej.
Cytowanie: Mwenda, M., Mosler, K., Bohmeier, B. et al. Continental-scale genomic surveillance of Plasmodium falciparum malaria across sub-Saharan Africa with rapid nanopore sequencing. Nat Commun 17, 4218 (2026). https://doi.org/10.1038/s41467-026-72358-z
Słowa kluczowe: malaria, monitoring genomowy, oporność na leki, sekwencjonowanie nanoporowe, Afryka Subsaharyjska