Clear Sky Science · sv
Ikke-nekroptotisk MLKL-funktion skadar mitokondrier och främjar åldrande hos hematopoetiska stamceller
Varför vårt livslånga blodfabrik slits ut
Långt inne i våra ben bygger en liten pool av stamceller tyst varje blod- och immuncell vi behöver under hela livet. Med åren sviktar denna fabrik: infektioner blir långdragna, anemi blir vanligare och blodcancer som myelodysplastiska syndrom förekommer oftare. Denna studie avslöjar en dold molekylär syndabock — ett oväntat beteende hos ett protein kallat MLKL — som långsamt skadar stamcellernas kraftverk och bidrar till åldrandet av vårt blodsystem.
Stressignaler som inte riktigt dödar
Hematopoetiska stamceller, de sällsynta ”mästar”-cellerna i benmärgen, är ovanligt motståndskraftiga mot celldöd, även när de bombarderas av inflammation eller kemoterapi. Författarna fokuserade på en molekylär väg som normalt används för att utlösa en dramatisk form av celldöd kallad nekroptos, driven av två proteiner, RIPK3 och MLKL. Med hjälp av genmodifierade möss som bär en fluorescerande sensor som lyser upp när MLKL aktiveras fann de att en rad vanliga stressorer — inflammatoriska molekyler som imiterar virusinfektion, bakteriella komponenter och ett kemoterapimedel som tvingar stamceller till delning — konsekvent aktiverade MLKL i stamceller och deras närmaste progenitorer, men inte i mer mogna blodförstadier. Överraskande nog, trots denna aktivering, dog inte stamcellerna i stora antal. Istället visade de med starkt aktivt MLKL sämre förmåga att engrafta och bilda lymfoida celler vid transplantation till nya möss, vilket antyder att MLKL tyst skadade funktion snarare än utlöste omedelbar celldöd.
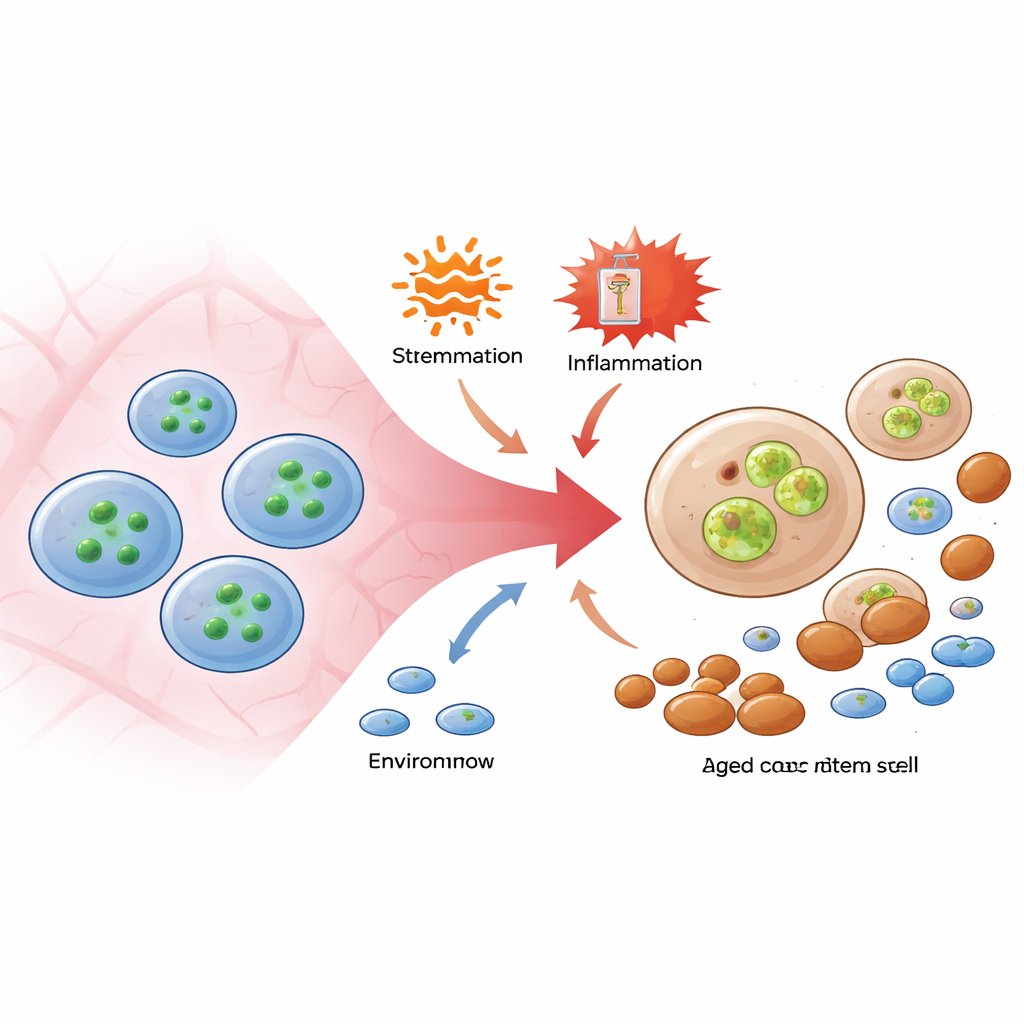
En skadeväg dold inuti överlevande celler
För att skilja död från dysfunktion använde forskarna möss som saknade MLKL, eller som bar en version av proteinet som inte kan aktiveras av RIPK3. När dessa djur utsattes för inflammatoriska stimuli eller upprepad kemoterapi överlevde deras stamceller ungefär lika väl som hos normala möss, och det totala antalet stamceller i benmärgen förblev likartat. Men de vanliga åldersliknande förändringarna — en expansion av stamceller som tenderar att producera myeloida celler och förlust av balanserade stamceller som kan göra både lymfoida och myeloida linjer — var tydligt dämpade när MLKL-aktiviteten togs bort. Ännu mer slående var att när MLKL-defekta stamceller utsattes för en onkogen stress som normalt modellerar pre-leukemisk sjukdom skyddades djuren från svår benmärgsinsufficiens. Dessa experiment visade att MLKL kan undergräva stamcellskvalitet inifrån, även när det hindras från att genomföra sitt klassiska program för celldöd.
Från slitage till verkligt åldrande
Teamet frågade sig sedan om denna icke-dödliga MLKL-aktivitet kan förklara normalt åldrande. Hos äldre möss lyste MLKL-sensorn starkare i stamcellerna, vilket visar att denna väg kroniskt engageras med åldern. Att ta bort MLKL stoppade inte att stamceller ackumulerades över tid, men det minskade klassiska kännetecken för åldrande: blodproduktionen blev mindre snedvriden mot myeloida celler, tidiga lymfoida progenitorer bevarades bättre och markörer för DNA-skada i stamcellerna var reducerade. Transplantationstester bekräftade att åldrande stamceller utan MLKL behöll starkare regenerativ kraft och en mer balanserad produktion av T- och B-lymfocyter. Viktigt är att den omgivande benmärgsmiljön hos åldrade möss visade liknande nivåer av inflammatoriska molekyler oavsett om MLKL fanns eller inte, och breda undersökningar av genaktivitet och kromatinstruktur i stamceller visade liten skillnad mellan normala gamla celler och de som saknade MLKL. Det tyder på att MLKL främst verkar genom en fysisk, snarare än genetisk, skademekanism.
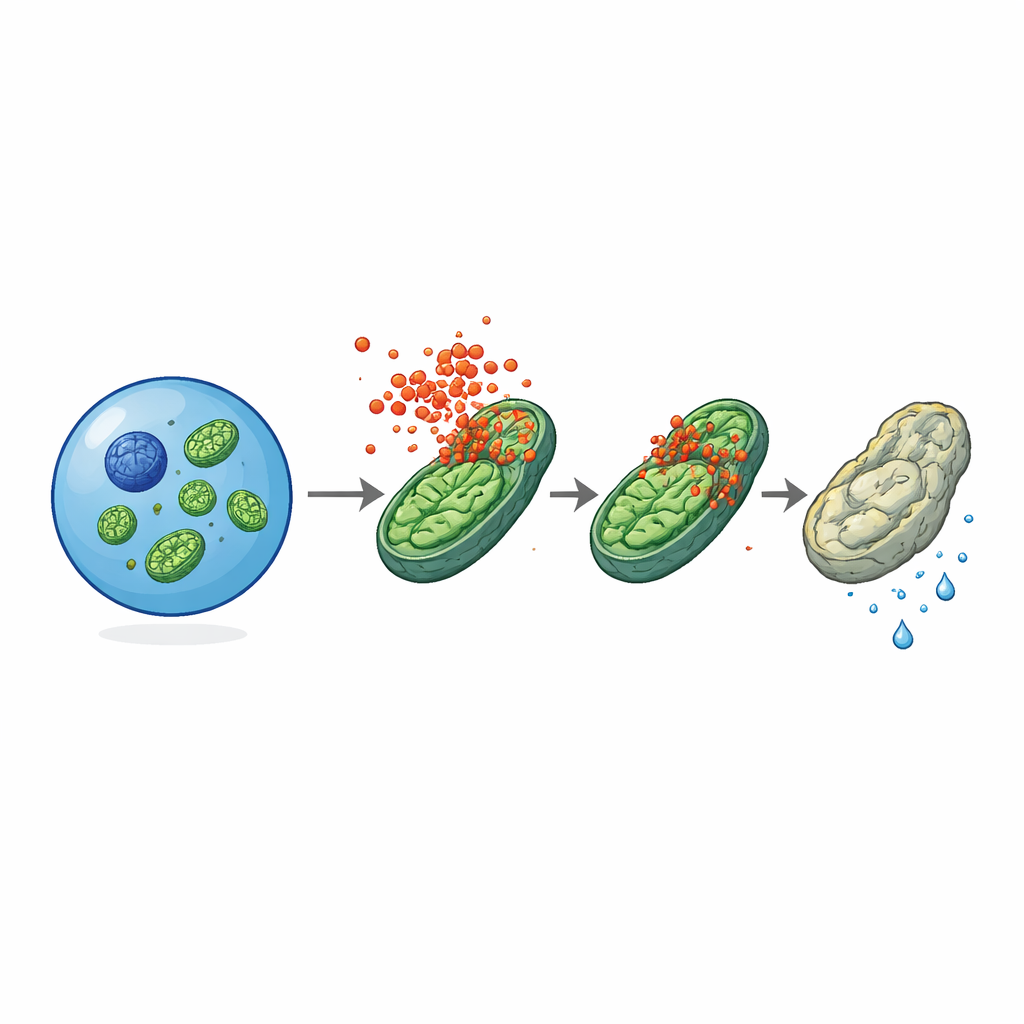
Kraftverk under attack
Elektronmikroskopi gav en avgörande ledtråd: mitokondrierna — de små organellerna som genererar energi — såg svullna och missformade ut i gamla stamceller från normala möss, men framstod som mycket friskare i åldersmatchade celler som saknade MLKL. Den aktiva, fosforylerade formen av MLKL hittades hopklustrad på mitokondriella membran, särskilt i åldrande eller inflammerade stamceller. Funktionella tester visade att gamla stamceller utan MLKL hade bättre mitokondriell membranpotential, producerade mer ATP och upprätthöll högre glykolytisk aktivitet än sina normala motsvarigheter, vilket tyder på att MLKL gradvis flyttar deras metabolism från ett ungdomligt, glykolyspräglat tillstånd mot ett mer stressat, syrekrävande läge. I isolerade mitokondrier exponerade för renade MLKL-fragment minskade proteinet direkt membranpotentialen, vilket indikerar att det kan störa eller destabiliserar mitokondriella membran även utanför hela den cellulära kontexten.
Vad detta betyder för hälsosamt åldrande
Sammantaget avslöjar arbetet att MLKL, länge känt som en avrättare i katastrofal celldöd, också fungerar som en långsam sabotör av stamcellernas mitokondrier. Upprepade episoder av inflammation, replikeringsstress och onkogena påfrestningar verkar konvergera på denna väg, vilket tillåter stamceller att överleva omedelbara kriser men till priset av ackumulerad skada som dämpar deras regenerativa kapacitet och förskjuter blodproduktionen mot mer riskfyllda mönster. Medan MLKL och dess partners kan vara fördelaktiga för att bekämpa infektioner och begränsa cancer i vissa sammanhang, kan en noggrann finjustering av denna väg — eller att skydda mitokondrierna från dess icke-dödliga angrepp — en dag hjälpa till att bevara ett yngre, mer motståndskraftigt blodsysten när vi åldras.
Citering: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Nyckelord: åldrande hos hematopoetiska stamceller, mitokondriell dysfunktion, MLKL, inflammation och kemoterapistress, metabolism hos blodstamceller