Clear Sky Science · ar
وظيفة MLKL غير النخرية تضر بالميتوكوندريا وتعزز شيخوخة الخلايا الجذعية الدموية
لماذا يتعب مصنع دمنا مدى الحياة
في أعماق عظامنا، تجمع صغير من الخلايا الجذعية يبني بهدوء كل خلية دموية ومناعية نحتاجها طوال الحياة. مع التقدّم في العمر، يضعف هذا المصنع: تطيل العدوى، وتصبح فقرات الدم أكثر شيوعًا، وتزداد حالات سرطانات الدم مثل متلازمات خلل التنسج النقوي. تكشف هذه الدراسة عن مشتبه جزيئي مخفي — سلوك غير متوقع لبروتين يُدعى MLKL — الذي يسبب إصابة تدريجية لمصانع الطاقة في الخلايا الجذعية ويساهم في تسريع شيخوخة جهاز الدم.
إشارات ضغط لا تقتل تمامًا
الخلايا الجذعية الدموية، وهي الخلايا «السيدة» النادرة في نخاع العظم، مقاومة بشكل غير عادي للموت حتى عند تعرضها للالتهاب أو العلاج الكيميائي. ركز الباحثون على مسار جزيئي يُستخدم عادة لتحفيز شكل درامي من موت الخلايا يسمى النخر المبرمج (necroptosis)، الذي تقوده بروتينات اثنتان، RIPK3 وMLKL. باستخدام فئران مهندَسة تحمل حساسًا فلوريًا يضيء عند تنشيط MLKL، وجدوا أن مجموعة من الضغوط الشائعة — جزيئات التهابية تُحاكي العدوى الفيروسية، مكونات بكتيرية، ودواء كيميائي يَجبر الخلايا الجذعية على الانقسام — تُشغّل MLKL باستمرار في الخلايا الجذعية وأقرب أسلافها، لكن ليس في الخلايا الدموية الأكثر نضجًا. والمفاجئ أنه بالرغم من هذا التنشيط، لم تمُت الخلايا الجذعية بأعداد كبيرة. بدلاً من ذلك، أظهرت الخلايا ذات نشاط MLKL العالي قدرة أدنى على الاستقرار وإنتاج الخلايا اللمفاوية عند زراعتها في فئران جديدة، مما يلمّح إلى أن MLKL يسبب تلفًا وظيفيًا هادئًا بدلاً من إثارة موت صريح.
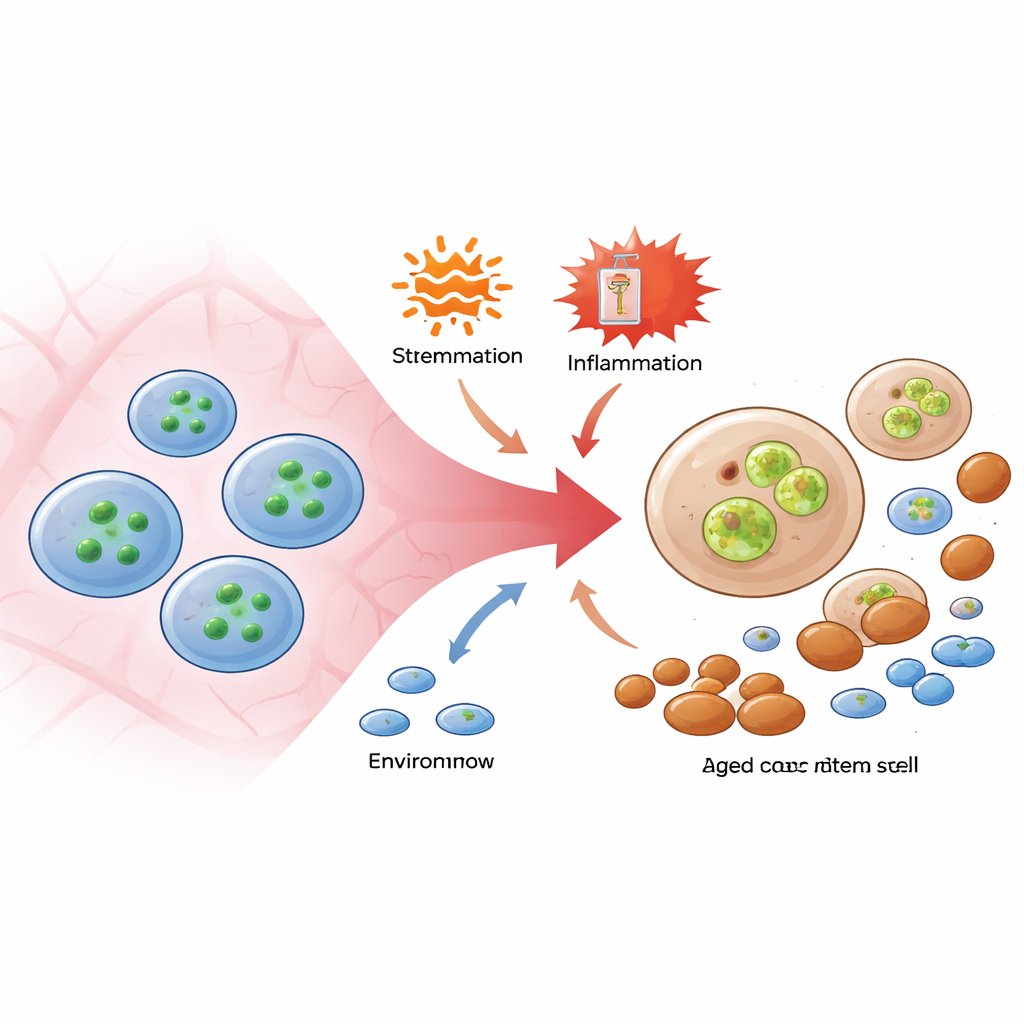
مسار تلف مخفي داخل الخلايا الناجية
لفصل الموت عن الخلل الوظيفي، استخدم الباحثون فئرانًا تفتقر إلى MLKL، أو تحمل نسخة من البروتين لا يمكن تفعيلها بواسطة RIPK3. عندما تعرّضت هذه الحيوانات لمحفزات التهابية أو لعلاجات كيميائية متكررة، نَجَت خلاياها الجذعية بمعدل مشابه لتلك في الفئران الطبيعية، وظل العدد الكلي للخلايا الجذعية في نخاع العظم متقاربًا. ومع ذلك، كانت التحولات المرتبطة بالعمر — توسع الخلايا الجذعية الميّالة نحو إنتاج الخلايا النخاعية وفقدان التوازن في الخلايا القادرة على إنتاج الخطين اللمفاوي والنخاعي — مخففة بشكل ملحوظ عند غياب نشاط MLKL. والأكثر بروزًا، حين أُجبرت خلايا جذعية محرومة من MLKL على مواجهة إجهاد مُسرطن يُحاكي مرضًا قبل اللوكيميا، حُميت الحيوانات من فشل نخاع عظمي شديد. أظهرت هذه التجارب أن MLKL يمكن أن يقوّض جودة الخلايا الجذعية من الداخل، حتى عندما يُمنَع عن تنفيذ برنامجه الكلاسيكي لموت الخلايا.
من التآكل إلى الشيخوخة الحقيقية
ثم سأل الفريق ما إذا كان هذا النشاط غير القاتل لـMLKL يفسّر الشيخوخة الطبيعية. في فئران أكبر سنًا، أضاء حساس MLKL بقوة أكبر في الخلايا الجذعية، كاشفًا أن هذا المسار ينخرط بشكل مزمن مع التقدّم في العمر. لم يمنع حذف MLKL تراكم الخلايا الجذعية مع الزمن، لكنه خفف علامات الشيخوخة الكلاسيكية: أصبح إنتاج الدم أقل انحرافًا نحو الخلايا النخاعية، وحُفظت الخلايا النامية اللمفاوية المبكرة بشكل أفضل، وانخفضت علامات تلف الحمض النووي في الخلايا الجذعية. أكدت اختبارات الزرع أن الخلايا الجذعية المسنة الخالية من MLKL حافظت على قدرة تجدد أقوى وإنتاج متوازن أكثر لخلايا T وB اللمفاوية. ومن المهم أن بيئة نخاع العظم المحيطة في الفئران المسنة أظهرت مستويات مشابهة من الجزيئات الالتهابية سواء وُجد MLKL أم لا، وكشوفات واسعة لنشاط الجينات وبنية الكروماتين في الخلايا الجذعية كشفت فروقًا ضئيلة بين الخلايا المسنة الطبيعية وتلك الخالية من MLKL. وهذا يشير إلى أن عمل MLKL يتم بالأساس عبر آلية فيزيائية، وليس جينية، للتسبب في الضرر.
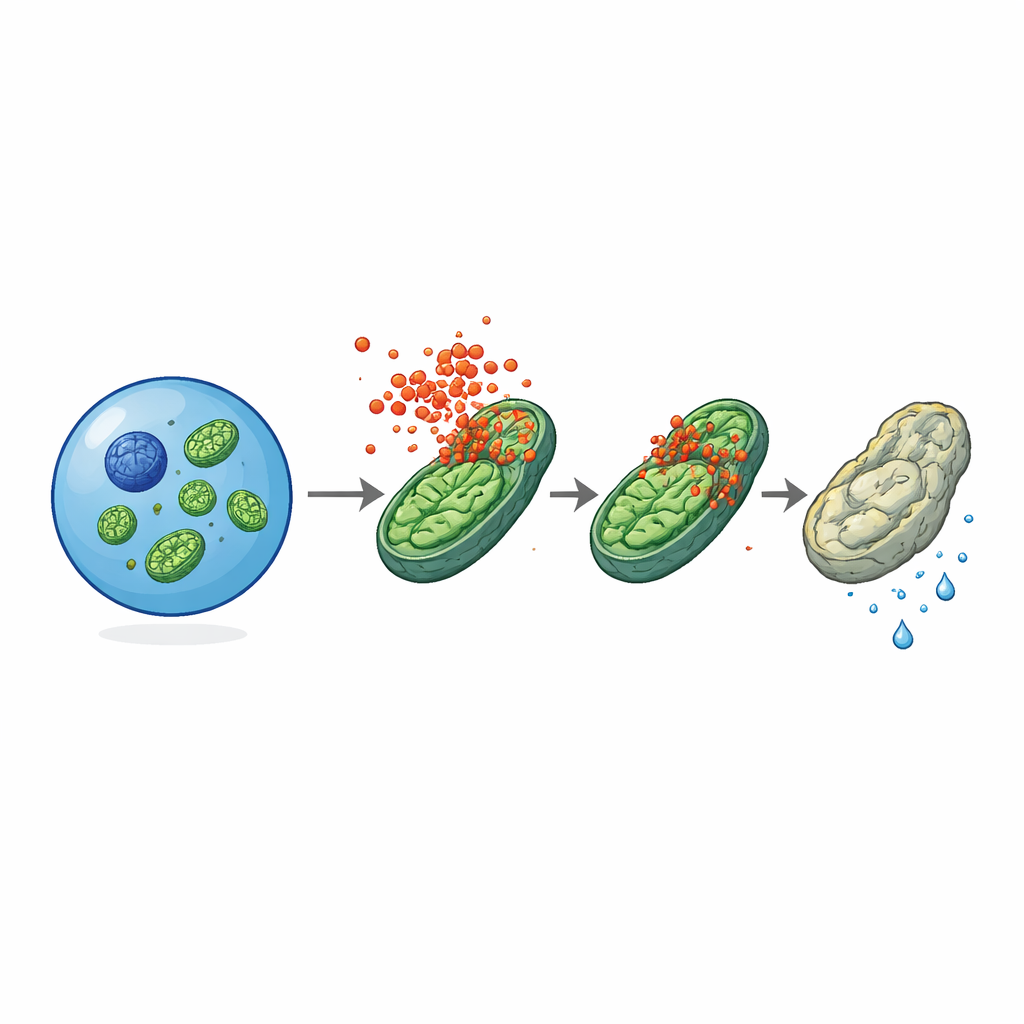
المصانع الطاقية تحت الهجوم
قدّم التصوير الإلكتروني دليلًا حاسمًا: بدت الميتوكوندريا — العضيات الصغيرة المسؤولة عن توليد الطاقة — منتفخة وغير مشكَّلة في الخلايا الجذعية المسنة من الفئران العادية، لكنها بدت أكثر صحة في الخلايا المماثلة الخالية من MLKL. وُجد شكل MLKL النشط والمفروز متجمعًا على أغشية الميتوكوندريا، خاصة في الخلايا الجذعية المسنة أو الملتهبة. أظهرت الاختبارات الوظيفية أن الخلايا الجذعية المسنة التي تفتقر إلى MLKL كان لديها جهد غشاء ميتوكوندري أفضل، وإنتاج أدنى من ATP، ونشاط تحلّل سُكَّري أعلى من نظرائها الطبيعية، مما يوحي بأن MLKL يدفع استقلابها تدريجيًا بعيدًا عن حالة شبابية مَيّالة للاعتماد على التحلّل السكري نحو وضع أكثر إجهادًا واعتمادًا على الأوكسجين. في الميتوكوندريا المعزولة المعرضة لقطع معزولة من MLKL، قلّل البروتين مباشرة من جهد الغشاء، مما يشير إلى أنه يمكنه غرز أو زعزعة استقرار أغشية الميتوكوندريا حتى خارج السياق الخلوي الكامل.
ماذا يعني هذا للشيخوخة الصحية
معًا، تكشف النتائج أن MLKL، المعروف طويلاً كمنفّذ لموت الخلايا الكارثي، يعمل أيضًا كخائن بطيء لمیتوكوندريا الخلايا الجذعية. تبدو نوبات متكررة من الالتهاب، ضغوط الانقسام، والاعتداءات المسرطنة متجمعة على هذا المسار، مما يتيح للخلايا الجذعية البقاء من الأزمات الفورية لكن على حساب تراكم تلف يقلل من قدرتها التجددية ويحوّل إنتاج الدم نحو أنماط أكثر خطورة. وبينما يمكن أن تكون MLKL وشركاؤه مفيدة لمكافحة العدوى وكبح السرطان في سياقات معينة، قد يساعد ضبط هذا المسار بعناية — أو حماية الميتوكوندريا من هجماته غير القاتلة — يومًا ما في الحفاظ على جهاز دم أصغر سنًا وأكثر مرونة مع تقدمنا في العمر.
الاستشهاد: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
الكلمات المفتاحية: شيخوخة الخلايا الجذعية الدموية, خلل وظيفي ميتوكوندري, MLKL, الالتهاب وإجهاد العلاج الكيميائي, استقلاب خلايا جذع الدم