Clear Sky Science · ru
Некрoптоз-независимая функция MLKL повреждает митохондрии и способствует старению гемопоэтических стволовых клеток
Почему фабрика крови изнашивается на всю жизнь
Глубоко внутри наших костей небольшой пул стволовых клеток незаметно производит все клетки крови и иммунной системы, которые нам нужны на протяжении жизни. С возрастом эта фабрика дает сбои: инфекции дольше не проходят, анемия становится более распространенной, и риск развития кровяных злокачественных заболеваний, таких как миелодиспластические синдромы, повышается. Это исследование выявляет скрытого молекулярного виновника — неожиданное поведение белка под названием MLKL — которое постепенно повреждает «энергетические станции» стволовых клеток и способствует старению кроветворной системы.
Сигналы стресса, которые не убивают окончательно
Гемопоэтические стволовые клетки, редкие «главные» клетки в костном мозге, особенно устойчивы к гибели, даже при атаке воспалением или химиотерапией. Авторы сосредоточили внимание на молекулярном пути, обычно задействованном для запуска драматической формы гибели клеток — некроптоза, управляемого двумя белками, RIPK3 и MLKL. Используя генетически модифицированных мышей с флуоресцентным сенсором, который светится при активации MLKL, они обнаружили, что широкий спектр обычных стрессов — провоспалительные молекулы, имитирующие вирусную инфекцию, бактериальные компоненты и химиопрепарат, вынуждающий стволовые клетки делиться — стабильно активировали MLKL в стволовых клетках и их ближайших предшественниках, но не в более зрелых предшественниках крови. Удивительно, что при этой активации стволовые клетки не массово умирали. Вместо этого клетки с высокой активностью MLKL хуже приживались и давали меньше лимфоидных клеток при трансплантации в новых животных, что указывает на то, что MLKL тихо нарушает функцию, не вызывая явной гибели.
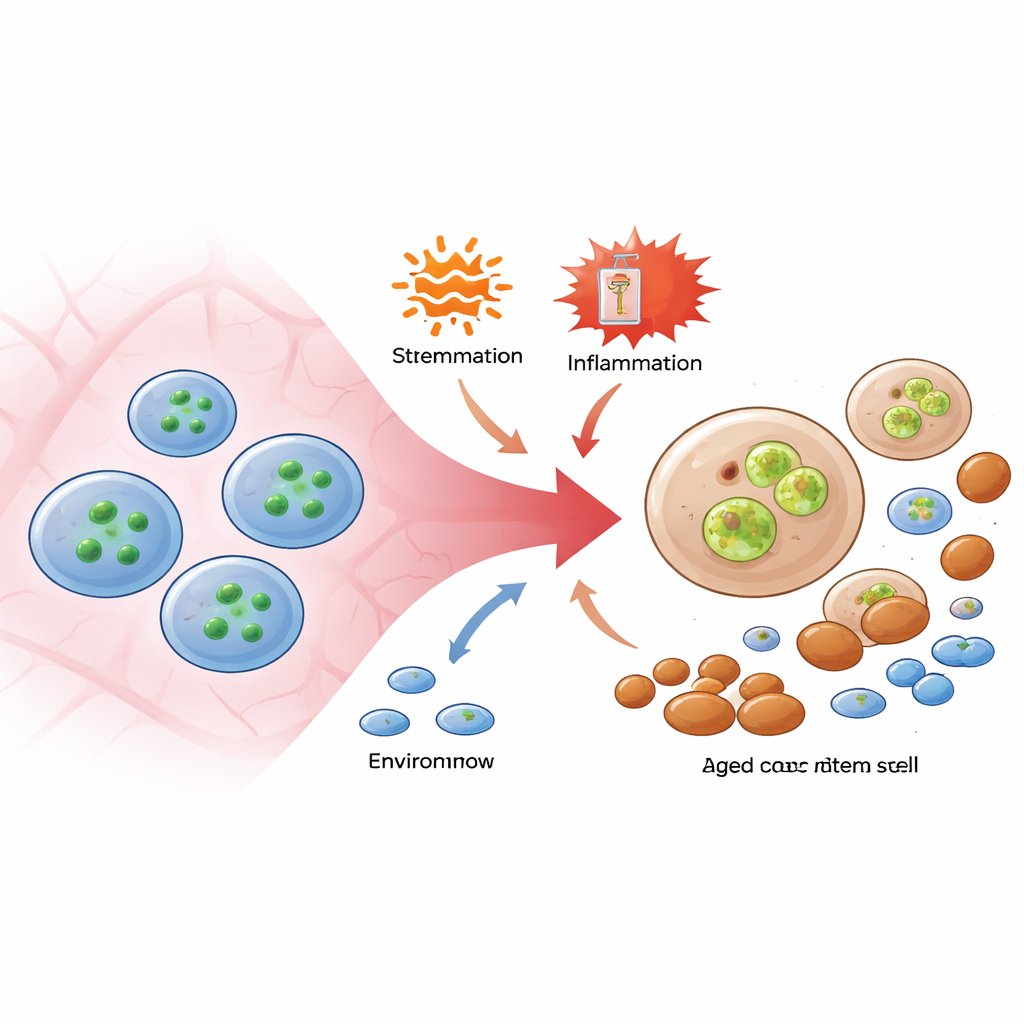
Путь повреждения, скрытый внутри выживших клеток
Чтобы отделить гибель от дисфункции, исследователи использовали мышей без MLKL или несущих вариант белка, который нельзя активировать через RIPK3. Когда этих животных подвергали воспалительным стимулям или повторной химиотерапии, их стволовые клетки выдерживали примерно так же, как у нормальных мышей, и общее число стволовых клеток в костном мозге оставалось схожим. Тем не менее типичные возрастные сдвиги — расширение пула стволовых клеток со смещением в сторону миелоидного направления и потеря сбалансированных стволовых клеток, способных давать и лимфоидные, и миелоидные линии — были заметно подавлены при отсутствии активности MLKL. Еще более впечатляюще: когда стволовые клетки, лишенные MLKL, подвергли онкогенному стрессу, который обычно моделирует предлейкемическое состояние, животные были защищены от тяжелой недостаточности костного мозга. Эти эксперименты показали, что MLKL может подрывать качество стволовых клеток изнутри, даже если ему не дают реализовать свою классическую программу клеточной гибели.
От износа к настоящему старению
Затем команда спросила, объясняет ли эта нефатальная активность MLKL обычное старение. У пожилых мышей сенсор MLKL светился ярче в стволовых клетках, что показало хроническую активацию этого пути с возрастом. Удаление MLKL не остановило накопление стволовых клеток с течением времени, но уменьшило классические признаки старения: кроветворение стало менее смещенным в сторону миелоидных клеток, ранние лимфоидные предшественники лучше сохранялись, а маркеры повреждения ДНК в стволовых клетках сокращались. Трансплантационные тесты подтвердили, что стареющие стволовые клетки без MLKL сохраняли большую регенеративную способность и более сбалансированное производство Т- и В-лимфоцитов. Важно, что окружающая среда костного мозга у старых мышей показывала схожие уровни воспалительных молекул независимо от наличия MLKL, а широкие обзоры активности генов и структуры хроматина в стволовых клетках выявили мало отличий между нормальными старыми клетками и клетками без MLKL. Это указывает на то, что MLKL действует в основном через физический, а не генетический механизм повреждения.
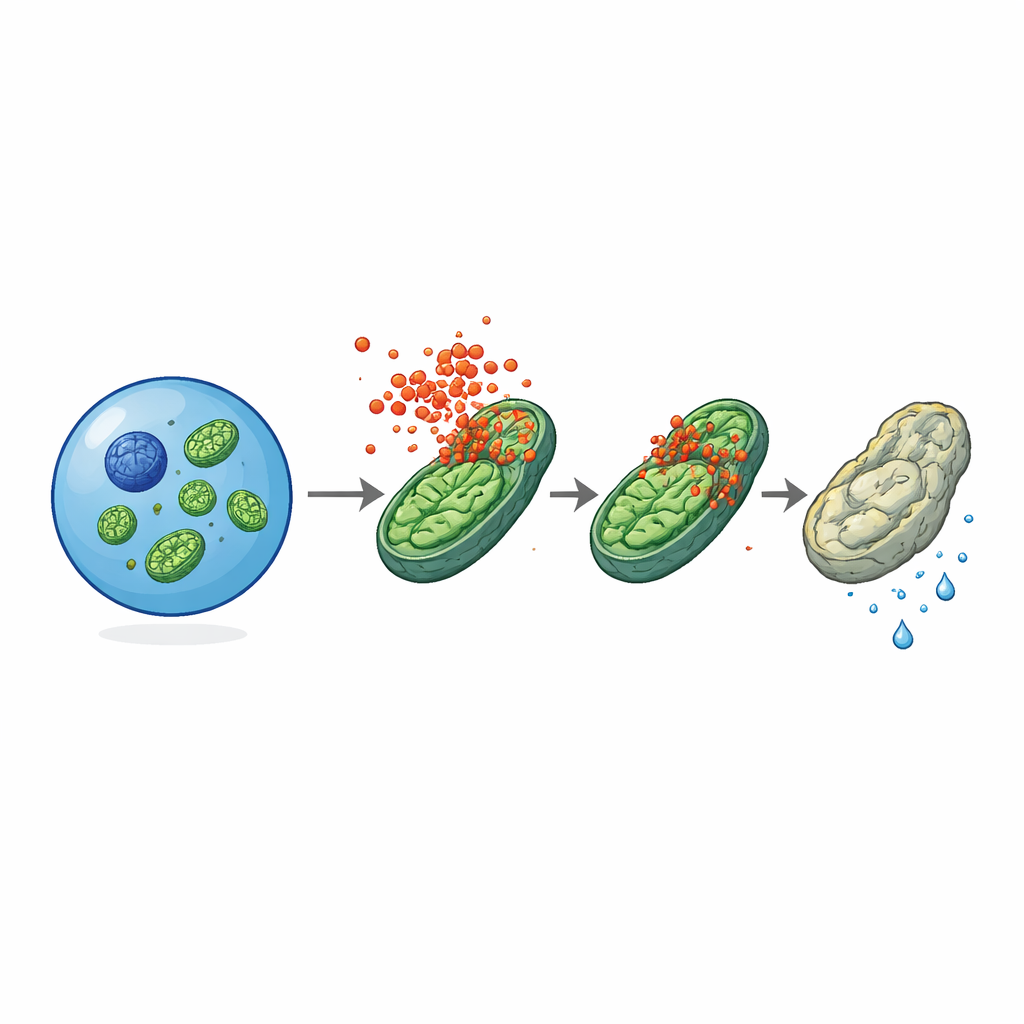
Атака на энергетические станции
Электронная микроскопия дала ключевую подсказку: митохондрии — крошечные органеллы, вырабатывающие энергию — выглядели вздутыми и деформированными в старых стволовых клетках нормальных мышей, но были гораздо здоровее в клетках того же возраста, лишенных MLKL. Активная, фосфорилированная форма MLKL обнаруживалась скоплениями на митохондриальных мембранах, особенно в старых или воспаленных стволовых клетках. Функциональные тесты показали, что старые стволовые клетки без MLKL имели более высокий митохондриальный мембранный потенциал, производили больше АТФ и поддерживали большую гликолитическую активность по сравнению с нормальными сверстниками, что указывает на то, что MLKL постепенно смещает их метаболизм от юношеского состояния с предпочитаемой гликолизом энергетикой к более стрессовому, требовательному к кислороду режиму. В изолированных митохондриях, подвергнутых воздействию очищенных фрагментов MLKL, белок напрямую снижал мембранный потенциал, что свидетельствует о том, что он может повреждать или дестабилизировать митохондриальные мембраны даже вне клеточного контекста.
Что это значит для здорового старения
В сумме работа показывает, что MLKL, давно известный как «палач» катастрофической клеточной гибели, также выполняет роль медленного саботажника митохондрий стволовых клеток. Повторяющиеся эпизоды воспаления, репликационного стресса и онкогенных ударов, по-видимому, сходятся в этой цепи, позволяя стволовым клеткам переживать острые кризисы, но ценой накопления повреждений, которые ослабляют их регенеративный потенциал и склоняют кроветворение к более рискованным схемам. Хотя MLKL и его партнеры в некоторых контекстах полезны для борьбы с инфекциями и сдерживания рака, точная настройка этого пути — или защита митохондрий от его нефатальных атак — может однажды помочь сохранить более молодую и устойчивую кровеносную систему по мере старения.
Цитирование: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Ключевые слова: старение гемопоэтических стволовых клеток, митохондриальная дисфункция, MLKL, воспаление и химиотерапевтический стресс, метаболизм кровяных стволовых клеток