Clear Sky Science · fr
Fonction non nécroptotique de MLKL endommage les mitochondries et favorise le vieillissement des cellules souches hématopoïétiques
Pourquoi l’usine à sang de notre vie s’use
Au cœur de nos os, une petite réserve de cellules souches construit discrètement toutes les cellules sanguines et immunitaires dont nous avons besoin tout au long de la vie. Avec l’âge, cette usine montre des signes de fatigue : les infections persistent, l’anémie devient plus fréquente et des cancers du sang tels que les syndromes myélodysplasiques apparaissent davantage. Cette étude met au jour un coupable moléculaire inattendu : un comportement surprenant d’une protéine appelée MLKL qui blesse progressivement les centrales énergétiques des cellules souches et contribue au vieillissement de notre système sanguin.
Des signaux de stress qui ne tuent pas tout à fait
Les cellules souches hématopoïétiques, ces rares « cellules maîtresses » de la moelle osseuse, résistent remarquablement à la mort, même lorsqu’elles sont assaillies par l’inflammation ou la chimiothérapie. Les auteurs se sont intéressés à une voie moléculaire normalement impliquée dans une forme spectaculaire de mort cellulaire appelée nécroptose, menée par deux protéines, RIPK3 et MLKL. En utilisant des souris génétiquement modifiées porteuses d’un détecteur fluorescent qui s’allume quand MLKL est activé, ils ont montré qu’une série de stress courants — molécules inflammatoires mimant une infection virale, composants bactériens et un médicament de chimiothérapie qui force les cellules souches à se diviser — activait de façon fiable MLKL dans les cellules souches et leurs progéniteurs immédiats, mais pas dans les précurseurs sanguins plus matures. De façon surprenante, malgré cette activation, les cellules souches ne mouraient pas en grand nombre. Au contraire, celles présentant une forte activité de MLKL montraient une moins bonne capacité d’engraftment et de production de cellules lymphoïdes lorsqu’elles étaient transplantées dans de nouveaux animaux, suggérant que MLKL endommageait discrètement la fonction plutôt que de déclencher une mort massive.
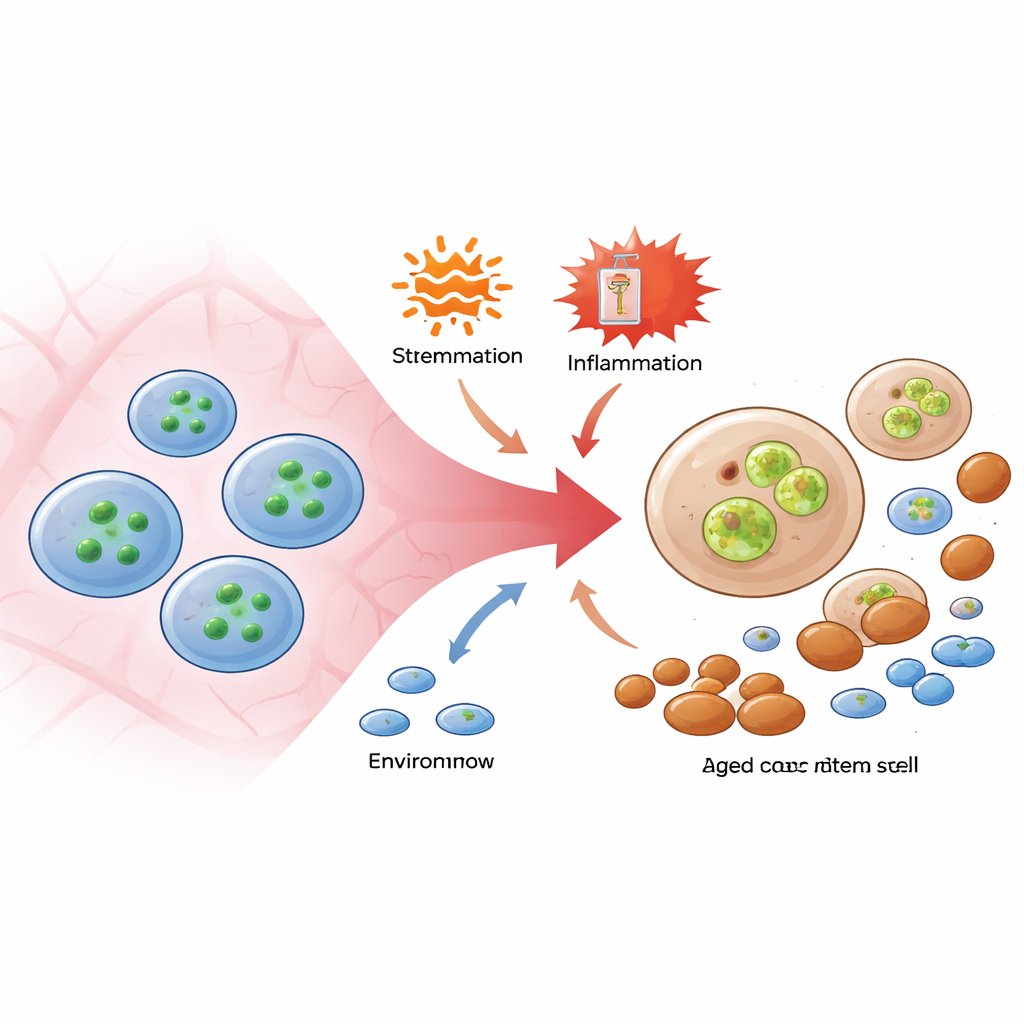
Une voie de dommage cachée au sein de cellules survivantes
Pour démêler mort et dysfonction, les chercheurs ont utilisé des souris dépourvues de MLKL, ou portant une forme de la protéine qui ne peut pas être activée par RIPK3. Lorsque ces animaux ont été exposés à des stimuli inflammatoires ou à des cycles répétés de chimiothérapie, leurs cellules souches survivaient à peu près autant que celles des souris normales, et le nombre total de cellules souches dans la moelle osseuse restait comparable. Cependant, les changements habituels liés à l’âge — expansion des cellules souches biaisées vers la production myéloïde et perte des cellules souches équilibrées capables de générer à la fois les lignées lymphoïde et myéloïde — étaient nettement atténués lorsque l’activité de MLKL était supprimée. Plus frappant encore, lorsque des cellules souches déficientes en MLKL ont été confrontées à un stress oncogénique modélisant habituellement une maladie pré‑leucémique, les animaux étaient protégés d’une insuffisance médullaire sévère. Ces expériences montrent que MLKL peut compromettre la qualité des cellules souches de l’intérieur, même lorsqu’on l’empêche d’exécuter son programme classique de mort cellulaire.
De l’usure au véritable vieillissement
L’équipe a ensuite cherché à savoir si cette activité non létale de MLKL pouvait expliquer le vieillissement normal. Chez les souris âgées, le détecteur de MLKL brillait plus intensément dans les cellules souches, révélant que cette voie est de plus en plus engagée avec l’âge. La suppression de MLKL n’empêchait pas l’accumulation de cellules souches au fil du temps, mais elle réduisait les traits classiques du vieillissement : la production sanguine était moins biaisée vers les cellules myéloïdes, les progéniteurs lymphoïdes précoces étaient mieux préservés et les marqueurs de dommages à l’ADN dans les cellules souches étaient diminués. Des tests de transplantation ont confirmé que les cellules souches âgées privées de MLKL conservaien t une puissance régénératrice plus forte et une production plus équilibrée de lymphocytes T et B. Fait important, l’environnement de la moelle osseuse chez les souris âgées présentait des niveaux similaires de molécules inflammatoires, que MLKL soit présent ou non, et des analyses larges de l’activité génique et de la structure de la chromatine dans les cellules souches révélaient peu de différences entre les cellules âgées normales et celles dépourvues de MLKL. Cela suggère que MLKL agit principalement par un mode de dommage physique, plutôt que génétique.
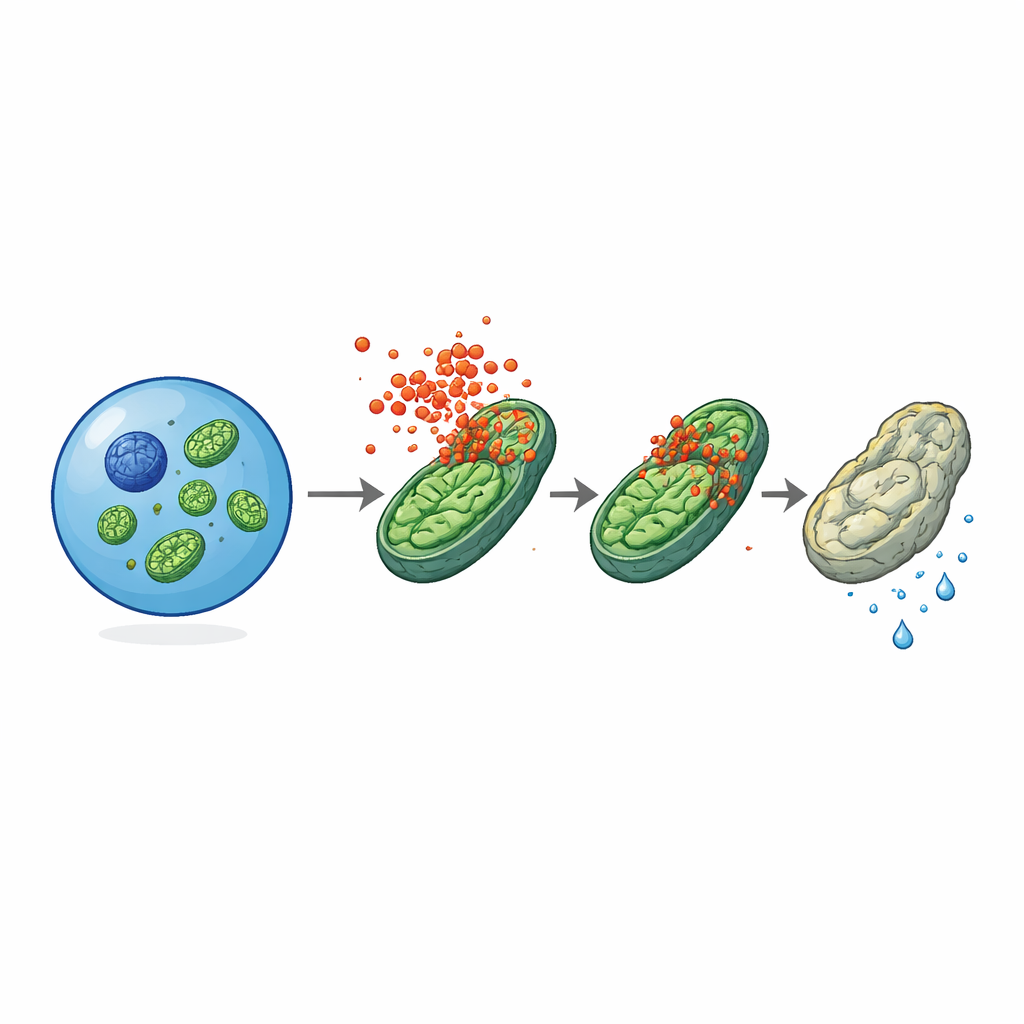
Des centrales énergétiques sous attaque
La microscopie électronique a fourni un indice crucial : les mitochondries — ces minuscules organites qui produisent l’énergie — apparaissaient gonflées et déformées dans les cellules souches âgées de souris normales, mais paraissaient bien plus saines dans les cellules du même âge privées de MLKL. La forme active et phosphorylée de MLKL se retrouvait regroupée sur les membranes mitochondriales, en particulier dans les cellules souches âgées ou enflammées. Des tests fonctionnels ont montré que les cellules souches âgées sans MLKL avaient un meilleur potentiel de membrane mitochondriale, produisaient plus d’ATP et maintenaient une activité glycolytique plus élevée que leurs homologues normales, suggérant que MLKL pousse progressivement leur métabolisme hors d’un état jeune plutôt axé sur la glycolyse vers un mode plus stressé et consommateur d’oxygène. Dans des mitochondries isolées exposées à des fragments purifiés de MLKL, la protéine réduisait directement le potentiel de membrane, indiquant qu’elle peut perforer ou déstabiliser les membranes mitochondriales même hors du contexte cellulaire complet.
Ce que cela signifie pour un vieillissement en bonne santé
Pris dans leur ensemble, ces travaux révèlent que MLKL, longtemps connu comme exécuteur d’une mort cellulaire catastrophique, joue aussi les saboteurs lents des mitochondries des cellules souches. Des épisodes répétés d’inflammation, de stress de réplication et d’insultes oncogéniques semblent converger vers cette voie, permettant aux cellules souches de survivre aux crises immédiates mais au prix d’un dommage cumulatif qui réduit leur capacité régénératrice et oriente la production sanguine vers des schémas plus risqués. Alors que MLKL et ses partenaires peuvent être bénéfiques pour combattre les infections et limiter certains cancers dans certains contextes, ajuster finement cette voie — ou protéger les mitochondries de ses attaques non létales — pourrait un jour aider à préserver un système sanguin plus jeune et plus résilient avec l’âge.
Citation: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Mots-clés: vieillissement des cellules souches hématopoïétiques, dysfonction mitochondriale, MLKL, inflammation et stress de chimiothérapie, métabolisme des cellules souches sanguines