Clear Sky Science · pl
Nie‑nekroptotyczna funkcja MLKL uszkadza mitochondria i sprzyja starzeniu się hematopoetycznych komórek macierzystych
Dlaczego nasza całe życie pracująca fabryka krwi się zużywa
Głęboko w kościach mała pula komórek macierzystych cicho wytwarza wszystkie komórki krwi i układu odpornościowego, których potrzebujemy przez całe życie. Z wiekiem ta fabryka słabnie: infekcje utrzymują się dłużej, niedokrwistość staje się częstsza, a nowotwory krwi, takie jak zespoły mielodysplastyczne, pojawiają się częściej. Badanie to odsłania ukrytego winowajcę molekularnego — nieoczekiwane zachowanie białka o nazwie MLKL — które stopniowo uszkadza elektrownię komórek macierzystych i przyczynia się do starzenia się układu krwiotwórczego.
Sygnały stresu, które nie zabijają do końca
Hematopoetyczne komórki macierzyste, rzadkie „komórki mistrzowskie” w szpiku kostnym, są wyjątkowo odporne na śmierć, nawet gdy są bombardowane zapaleniem lub chemioterapią. Autorzy skupili się na szlaku molekularnym zwykle wykorzystywanym do uruchamiania dramatycznej formy śmierci komórkowej zwanej nekroptozą, napędzanej przez dwa białka: RIPK3 i MLKL. Używając zmodyfikowanych myszy niosących fluorescencyjny czujnik, który świeci, gdy MLKL jest aktywowany, stwierdzili, że różne powszechne stresy — cząsteczki zapalne naśladujące infekcję wirusową, składniki bakteryjne i lek chemioterapeutyczny wymuszający podziały komórek — niezawodnie włączały MLKL w komórkach macierzystych i ich najbliższych progenitorach, ale nie w bardziej dojrzałych prekursorach krwi. Co zaskakujące, pomimo tej aktywacji komórki macierzyste nie ginęły masowo. Zamiast tego te z silnie aktywnym MLKL miały gorszą zdolność do zasiedlania i wytwarzania komórek limfoidalnych po przeszczepieniu do nowych myszy, co sugeruje, że MLKL cicho uszkadza funkcję, zamiast wywoływać bezpośrednią śmierć.
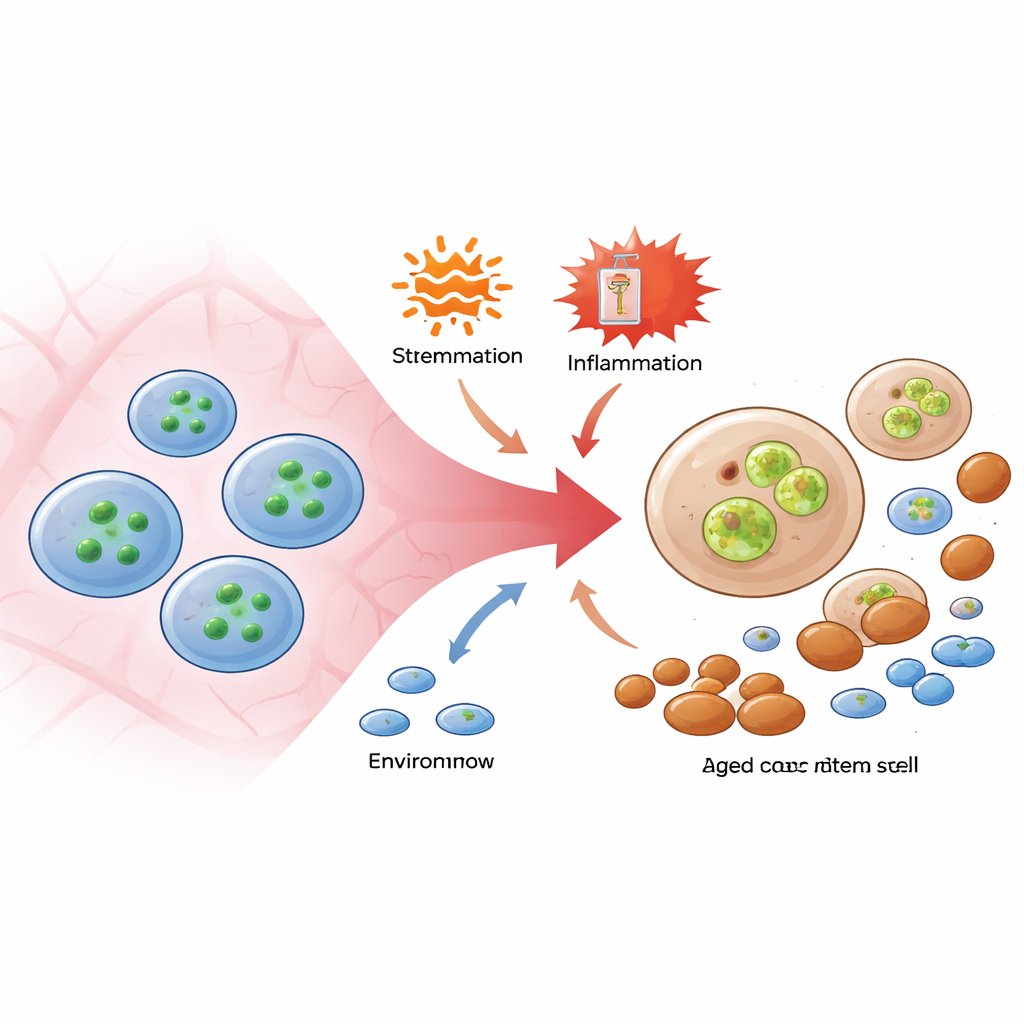
Ścieżka uszkodzeń ukryta w przeżywających komórkach
Aby rozróżnić śmierć od dysfunkcji, badacze użyli myszy pozbawionych MLKL lub niosących wersję białka, której nie można włączyć przez RIPK3. Kiedy te zwierzęta były wystawione na bodźce zapalne lub powtarzaną chemioterapię, ich komórki macierzyste przeżywały mniej więcej tak samo jak u myszy normalnych, a całkowita liczba komórek macierzystych w szpiku pozostawała podobna. Jednak typowe wiekowe zmiany — ekspansja komórek macierzystych zapatrzonych w produkcję komórek mieloidalnych i utrata zrównoważonych komórek macierzystych zdolnych do tworzenia zarówno linii limfoidalnej, jak i mieloidalnej — były wyraźnie złagodzone, gdy aktywność MLKL została usunięta. Jeszcze bardziej uderzające, gdy komórki macierzyste pozbawione MLKL zmuszono do stawienia czoła stresowi onkogennemu modelującemu zwykle przed‑białaczkową chorobę, zwierzęta były chronione przed ciężką niewydolnością szpiku. Eksperymenty te wykazały, że MLKL może podkopywać jakość komórek macierzystych „od środka”, nawet gdy uniemożliwia się mu wykonanie klasycznego programu śmierci komórkowej.
Od zużycia do prawdziwego starzenia
Zespół zapytał następnie, czy ta nieletalna aktywność MLKL pomaga wyjaśnić normalne starzenie. U starszych myszy czujnik MLKL świecił jaśniej w komórkach macierzystych, co ujawniło, że ten szlak staje się przewlekle zaangażowany z wiekiem. Usunięcie MLKL nie powstrzymało gromadzenia się komórek macierzystych w czasie, ale zmniejszyło klasyczne cechy starzenia: produkcja krwi stała się mniej przesunięta w stronę komórek mieloidalnych, wczesne progenitory limfoidalne były lepiej zachowane, a markery uszkodzeń DNA w komórkach macierzystych uległy redukcji. Testy przeszczepów potwierdziły, że stare komórki macierzyste pozbawione MLKL zachowały mocniejszą zdolność regeneracyjną i bardziej zrównoważoną produkcję limfocytów T i B. Co ważne, otoczenie szpiku kostnego u starych myszy wykazywało podobne poziomy cząsteczek zapalnych niezależnie od obecności MLKL, a szerokie przeglądy aktywności genów i struktury chromatyny w komórkach macierzystych wykazały niewielkie różnice między normalnymi starymi komórkami a tymi pozbawionymi MLKL. To sugeruje, że MLKL działa głównie przez sposób fizyczny, a nie genetyczny, powodując uszkodzenie.
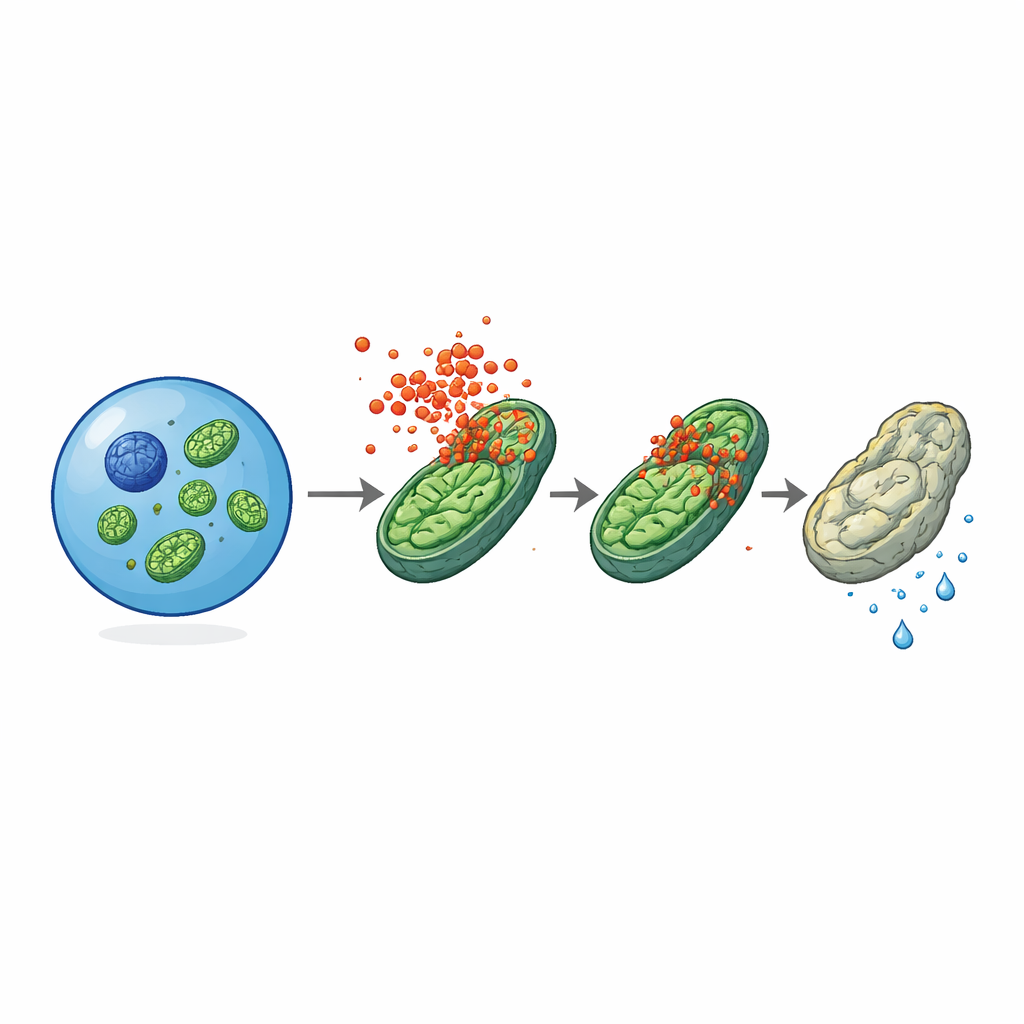
Atak na elektrownie komórkowe
Mikroskopia elektronowa dostarczyła kluczowej wskazówki: mitochondria — maleńkie organelle wytwarzające energię — wyglądały na spuchnięte i zdeformowane w starych komórkach macierzystych pochodzących od normalnych myszy, ale wydawały się znacznie zdrowsze w komórkach w tym samym wieku pozbawionych MLKL. Aktywna, ufosforylowana forma MLKL była wykrywana w skupiskach na błonach mitochondrialnych, szczególnie w komórkach macierzystych starych lub zapalnych. Testy funkcjonalne wykazały, że stare komórki macierzyste bez MLKL miały lepszy potencjał błony mitochondrialnej, produkowały więcej ATP i utrzymywały wyższą aktywność glikolityczną niż ich normalne odpowiedniki, co sugeruje, że MLKL stopniowo popycha ich metabolizm z młodzieńczego stanu preferującego glikolizę w stronę bardziej obciążonego, tlenowego trybu. W wyizolowanych mitochondriach wystawionych na oczyszczone fragmenty MLKL białko bezpośrednio obniżało potencjał błonowy, wskazując, że może ono uszkadzać lub destabilizować błony mitochondrialne nawet poza pełnym kontekstem komórkowym.
Co to oznacza dla zdrowego starzenia
Podsumowując, praca ujawnia, że MLKL, długo znany jako wykonawca katastrofalnej śmierci komórkowej, pełni także rolę powolnego sabotażysty mitochondriów komórek macierzystych. Powtarzające się epizody zapalenia, stres replikacyjny i urazy onkogenne wydają się zbiegać na tym szlaku, pozwalając komórkom macierzystym przetrwać natychmiastowe kryzysy, ale kosztem kumulatywnych uszkodzeń, które osłabiają ich zdolność regeneracyjną i przesuwają produkcję krwi w kierunku ryzykowniejszych wzorców. Choć MLKL i jego partnerzy mogą być korzystni w zwalczaniu infekcji i hamowaniu nowotworów w określonych kontekstach, ostrożne modulowanie tego szlaku — lub osłanianie mitochondriów przed jego nieletalnymi atakami — może pewnego dnia pomóc zachować młodszy, bardziej odporny układ krwiotwórczy w miarę starzenia się.
Cytowanie: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Słowa kluczowe: starzenie się hematopoetycznych komórek macierzystych, dysfunkcja mitochondrialna, MLKL, stres zapalny i chemioterapia, metabolizm komórek macierzystych krwi