Clear Sky Science · nl
Niet-necroptotische MLKL-functie beschadigt mitochondriën en bevordert veroudering van hematopoëtische stamcellen
Waarom de levenslange fabriek van ons bloed verslijt
Diep in onze botten bouwt een kleine voorraad stamcellen geruisloos alle bloed- en immuuncellen die we ons hele leven nodig hebben. Met het ouder worden hapert deze fabriek: infecties duren langer, bloedarmoede komt vaker voor en bloedkankers zoals myelodysplastische syndromen treden vaker op. Deze studie onthult een verborgen moleculaire dader—een onverwacht gedrag van een eiwit genaamd MLKL—dat langzaam de energiecentrales van stamcellen beschadigt en bijdraagt aan de veroudering van ons bloedvitalsysteem.
Stresssignalen die niet helemaal doden
Hematopoëtische stamcellen, de zeldzame “meester”-cellen in het beenmerg, zijn ongewoon resistent tegen celdood, zelfs wanneer ze worden blootgesteld aan ontsteking of chemotherapie. De auteurs richtten zich op een moleculaire route die normaal wordt gebruikt om een dramatische vorm van celdood te activeren, necroptose, gedreven door twee eiwitten, RIPK3 en MLKL. Met behulp van genetisch gemodificeerde muizen die een fluorescerende sensor dragen die oplicht wanneer MLKL wordt geactiveerd, vonden ze dat een reeks gangbare stressoren—ontstekingsmoleculen die virale infectie nabootsen, bacteriële componenten en een chemotherapiemiddel dat stamcellen dwingt te delen—betrouwbaar MLKL activeerden in stamcellen en hun dichtstbijzijnde nageslacht, maar niet in meer rijpe bloedvoorlopers. Verrassend genoeg stierven de stamcellen, ondanks deze activatie, niet in groten getale. In plaats daarvan hadden de cellen met sterk actieve MLKL een slechtere capaciteit om zich in te nestelen en lymfoïde cellen te vormen wanneer ze in nieuwe muizen werden getransplanteerd, wat suggereert dat MLKL stilletjes functie beschadigt in plaats van directe celdood te veroorzaken.
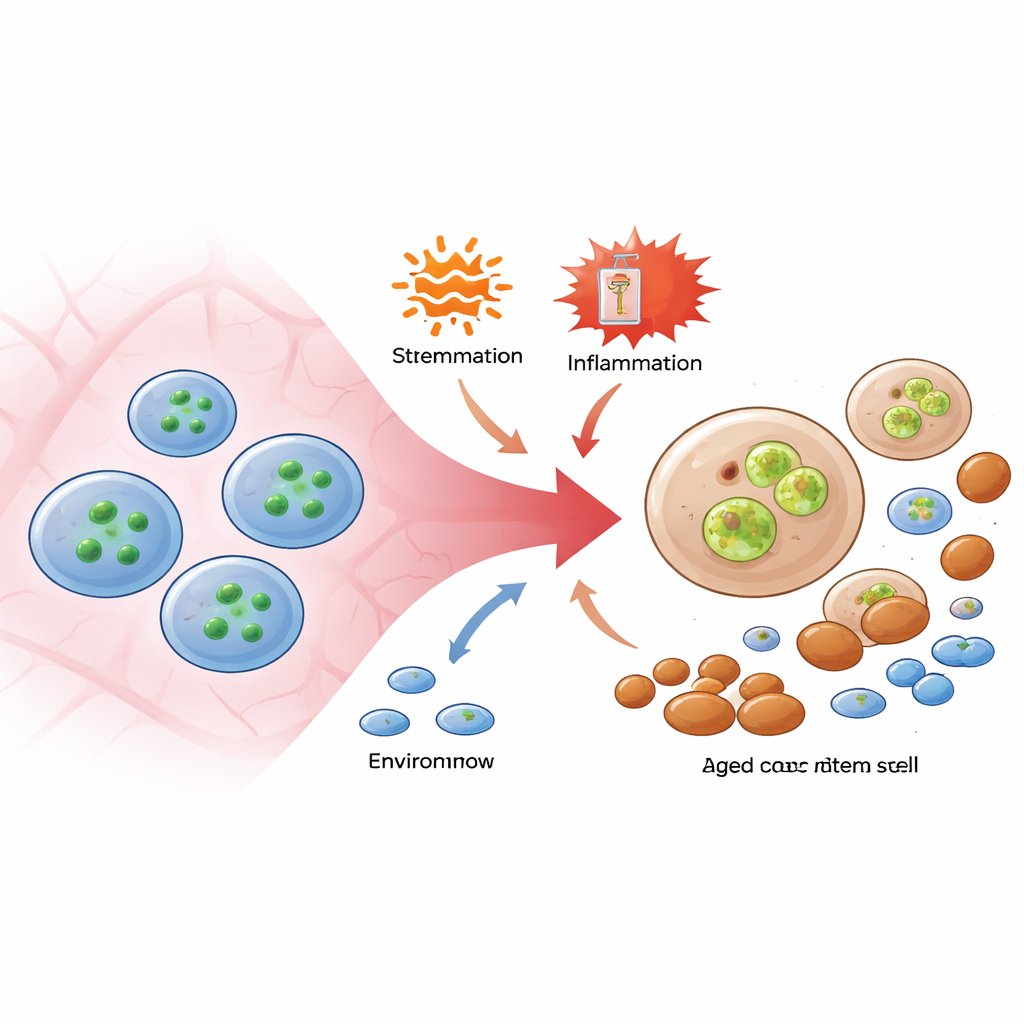
Een schadepad verborgen binnen overlevende cellen
Om dood van disfunctie te scheiden, gebruikten de onderzoekers muizen zonder MLKL, of muizen met een versie van het eiwit die niet door RIPK3 kan worden geactiveerd. Wanneer deze dieren werden blootgesteld aan ontstekingsstimuli of herhaalde chemotherapie, overleefden hun stamcellen ongeveer even goed als die van normale muizen, en het totale aantal stamcellen in het beenmerg bleef vergelijkbaar. De gebruikelijke leeftijdsgerelateerde verschuivingen—uitbreiding van stamcellen die de neiging hebben myeloïde cellen te produceren en verlies van gebalanceerde stamcellen die zowel lymfoïde als myeloïde lijnen kunnen maken—werden echter duidelijk afgezwakt wanneer MLKL-activiteit werd verwijderd. Nog opvallender was dat, wanneer MLKL-deficiënte stamcellen werden blootgesteld aan een oncogene stress die gewoonlijk pre-leukemische ziekte nabootst, de dieren beschermd waren tegen ernstige beenmergfalen. Deze experimenten toonden aan dat MLKL de kwaliteit van stamcellen van binnenuit kan ondermijnen, zelfs wanneer het wordt verhinderd zijn klassieke celdoodprogramma uit te voeren.
Van slijtage naar ware veroudering
Het team vroeg zich vervolgens af of deze niet-dodelijke MLKL-activiteit normale veroudering kan verklaren. Bij oudere muizen lichtte de MLKL-sensor helderder op in stamcellen, wat liet zien dat dit pad chronisch geactiveerd raakt met de leeftijd. Het verwijderen van MLKL stopte niet dat stamcellen in de loop van de tijd ophoopten, maar het verminderde wel klassieke kenmerken van veroudering: de bloedvorming scheef minder richting myeloïde cellen, vroege lymfoïde voorlopercellen bleven beter bewaard en DNA-schademarkers in stamcellen waren verminderd. Transplantatietests bevestigden dat oude stamcellen zonder MLKL sterkere regeneratieve kracht en een evenwichtiger productie van T- en B-lymfocyten behielden. Belangrijk is dat de omliggende beenmergomgeving in oude muizen vergelijkbare niveaus van ontstekingsmoleculen vertoonde, ongeacht de aanwezigheid van MLKL, en breedgaande onderzoeken van genexpressie en chromatinestructuur in stamcellen lieten weinig verschil zien tussen normale oude cellen en cellen zonder MLKL. Dat suggereert dat MLKL hoofdzakelijk werkt via een fysiek, eerder dan genetisch, schademechanisme.
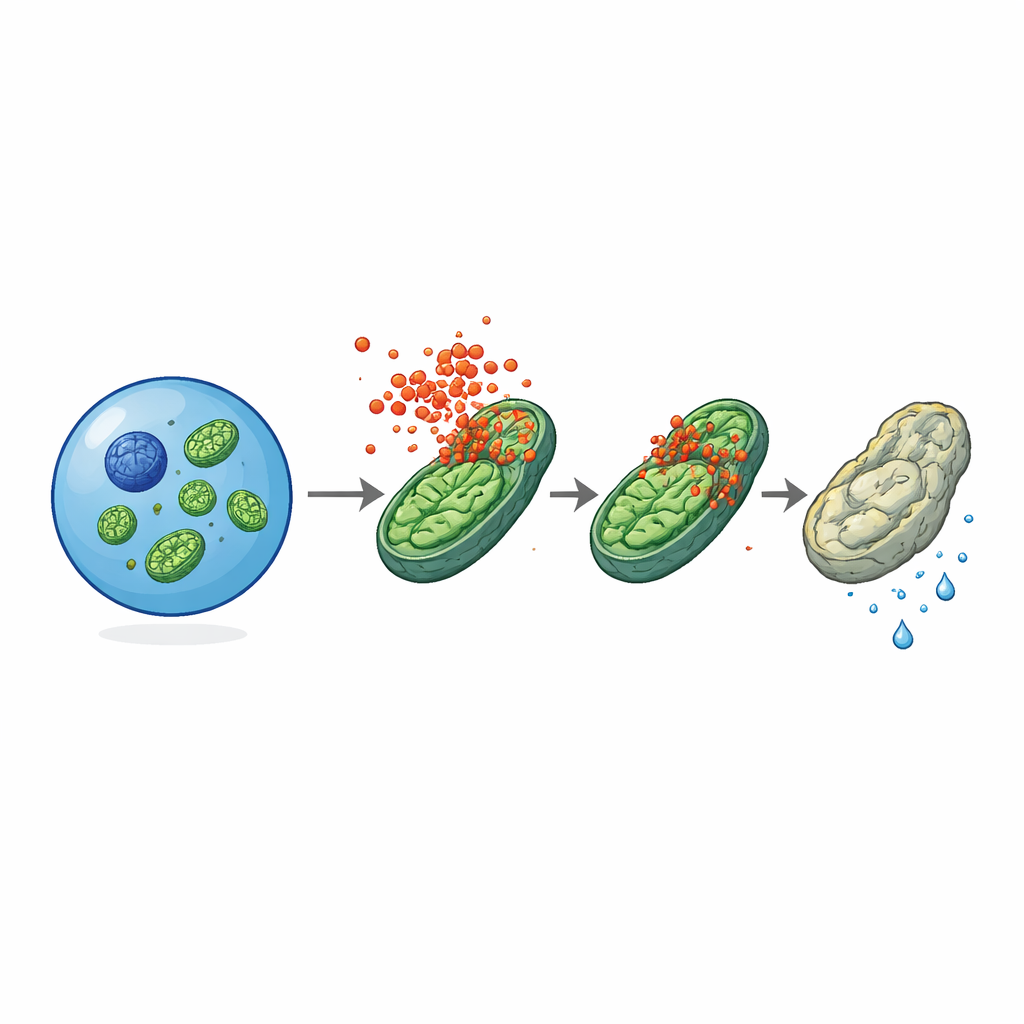
Energiecentrales onder aanval
Elektronenmicroscopie gaf een cruciale aanwijzing: mitochondriën—de kleine organellen die energie genereren—leken gezwollen en misvormd in oude stamcellen van normale muizen, maar oogden veel gezonder in leeftijdsgenoten zonder MLKL. De actieve, gefosforyleerde vorm van MLKL werd gevonden in clusters op mitochondriale membranen, vooral in oude of ontstoken stamcellen. Functionele tests toonden aan dat oude stamcellen zonder MLKL een betere mitochondriale membraanpotentiaal hadden, meer ATP produceerden en een hogere glycolytische activiteit behielden dan hun normale tegenhangers, wat suggereert dat MLKL hun metabolisme geleidelijk wegduwt van een jeugdig, op glycolyse gericht profiel naar een meer gestreste, zuurstofvragende toestand. In geïsoleerde mitochondriën die werden blootgesteld aan gezuiverde MLKL-fragmenten, verlaagde het eiwit direct de membraanpotentiaal, wat aangeeft dat het membranen van mitochondriën kan doorboren of destabiliseren, zelfs buiten de volledige cellulaire context.
Wat dit betekent voor gezond ouder worden
Alles bij elkaar laat het werk zien dat MLKL, lang bekend als een uitvoerder van catastrofale celdood, ook een sluipende saboteur is van mitochondriën in stamcellen. Herhaalde episodes van ontsteking, replicatiestress en oncogene aanvallen lijken op deze route samen te komen, waardoor stamcellen acute crises overleven maar daardoor cumulatieve schade oplopen die hun regeneratieve capaciteit verlaagt en de bloedvorming naar riskantere patronen kantelt. Hoewel MLKL en zijn partners in bepaalde contexten nuttig kunnen zijn om infecties te bestrijden en kanker te remmen, kan het zorgvuldig bijsturen van dit pad—of het afschermen van mitochondriën tegen zijn niet-dodelijke aanvallen—op termijn helpen een jonger, veerkrachtiger bloedstelsel te behouden naarmate we ouder worden.
Bronvermelding: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Trefwoorden: veroudering van hematopoëtische stamcellen, mitochondriale disfunctie, MLKL, ontsteking en chemotherapiestress, metabolisme van bloedstamcellen