Clear Sky Science · de
Nekroptoseunabhängige MLKL-Funktion schädigt Mitochondrien und fördert die Alterung hämatopoetischer Stammzellen
Warum die lebenslange Fabrik unseres Bluts verschleißt
Tief in unseren Knochen sorgt ein kleiner Pool von Stammzellen unaufhörlich für alle Blut- und Immunzellen, die wir im Laufe des Lebens brauchen. Mit dem Alter gerät diese Fabrik ins Stocken: Infektionen dauern länger, Anämie wird häufiger, und Blutkrebserkrankungen wie myelodysplastische Syndrome treten vermehrt auf. Die vorliegende Studie enthüllt einen versteckten molekularen Übeltäter — ein unerwartetes Verhalten des Proteins MLKL — das nach und nach die Kraftwerke der Stammzellen schädigt und so zur Alterung unseres Blutsystems beiträgt.
Stresssignale, die nicht ganz töten
Hämatopoetische Stammzellen, die seltenen „Master“-Zellen im Knochenmark, sind ungewöhnlich widerstandsfähig gegenüber Zelltod, selbst wenn sie durch Entzündung oder Chemotherapie unter Druck gesetzt werden. Die Autoren konzentrierten sich auf einen molekularen Weg, der normalerweise verwendet wird, um eine dramatische Form des Zelltods namens Nekroptose auszulösen, angetrieben von den Proteinen RIPK3 und MLKL. Mithilfe gentechnisch veränderter Mäuse mit einem fluoreszenten Sensor, der aufleuchtet, wenn MLKL aktiviert wird, stellten sie fest, dass eine Reihe verbreiteter Stressoren — entzündliche Moleküle, die eine Virusinfektion nachahmen, bakterielle Komponenten und ein Chemotherapeutikum, das Stammzellen zur Teilung zwingt — zuverlässig MLKL in Stammzellen und ihren engsten Vorläufern aktivierten, jedoch nicht in reiferen Blutvorläufern. Überraschenderweise führte diese Aktivierung nicht zu einem massiven Zelltod. Stattdessen zeigten Zellen mit stark aktiven MLKL eine schlechtere Fähigkeit zur Einnistung und zur Bildung lymphoider Zellen nach Transplantation in neue Mäuse, was darauf hindeutet, dass MLKL eher die Funktion untergräbt als einen offensichtlichen Tod auszulösen.
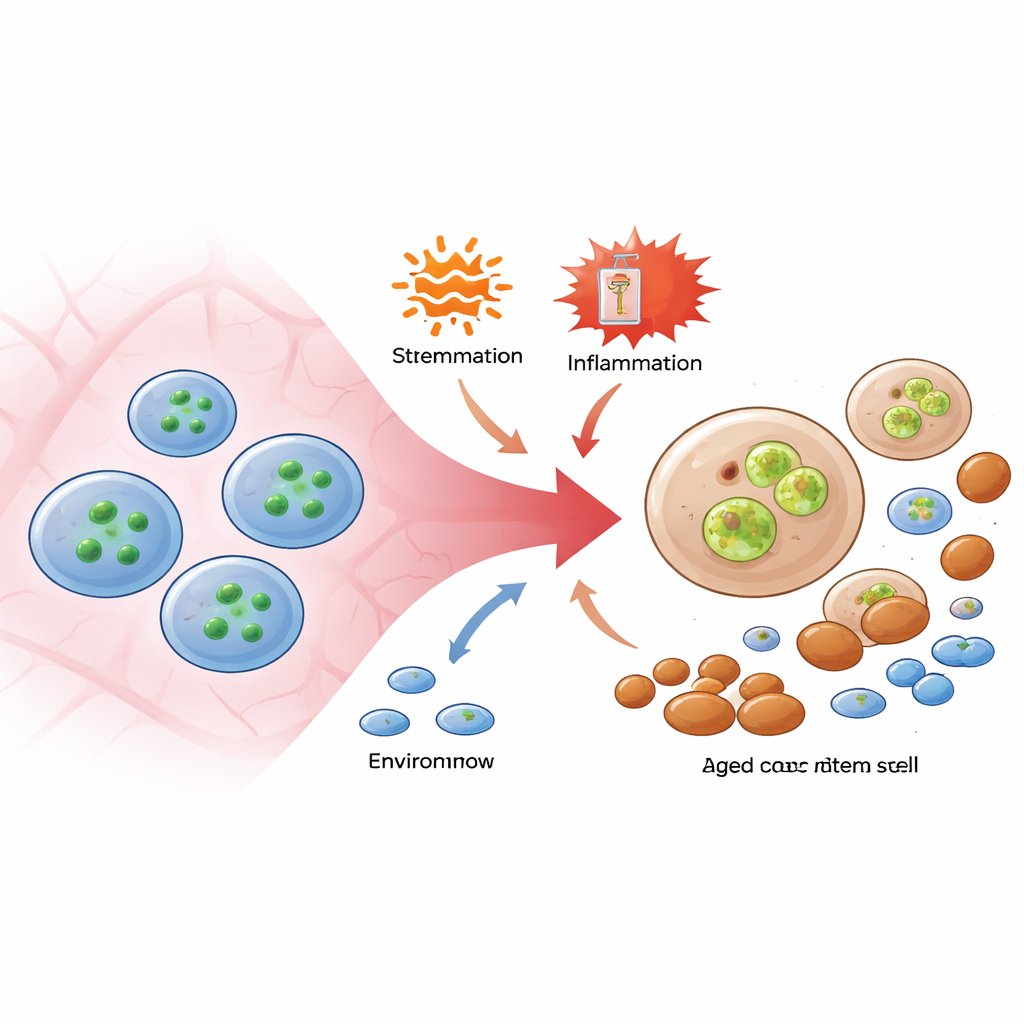
Ein Schadensweg verborgen in überlebenden Zellen
Um Tod und Dysfunktion zu entkoppeln, verwendeten die Forscher Mäuse, denen MLKL fehlte, oder Mäuse, die eine Version des Proteins trugen, die von RIPK3 nicht aktiviert werden kann. Wenn diese Tiere entzündlichen Stimuli oder wiederholter Chemotherapie ausgesetzt wurden, überlebten ihre Stammzellen etwa genauso gut wie die normaler Mäuse, und die Gesamtzahl der Stammzellen im Knochenmark blieb ähnlich. Allerdings waren die typischen altersähnlichen Verschiebungen — eine Ausweitung von Stammzellen mit myeloider Tendenz und der Verlust ausgeglichener Stammzellen, die sowohl lymphoide als auch myeloide Linien erzeugen können — deutlich abgeschwächt, wenn MLKL-Aktivität fehlte. Noch auffälliger: Wenn MLKL-defiziente Stammzellen einem onkogenen Stress ausgesetzt wurden, der normalerweise ein präleukämisches Modell nachahmt, waren die Tiere vor schwerer Knochenmarkinsuffizienz geschützt. Diese Experimente zeigten, dass MLKL die Qualität von Stammzellen von innen heraus unterminieren kann, selbst wenn es daran gehindert ist, sein klassisches Tötungsprogramm auszuführen.
Vom Verschleiß zur echten Alterung
Das Team fragte anschließend, ob diese nicht‑tödliche MLKL-Aktivität die normale Alterung erklären hilft. In älteren Mäusen leuchtete der MLKL-Sensor in Stammzellen stärker auf, was zeigt, dass dieser Weg mit dem Alter chronisch aktiviert ist. Das Entfernen von MLKL verhinderte nicht, dass Stammzellen im Laufe der Zeit zunahmen, reduzierte jedoch klassische Altersmerkmale: die Blutbildung war weniger stark zugunsten myeloider Zellen verschoben, frühe lymphoide Vorläufer wurden besser erhalten, und DNA-Schadensmarker in Stammzellen waren reduziert. Transplantationstests bestätigten, dass gealterte Stammzellen ohne MLKL eine stärkere regenerative Kapazität und eine ausgewogenere Produktion von T‑ und B‑Lymphozyten behielten. Wichtig ist, dass die umgebende Knochenmarksnische in gealterten Mäusen ähnliche Mengen entzündlicher Moleküle zeigte, unabhängig davon, ob MLKL vorhanden war oder nicht, und breit angelegte Analysen der Genaktivität und Chromatinstruktur in Stammzellen wenig Unterschied zwischen normalen alten Zellen und solchen ohne MLKL ergaben. Das deutet darauf hin, dass MLKL hauptsächlich durch einen physischen, eher als einen genetischen Schadensmechanismus wirkt.
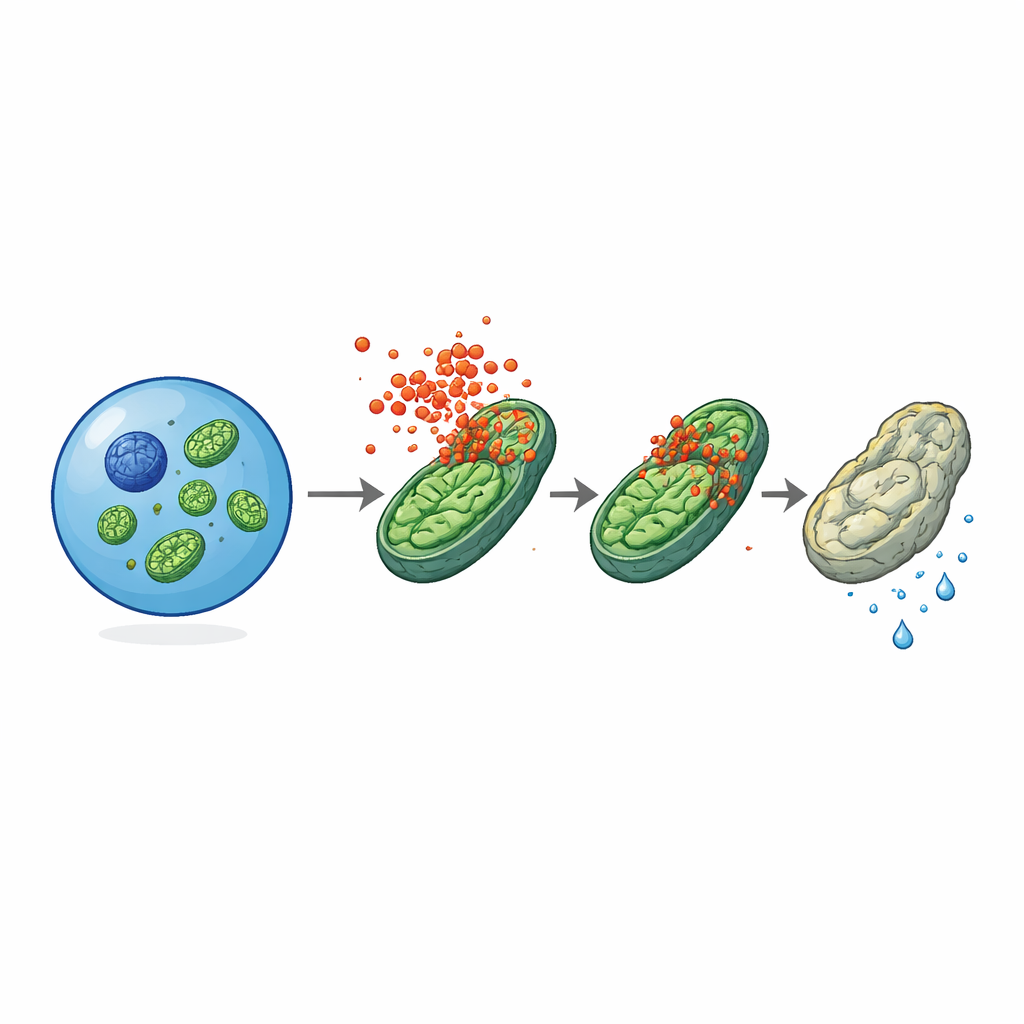
Kraftwerke unter Angriff
Die Elektronenmikroskopie lieferte einen entscheidenden Hinweis: Mitochondrien — die winzigen Organellen, die Energie erzeugen — wirkten in alten Stammzellen normaler Mäuse geschwollen und verformt, erschienen aber in altersgleichen Zellen ohne MLKL deutlich gesünder. Die aktive, phosphorylierte Form von MLKL fand sich gehäuft an mitochondrialen Membranen, besonders in gealterten oder entzündeten Stammzellen. Funktionelle Tests zeigten, dass alte Stammzellen ohne MLKL ein besseres mitochondriales Membranpotenzial hatten, mehr ATP produzierten und eine höhere glykolytische Aktivität aufwiesen als ihre normalen Gegenstücke. Das deutet darauf hin, dass MLKL ihre Zellstoffwechsel allmählich von einem jugendlichen, glykolyselastigen Zustand hin zu einem gestressteren, stärker auf Sauerstoff angewiesenen Zustand verschiebt. In isolierten Mitochondrien, die gereinigten MLKL‑Fragmenten ausgesetzt wurden, reduzierte das Protein direkt das Membranpotenzial, was darauf hinweist, dass es mitochondriale Membranen direkt stören oder destabilisieren kann, selbst außerhalb des vollständigen zellulären Kontexts.
Was das für gesundes Altern bedeutet
Zusammengefasst zeigt die Arbeit, dass MLKL, lange bekannt als Vollstrecker katastrophalen Zelltods, auch als langsamer Saboteur der Stammzell‑Mitochondrien fungiert. Wiederholte Schübe von Entzündung, Replikationsstress und onkogenen Angriffen scheinen auf diesen Weg zusammenzulaufen, sodass Stammzellen unmittelbare Krisen überleben, jedoch auf Kosten kumulativer Schäden, die ihre regenerative Fähigkeit abschwächen und die Blutbildung in risikoreichere Muster kippen. Während MLKL und seine Partner in bestimmten Kontexten nützlich sind, etwa beim Kampf gegen Infektionen und bei der Eindämmung von Krebs, könnte die gezielte Feinabstimmung dieses Weges — oder das Abschirmen von Mitochondrien gegen seine nicht‑tödlichen Angriffe — eines Tages helfen, ein jüngeres, widerstandsfähigeres Blutsystem im Alter zu bewahren.
Zitation: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Schlüsselwörter: Alterung hämatopoetischer Stammzellen, mitochondriale Dysfunktion, MLKL, Entzündung und Chemotherapie-Stress, Stoffwechsel von Blutstammzellen