Clear Sky Science · pt
Função não-necroptótica da MLKL danifica mitocôndrias e promove o envelhecimento de células‑tronco hematopoéticas
Por que a fábrica vital do nosso sangue se desgasta ao longo da vida
Nas profundezas dos nossos ossos, uma pequena reserva de células‑tronco constrói silenciosamente todas as células sanguíneas e do sistema imune de que precisamos durante a vida. Com o avanço da idade, essa fábrica falha: infecções persistem, anemia se torna mais frequente e cânceres sanguíneos, como síndromes mielodisplásicas, surgem com maior incidência. Este estudo revela um culpado molecular oculto — um comportamento inesperado de uma proteína chamada MLKL — que paulatinamente prejudica as usinas de energia das células‑tronco e contribui para o envelhecimento do nosso sistema sanguíneo.
Sinais de estresse que não chegam a matar
As células‑tronco hematopoéticas, as raras “mestres” da medula óssea, são notavelmente resistentes à morte, mesmo quando submetidas a inflamação ou quimioterapia. Os autores concentraram‑se numa via molecular normalmente usada para desencadear uma forma dramática de morte celular chamada necroptose, estimulada por duas proteínas, RIPK3 e MLKL. Usando camundongos geneticamente modificados com um sensor fluorescente que acende quando a MLKL é ativada, eles descobriram que uma variedade de estresses comuns — moléculas inflamatórias que imitam infecção viral, componentes bacterianos e um fármaco quimioterápico que força as células‑tronco a se dividirem — ativava de forma consistente a MLKL nas células‑tronco e em seus progenitores mais próximos, mas não em precursores sanguíneos mais maduros. Surpreendentemente, apesar dessa ativação, as células‑tronco não morreram em grande número. Em vez disso, aquelas com MLKL altamente ativa mostraram menor capacidade de enxertia e de gerar células linfóides quando transplantadas para novos animais, sugerindo que a MLKL prejudicava silenciosamente a função em vez de provocar morte imediata.
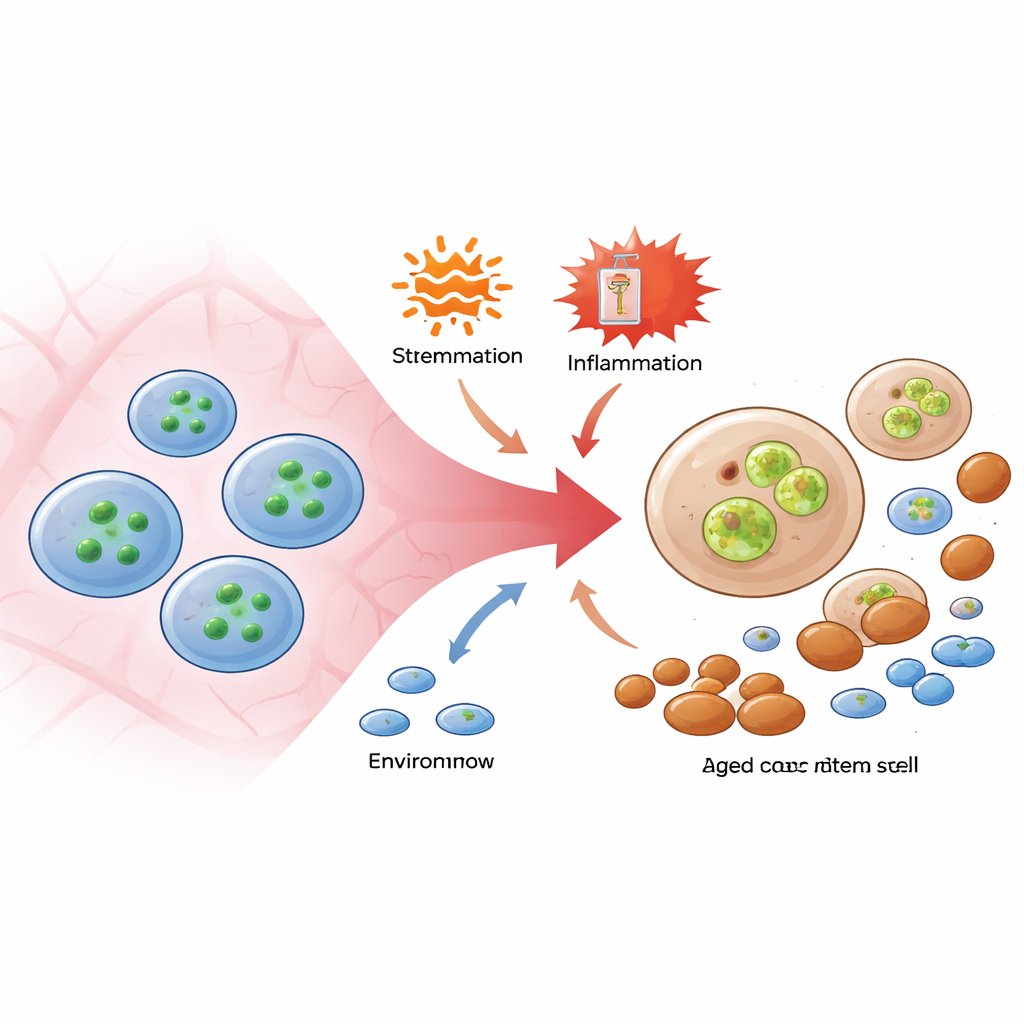
Uma via de dano oculta dentro de células sobreviventes
Para separar morte de disfunção, os pesquisadores usaram camundongos sem MLKL ou portadores de uma versão da proteína que não pode ser ativada por RIPK3. Quando esses animais foram desafiados com estímulos inflamatórios ou ciclos repetidos de quimioterapia, suas células‑tronco sobreviveram em nível semelhante ao dos camundongos normais, e o número total de células‑tronco na medula óssea permaneceu parecido. Contudo, as mudanças típicas associadas ao envelhecimento — expansão de células‑tronco tendendo à produção de linhagem mieloide e perda de células‑tronco equilibradas capazes de gerar tanto linhagens linfóide quanto mieloide — foram marcadamente atenuadas quando a atividade da MLKL foi removida. Ainda mais notável, quando células‑tronco deficientes em MLKL foram submetidas a um estresse oncogênico que normalmente modela doença pré‑leucêmica, os animais foram protegidos de falência grave da medula óssea. Esses experimentos mostraram que a MLKL pode minar a qualidade das células‑tronco de dentro, mesmo quando está impedida de executar seu programa clássico de morte celular.
Do desgaste ao envelhecimento verdadeiro
Em seguida, a equipe perguntou se essa atividade não letal da MLKL ajuda a explicar o envelhecimento normal. Em camundongos mais velhos, o sensor de MLKL brilhava mais intensamente nas células‑tronco, revelando que essa via torna‑se cronicamente engajada com a idade. A deleção de MLKL não impediu o acúmulo de células‑tronco ao longo do tempo, mas atenuou sinais clássicos de envelhecimento: a produção sanguínea ficou menos enviesada para linhagem mieloide, os progenitores linfóides precoces foram melhor preservados e marcadores de dano ao DNA nas células‑tronco foram reduzidos. Testes de transplante confirmaram que células‑tronco envelhecidas sem MLKL mantinham maior poder regenerativo e produção mais equilibrada de linfócitos T e B. Importante, o microambiente da medula óssea em camundongos idosos mostrou níveis semelhantes de moléculas inflamatórias, com ou sem MLKL, e levantamentos amplos de atividade gênica e estrutura da cromatina nas células‑tronco revelaram pouca diferença entre células velhas normais e aquelas sem MLKL. Isso sugere que a MLKL age principalmente por um modo físico, em vez de genético, de dano.
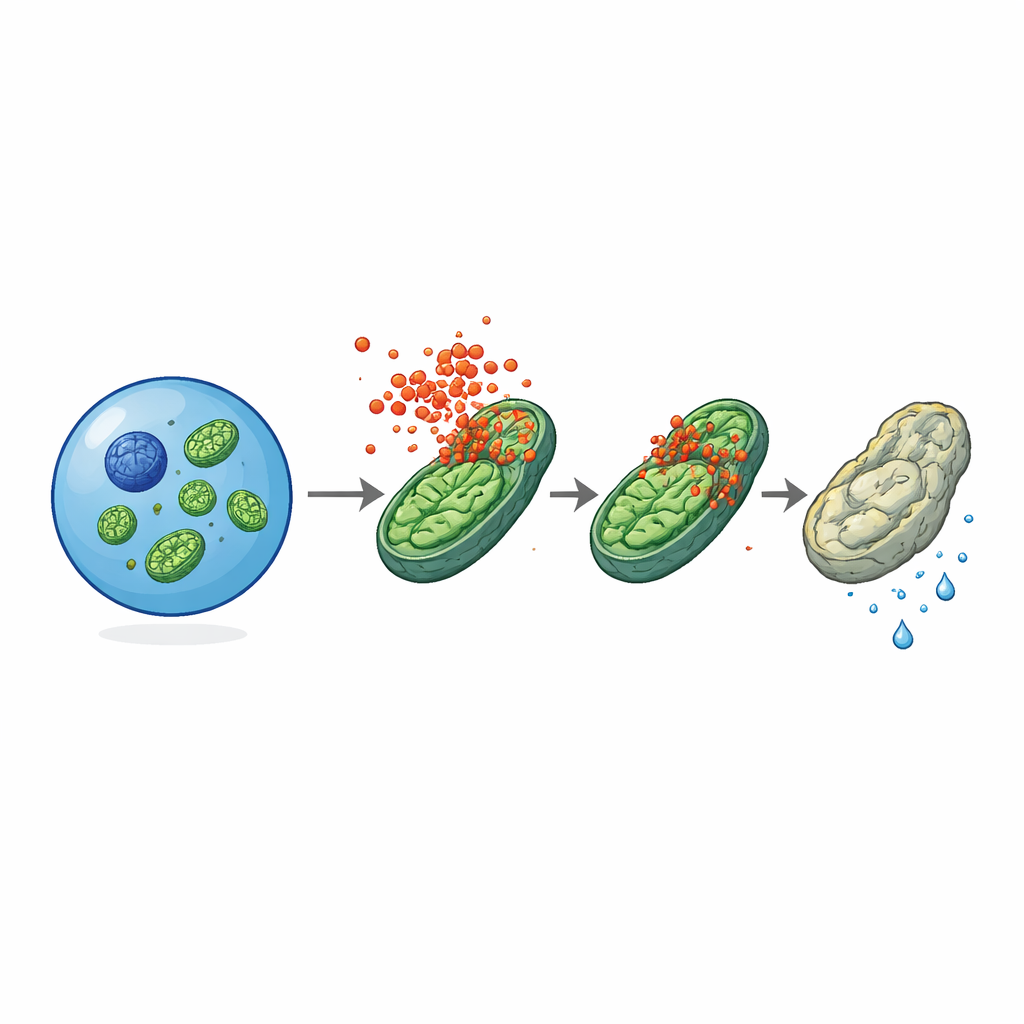
Usinas de energia sob ataque
A microscopia eletrônica forneceu uma pista crucial: as mitocôndrias — os pequenos organelos que geram energia — pareciam inchadas e com morfologia alterada em células‑tronco velhas de camundongos normais, mas mostravam‑se muito mais saudáveis em células da mesma idade desprovidas de MLKL. A forma ativa e fosforilada da MLKL foi encontrada agrupando‑se nas membranas mitocondriais, especialmente em células‑tronco envelhecidas ou inflamadas. Testes funcionais mostraram que células‑tronco idosas sem MLKL tinham melhor potencial de membrana mitocondrial, produziam mais ATP e mantinham maior atividade glicolítica do que suas contrapartes normais, sugerindo que a MLKL empurra gradualmente seu metabolismo de um estado juvenil, inclinado à glicólise, para um modo mais estressado e dependente de oxigênio. Em mitocôndrias isoladas expostas a fragmentos purificados de MLKL, a proteína reduziu diretamente o potencial de membrana, indicando que ela pode perfurar ou desestabilizar membranas mitocondriais mesmo fora do contexto celular completo.
O que isso significa para um envelhecimento saudável
Em conjunto, o trabalho revela que a MLKL, conhecida há muito como executora de morte celular catastrófica, também atua como sabotadora lenta das mitocôndrias das células‑tronco. Repentes repetidos de inflamação, estresse de replicação e insultos oncogênicos parecem convergir nessa via, permitindo que as células‑tronco sobrevivam às crises imediatas, mas ao custo de danos acumulativos que reduzem sua capacidade regenerativa e inclinam a produção sanguínea para padrões mais arriscados. Embora a MLKL e seus parceiros possam ser úteis no combate a infecções e no controle do câncer em certos contextos, modular cuidadosamente essa via — ou proteger as mitocôndrias de seus ataques não letais — pode, um dia, ajudar a preservar um sistema sanguíneo mais jovem e resiliente à medida que envelhecemos.
Citação: Yamada, Y., Yang, J., Saiki-Tsuchiya, A. et al. Non-necroptotic MLKL function damages mitochondria and promotes hematopoietic stem cell aging. Nat Commun 17, 2798 (2026). https://doi.org/10.1038/s41467-026-71060-4
Palavras-chave: envelhecimento de células‑tronco hematopoéticas, disfunção mitocondrial, MLKL, inflamação e estresse por quimioterapia, metabolismo de células‑tronco sanguíneas