Clear Sky Science · sv
CTGF-LRP1:s roll i försämrad läkning av kejsarsnittssnitt
Varför kejsarsnittssår ibland inte läker som de ska
När kejsarsnitt blir allt vanligare globalt uppstår en tyst komplikation som påverkar många kvinnor långt efter förlossningen. Vissa kejsarsnittssår i livmodern läker dåligt och lämnar en liten fickliknande defekt i livmoderväggen som kallas en ”nisch”. Denna defekt kan orsaka långvarig blödning, smärta och fertilitetsproblem och kan öka riskerna vid framtida graviditeter. Läkare förstår fortfarande inte fullt ut varför vissa ärr läker väl medan andra inte gör det. Den här studien använder banbrytande enkelcellsanalys och djurexperiment för att kartlägga vad som går fel i den mikroskopiska läkningsmiljön i dessa livmodersår och pekar på nya sätt att förutsäga och möjligen förbättra återhämtningen.
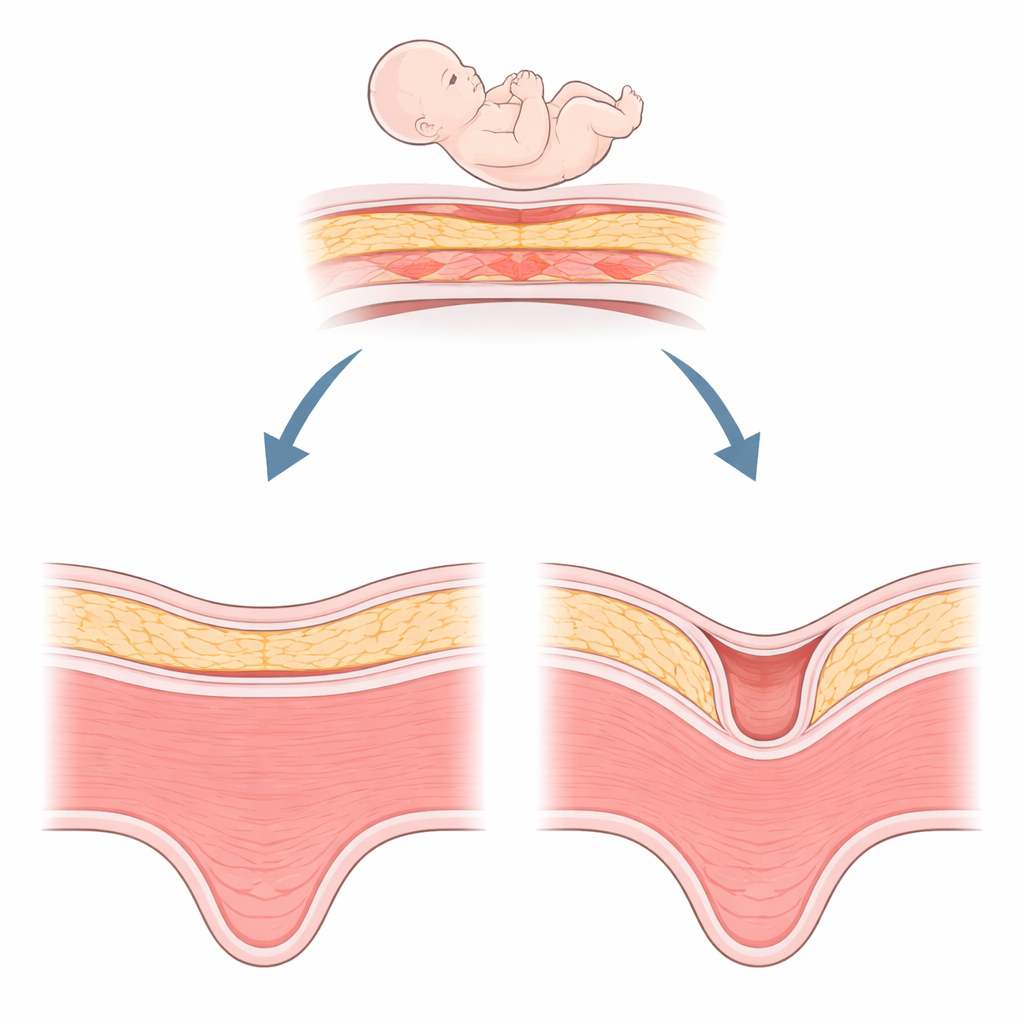
Ett dolt problem efter kejsarsnitt
En nisch är i grunden en inbuktning i livmoderns muskel vid platsen för ett tidigare kejsarsnitt, minst två millimeter djup. Den är förvånansvärt vanlig—ses hos ungefär hälften av kvinnorna efter kejsarsnitt—och upptäckten ökar med bättre ultraljuds- och magnetkameraundersökningar. Kvinnor med en nisch kan märka fläckblödning efter mensen, kronisk bäckensmärta eller svårigheter att bli gravida. I senare graviditeter kan en nisch kopplas till farliga problem såsom onormal moderkaksfäste eller uterusruptur. Kirurger kan försöka trimma och reparera denna defekt, men läkning blir inte alltid tillfredsställande. Detta har lämnat kliniker som söker efter biologiska förklaringar bortom bara kirurgisk teknik.
Zooma in på enskilda celler i ärret
Forskarlaget samlade vävnad från tre områden hos kvinnor som genomgick kirurgi: väl läkta kejsarsnittsärr, dåligt läkt nischvävnad och närliggande till synes normal livmodermuskel. De använde sedan enkelcells-RNA-sekvensering, en teknik som läser vilka gener som är aktiva i tusentals individuella celler, för att kartlägga den cellulära landskapet i dessa regioner. Totalt profilerade de mer än 135 000 celler och identifierade åtta huvudsakliga typer, inklusive glattmuskelceller, immunceller, blodkärlsceller och fibroblaster—bindvävscellerna som bygger upp ett sårs stomme. Jämfört med väl läkta ärr innehöll nischvävnad fler fibroblaster men färre endotelceller, som bekläder blodkärl och hjälper till att samordna vävnadsreparation.
Den saknade signalen mellan kärl och ärrbyggare
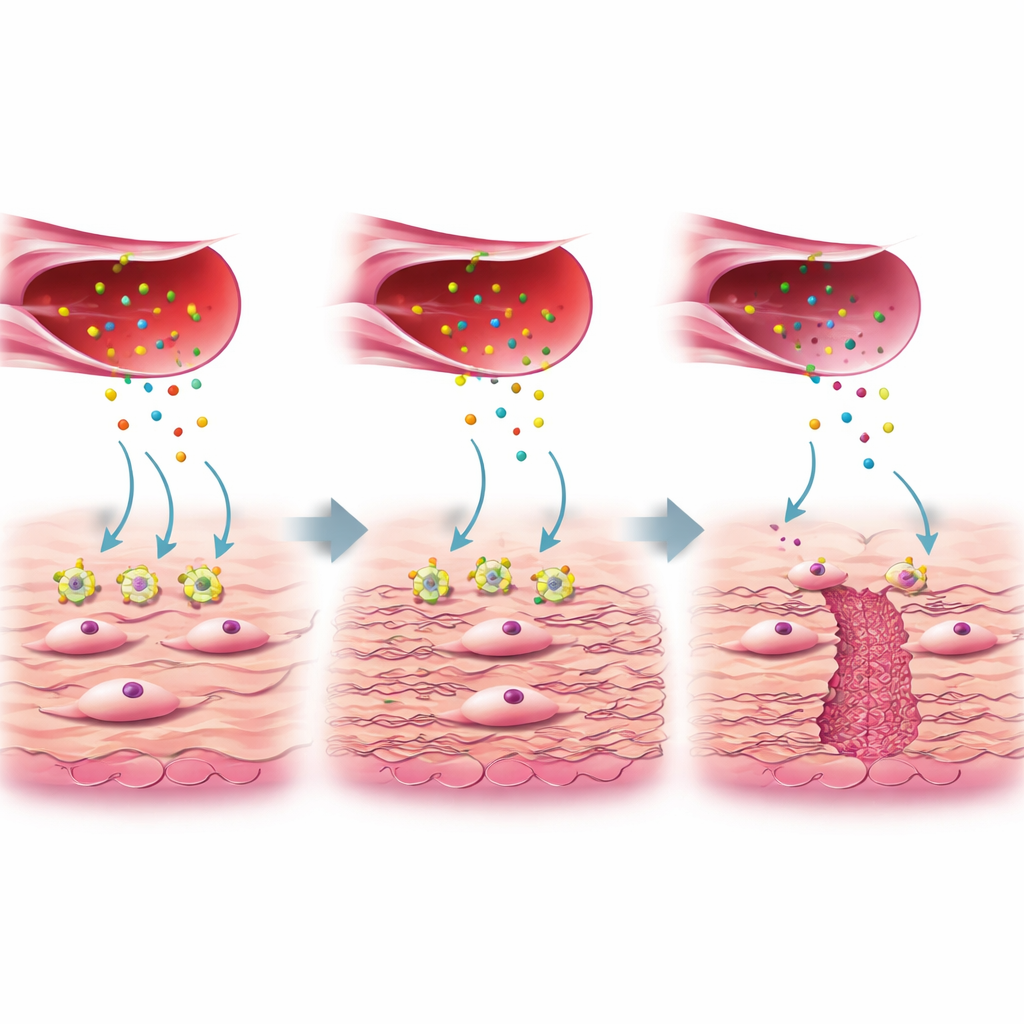
Närmare analys visade att inte alla fibroblaster är lika. En undergrupp, kallad FB3 i studien, visade genaktivitet kopplad till kollagenproduktion och sårläkning och var riklig i väl läkta ärr men minskad i nischvävnad. Dessa hjälpsamma FB3-celler svarar normalt på ett proteinsignal kallat connective tissue growth factor (CTGF), som frisätts av en särskild undergrupp av aktiverade endotelceller. CTGF binder till en receptor på fibroblaster som heter LRP1. Vid sund läkning slår denna CTGF–LRP1-interaktion på interna banor (ERK och WNT) som talar om för fibroblasterna att lägga ned hållbart kollagen och andra komponenter i den extracellulära matrisen, för att fylla igen och stärka livmoderväggen. I nischvävnad var dock LRP1-nivåerna på FB3-fibroblaster markant lägre, även om CTGF-produktionen från blodkärlsceller var likartad. Författarna visade i cellkulturer att när LRP1 var reducerat eller blockerat svarade fibroblasterna inte på CTGF, producerade mindre kollagen och de viktiga reparationsvägarna dämpades.
Från labbet till patienter och djurmodeller
Teamet undrade sedan om detta signalsystem kunde hjälpa till att förutsäga hur väl en kirurgisk reparation skulle läka. I prover från 60 kvinnor som genomgick transvaginal nischreparation hade de som senare fick väl läkta ärr högre nivåer av CTGF och LRP1 än de vars ärr förblev problematiska, och kombinationen av båda markörerna förutsade resultat bäst. För att testa om ökat CTGF kunde underlätta läkning använde forskarna en råttmodell där en kontrollerad skada gjordes i livmodern. Råttor som behandlades med rekombinant mänskligt CTGF utvecklade tjockare muskelager, mindre tät kollagennedslagning och bättre organiserad vävnad runt såret än obehandlade djur. Fibroblaster från dessa råttor producerade också mer kollagen när de exponerades för CTGF—om inte LRP1 experimentellt slogs ned, vilket återigen betonar betydelsen av CTGF–LRP1-partnerskapet.
Vad detta betyder för framtida mödrar
Sammantaget målar fynden upp en bild av nischbildning som ett brott i kommunikationen mellan blodkärl och ärrbyggande celler på mikroskopisk nivå. När fibroblaster saknar tillräckligt med LRP1 kan de inte riktig ”höra” CTGF:s uppmaning att bygga upp igen, vilket lämnar ett svagt, förtunnat område i livmoderväggen istället för ett jämnt, solidt ärr. Detta arbete antyder att mätning av CTGF och LRP1 kring tiden för kejsarsnitt eller nischreparation en dag kan hjälpa läkare att förutsäga vem som riskerar dålig läkning. Det väcker också möjligheten att riktade behandlingar—såsom lokal CTGF-leverans eller läkemedel som säkert stärker de nedströms reparationsbanorna—kan förbättra resultaten. Medan sådana terapier kräver noggranna tester för säkerhet och långtidseffekter erbjuder studien en detaljerad färdplan för att omvandla grundläggande cellulära insikter till bättre vård för kvinnor efter kejsarsnitt.
Citering: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Nyckelord: kejsarsnittsärrdefekt, sårläkning, fibroblaster, växtfaktorsignalering, uterint nisch