Clear Sky Science · pt
Papel do CTGF-LRP1 na cicatrização prejudicada de incisões por cesariana
Por que cicatrizes de cesariana às vezes não cicatrizam corretamente
À medida que os partos por cesariana se tornam mais comuns no mundo, uma complicação silenciosa afeta muitas mulheres muito tempo após o parto. Algumas cicatrizes de cesariana no útero cicatrizam mal, deixando um defeito em forma de bolsa na parede uterina chamado “nicho”. Esse defeito pode causar sangramento prolongado, dor e problemas de fertilidade, além de aumentar riscos em gestações futuras. Ainda assim, os médicos não entendem completamente por que algumas cicatrizes cicatrizam bem enquanto outras não. Este estudo usa análises de célula única de ponta e experimentos animais para descobrir o que dá errado no ambiente microscópico da cicatrização dessas cicatrizes uterinas e aponta novas maneiras de prever e possivelmente melhorar a recuperação.
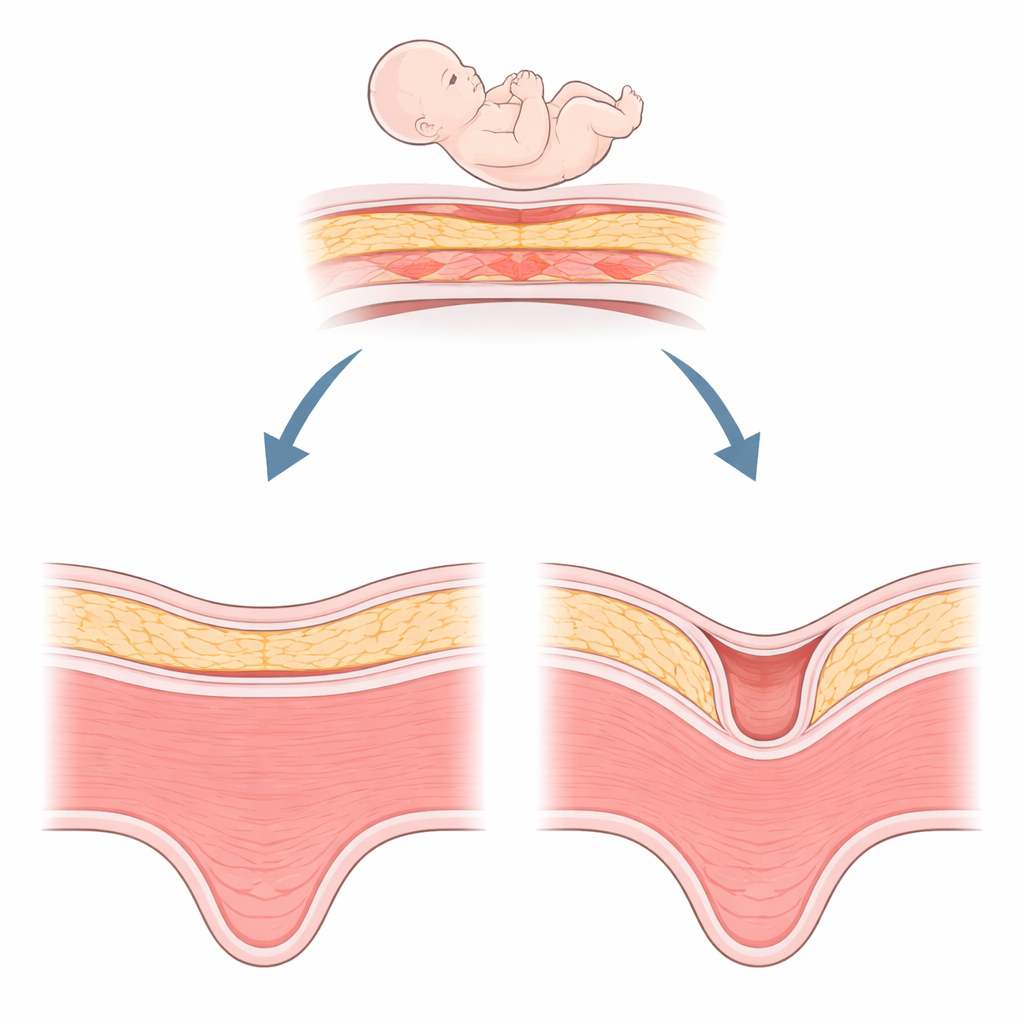
Um problema oculto após o parto por cesariana
Um nicho é essencialmente uma depressão no músculo do útero no local de uma incisão cesariana anterior, com pelo menos dois milímetros de profundidade. É surpreendentemente comum — observado em cerca da metade das mulheres após cesariana — e sua detecção vem aumentando com exames de ultrassom e ressonância magnética mais sensíveis. Mulheres com nicho podem notar spotting após o período menstrual, desconforto pélvico crônico ou dificuldade para engravidar. Em gestações posteriores, um nicho pode estar ligado a problemas perigosos, como implantação placentária anômala ou ruptura uterina. Cirurgiões podem tentar ressecar e reparar esse defeito, mas a cicatrização nem sempre é satisfatória. Isso deixou os clínicos procurando explicações biológicas além da técnica cirúrgica isolada.
Aproximando-se das células individuais na cicatriz
Os pesquisadores coletaram tecido de três áreas em mulheres submetidas à cirurgia: cicatrizes cesarianas bem cicatrizadas, tecido de nicho mal cicatrizado e músculo uterino aparentemente normal nas proximidades. Em seguida, usaram sequenciamento de RNA de célula única, uma tecnologia que lê quais genes estão ativos em milhares de células individuais, para mapear a paisagem celular dessas regiões. No total, perfilaram mais de 135.000 células e identificaram oito tipos principais, incluindo células musculares lisas, células imunes, células vasculares e fibroblastos — as células do tecido conjuntivo que constroem a estrutura de uma cicatriz. Em comparação com cicatrizes bem cicatrizadas, o tecido de nicho continha mais fibroblastos, mas menos células endoteliais, que revestem os vasos sanguíneos e ajudam a coordenar a reparação tecidual.
O sinal ausente entre vasos e construtores da cicatriz
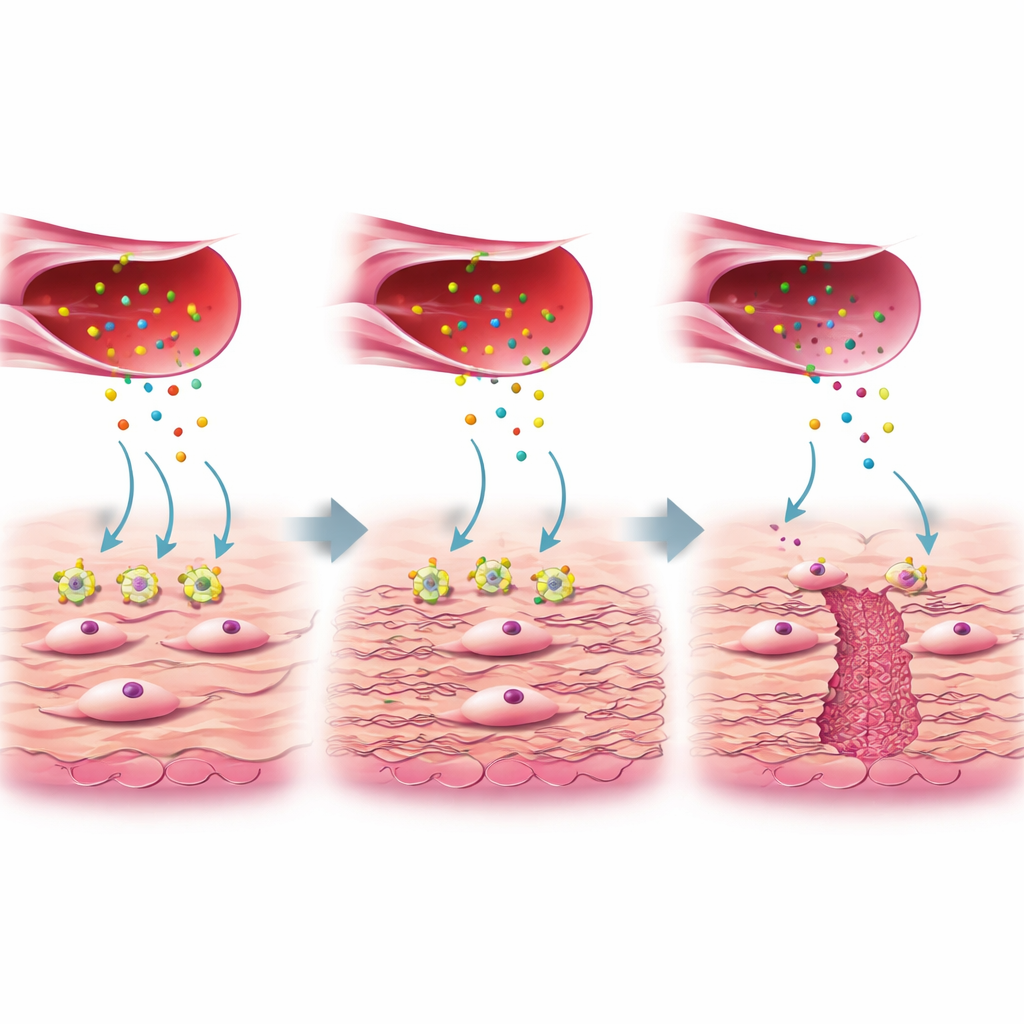
Um exame mais atento revelou que nem todos os fibroblastos são iguais. Um subgrupo, chamado FB3 no estudo, mostrou atividade gênica ligada à produção de colágeno e cicatrização e era abundante em cicatrizes bem cicatrizadas, mas reduzido no tecido de nicho. Essas células FB3 úteis normalmente respondem a um sinal proteico chamado fator de crescimento do tecido conjuntivo (CTGF), que é liberado por um subgrupo especial de células endoteliais ativadas. O CTGF se liga a um receptor nos fibroblastos chamado LRP1. Na cicatrização saudável, essa interação CTGF–LRP1 ativa vias internas (ERK e WNT) que dizem aos fibroblastos para depositarem colágeno resistente e outros componentes da matriz extracelular, preenchendo e reforçando a parede uterina. No tecido de nicho, entretanto, os níveis de LRP1 nos fibroblastos FB3 estavam marcadamente mais baixos, embora a produção de CTGF pelas células vasculares fosse semelhante. Os autores mostraram em culturas celulares que quando o LRP1 foi reduzido ou bloqueado, os fibroblastos deixaram de responder ao CTGF, produziram menos colágeno e as principais vias de reparo foram atenuadas.
Do banco de laboratório para pacientes e modelos animais
A equipe então perguntou se esse par de sinalização poderia ajudar a prever quão bem uma reparação cirúrgica iria cicatrizar. Em amostras de 60 mulheres que passaram por reparo transvaginal de nicho, aquelas cujas cicatrizes cicatrizaram bem depois apresentaram níveis mais altos de CTGF e LRP1 do que aquelas cujas cicatrizes permaneceram problemáticas, e a combinação de ambos os marcadores foi a melhor preditora do desfecho. Para testar se aumentar o CTGF poderia ajudar a cicatrização, os pesquisadores usaram um modelo em ratos no qual foi feita uma lesão controlada no útero. Ratos tratados com CTGF humano recombinante desenvolveram camadas musculares mais espessas, cicatrizes de colágeno menos densas e tecido melhor organizado ao redor da ferida do que animais não tratados. Fibroblastos desses ratos também produziram mais colágeno quando expostos ao CTGF — a menos que o LRP1 fosse experimentalmente reduzido, o que novamente sublinha a importância da parceria CTGF–LRP1.
O que isso significa para futuras mães
Em conjunto, os achados desenham um quadro da formação de nicho como uma falha na comunicação entre vasos sanguíneos e células construtoras da cicatriz no nível microscópico. Quando os fibroblastos não têm LRP1 suficiente, eles não conseguem “ouvir” corretamente o chamado do CTGF para reconstruir, deixando uma área fraca e afinada na parede uterina em vez de uma cicatriz lisa e sólida. Este trabalho sugere que medir CTGF e LRP1 ao redor do momento da cesariana ou do reparo do nicho poderia, um dia, ajudar os médicos a prever quem está em risco de má cicatrização. Também levanta a possibilidade de tratamentos direcionados — como entrega local de CTGF ou fármacos que aumentem com segurança as vias de reparo a jusante — que poderiam melhorar os resultados. Embora tais terapias exijam testes cuidadosos de segurança e efeitos a longo prazo, o estudo oferece um roteiro detalhado para converter insights celulares básicos em cuidados melhores para mulheres após o parto por cesariana.
Citação: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Palavras-chave: defeito de cicatriz de cesariana, cicatrização de feridas, fibroblastos, sinalização de fatores de crescimento, nicho uterino