Clear Sky Science · pl
Rola CTGF‑LRP1 w zaburzonym gojeniu nacięć po cięciu cesarskim
Dlaczego blizny po cięciu cesarskim czasem nie goją się prawidłowo
W miarę jak porody przez cesarskie cięcie stają się coraz bardziej powszechne na świecie, ciche powikłanie dotyka wiele kobiet długo po porodzie. Niektóre blizny w macicy goją się źle, pozostawiając mały, kieszonkowaty ubytek w ścianie macicy zwany „niche”. Ten defekt może powodować przedłużone krwawienia, ból i problemy z płodnością, a także zwiększać ryzyko w kolejnych ciążach. Mimo to lekarze wciąż nie rozumieją w pełni, dlaczego jedne blizny goją się dobrze, a inne nie. W tym badaniu zastosowano zaawansowaną analizę pojedynczych komórek i eksperymenty na zwierzętach, aby odkryć, co idzie nie tak w mikroskopijnym środowisku gojenia tych blizn i wskazać nowe sposoby przewidywania oraz ewentualnego poprawiania procesu rekonwalescencji.
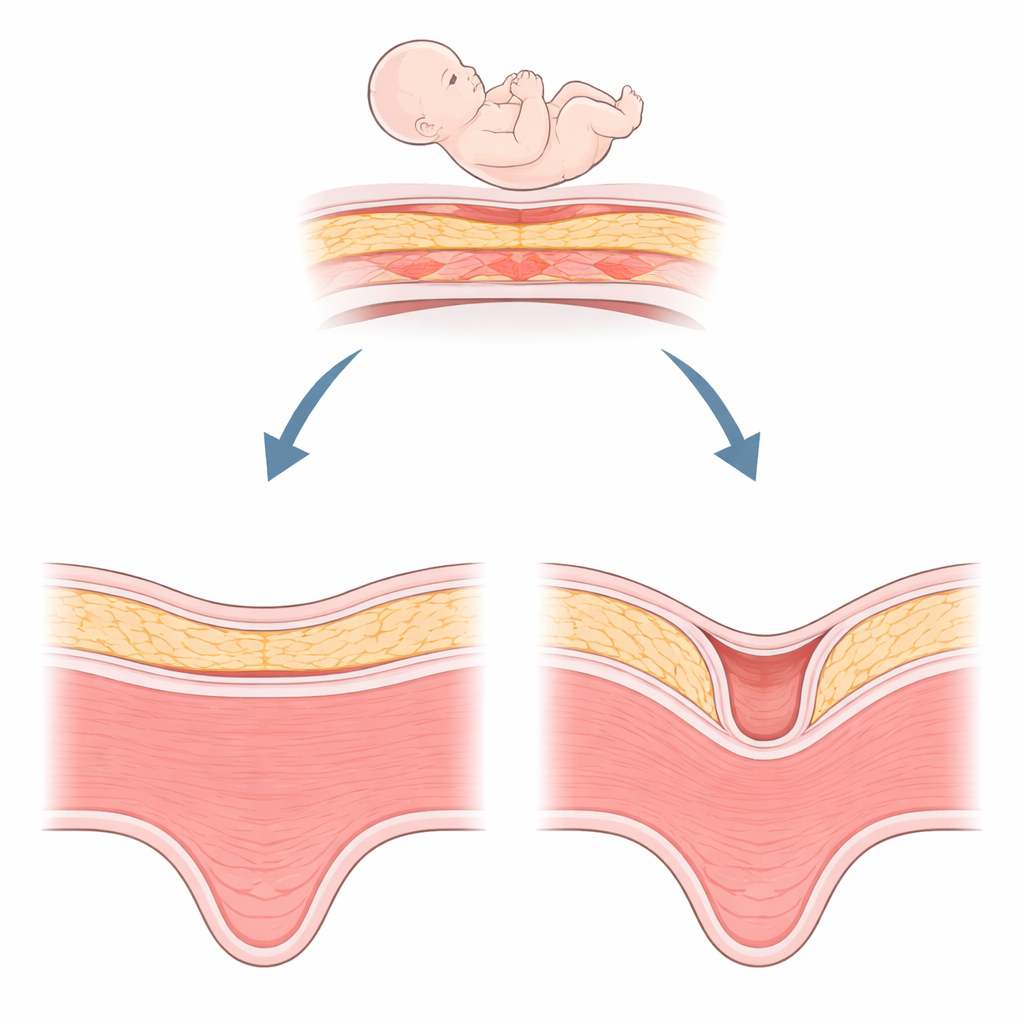
Ukryty problem po porodzie przez cesarskie cięcie
Niche to w istocie zagłębienie w mięśniu macicy w miejscu poprzedniego nacięcia cesarskiego, o głębokości co najmniej dwóch milimetrów. Jest zaskakująco powszechne — obserwuje się je u około połowy kobiet po cięciu cesarskim — a wykrywalność rośnie dzięki lepszym badaniom ultrasonograficznym i rezonansowi magnetycznemu. Kobiety z niche mogą zauważyć plamienie po miesiączce, przewlekły ból miednicy lub trudności z zajściem w ciążę. W późniejszych ciążach obecność niche może wiązać się z niebezpiecznymi komplikacjami, takimi jak nieprawidłowe przyczepienie łożyska lub pęknięcie macicy. Chirurdzy mogą próbować przyciąć i naprawić ten defekt, ale gojenie nie zawsze jest zadowalające. To skłoniło klinicystów do poszukiwania wyjaśnień biologicznych wykraczających poza samą technikę chirurgiczną.
Przyjrzenie się pojedynczym komórkom blizny
Naukowcy pobrali tkankę z trzech obszarów u kobiet poddawanych operacji: dobrze zagojonych blizn po cięciu cesarskim, źle zagojonej tkanki niche oraz pobliskiego pozornie prawidłowego mięśnia macicy. Następnie zastosowali sekwencjonowanie RNA pojedynczych komórek, technologię odczytującą, które geny są aktywne w tysiącach poszczególnych komórek, aby zmapować krajobraz komórkowy tych regionów. W sumie scharakteryzowali ponad 135 000 komórek i zidentyfikowali osiem głównych typów, w tym komórki mięśni gładkich, komórki układu odpornościowego, komórki naczyń krwionośnych oraz fibroblasty — komórki tkanki łącznej, które budują rusztowanie blizny. W porównaniu z dobrze zagojonymi bliznami, tkanka niche zawierała więcej fibroblastów, lecz mniej komórek śródbłonka, które wyściełają naczynia krwionośne i koordynują naprawę tkanek.
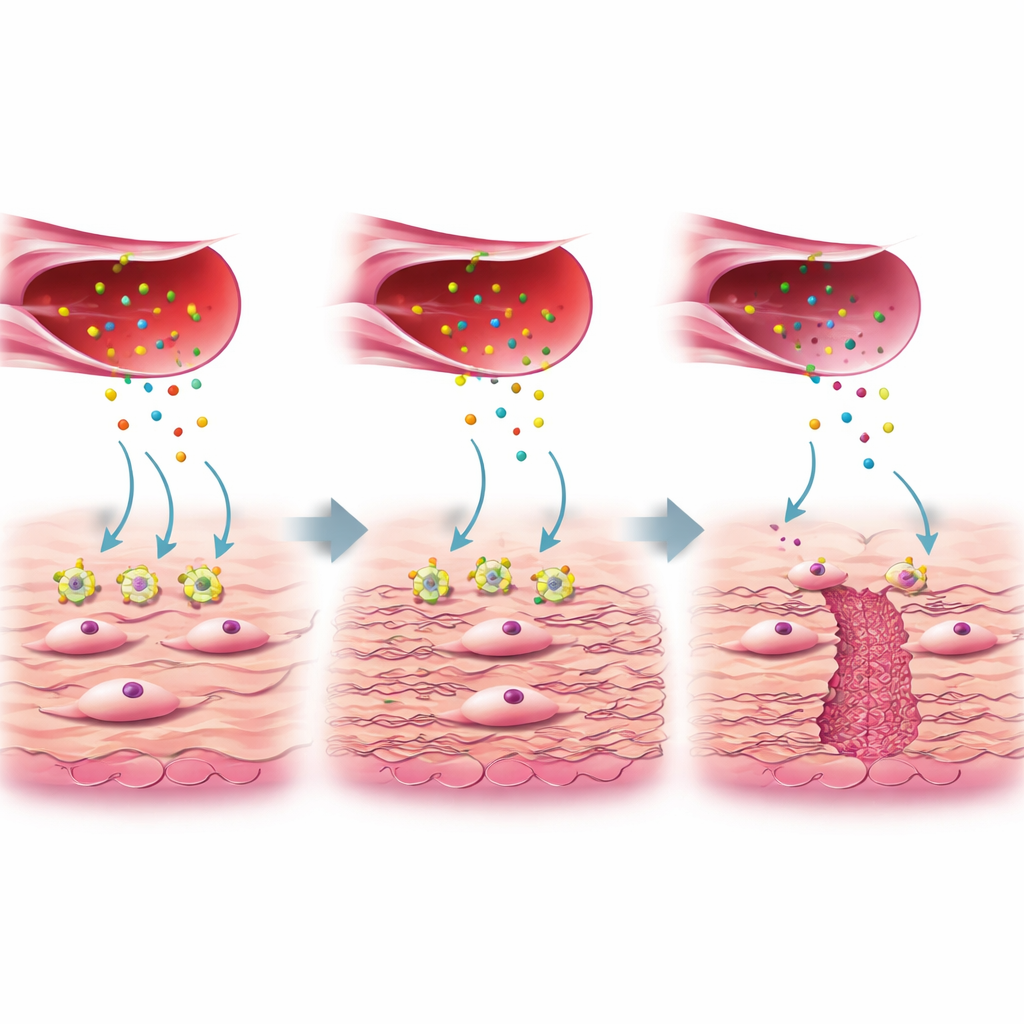
Brakujący sygnał między naczyniami a twórcami blizny
Bliższa analiza ujawniła, że nie wszystkie fibroblasty są takie same. Jedna podgrupa, oznaczona w badaniu jako FB3, wykazywała aktywność genów związaną z produkcją kolagenu i gojeniem ran i była obfita w dobrze zagojonych bliznach, lecz zmniejszona w tkance niche. Te pożyteczne komórki FB3 normalnie reagują na białkowy sygnał zwany czynnikiem wzrostu tkanki łącznej (CTGF), uwalniany przez specjalną podgrupę aktywowanych komórek śródbłonka. CTGF wiąże się z receptorem na fibroblastach nazwanym LRP1. W zdrowym gojeniu to oddziaływanie CTGF–LRP1 włącza wewnętrzne szlaki (ERK i WNT), które nakazują fibroblastom odkładać wytrzymały kolagen i inne składniki macierzy zewnątrzkomórkowej, wypełniając i wzmacniając ścianę macicy. W tkance niche poziomy LRP1 na fibroblastach FB3 były wyraźnie niższe, mimo że produkcja CTGF przez komórki naczyniowe była podobna. Autorzy wykazali w hodowlach komórkowych, że gdy LRP1 było zmniejszone lub zablokowane, fibroblasty nie reagowały na CTGF, produkowały mniej kolagenu, a kluczowe szlaki naprawcze były stłumione.
Od laboratorium do pacjentek i modeli zwierzęcych
Zespół zapytał następnie, czy ta para sygnałowa może pomóc przewidzieć, jak dobrze zagoi się naprawa chirurgiczna. W próbkach od 60 kobiet, które przeszły przezpochwową naprawę niche, te, których blizny później dobrze się zagoiły, miały wyższe poziomy CTGF i LRP1 niż kobiety, u których blizny pozostały problematyczne; kombinacja obu markerów najlepiej przewidywała wynik. Aby sprawdzić, czy wzmocnienie CTGF może sprzyjać gojeniu, badacze użyli modelu szczura, w którym wykonano kontrolowane uszkodzenie macicy. Szczury leczone rekombinowanym ludzkim CTGF rozwinęły grubsze warstwy mięśniowe, mniej gęste bliznowacenie kolagenowe i lepiej zorganizowaną tkankę wokół rany niż zwierzęta nieleczone. Fibroblasty z tych szczurów także produkowały więcej kolagenu po ekspozycji na CTGF — chyba że LRP1 zostało eksperymentalnie wyciszone, co ponownie podkreśla znaczenie partnerstwa CTGF–LRP1.
Co to znaczy dla przyszłych matek
Podsumowując, wyniki kreślą obraz formowania się niche jako załamania komunikacji między naczyniami krwionośnymi a komórkami budującymi bliznę na poziomie mikroskopowym. Gdy fibroblasty mają zbyt mało LRP1, nie potrafią właściwie „usłyszeć” sygnału CTGF, by odbudować tkankę, pozostawiając słaby, przerzedzony odcinek ściany macicy zamiast gładkiej, zwartej blizny. Praca ta sugeruje, że pomiar CTGF i LRP1 w okresie cięcia cesarskiego lub naprawy niche mógłby kiedyś pomóc lekarzom przewidzieć, kto jest zagrożony złym gojeniem. Otwartą pozostaje także możliwość zastosowania terapii ukierunkowanych — takich jak miejscowe podanie CTGF lub leki bezpiecznie pobudzające szlaki naprawcze — które mogłyby poprawić wyniki. Choć takie terapie wymagają ostrożnego badania pod kątem bezpieczeństwa i długoterminowych skutków, badanie daje szczegółową mapę, jak przekształcić podstawowe odkrycia komórkowe w lepszą opiekę dla kobiet po porodzie przez cesarskie cięcie.
Cytowanie: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Słowa kluczowe: defekt blizny po cesarskim cięciu, gojenie ran, fibroblasty, sygnalizacja czynników wzrostu, niche macicy