Clear Sky Science · de
Rolle von CTGF-LRP1 bei gestörtem Heilungsverlauf von Kaiserschnittnarben
Warum Kaiserschnittnarben manchmal nicht richtig verheilen
Da Kaiserschnittgeburten weltweit zunehmen, betrifft eine stille Komplikation viele Frauen lange nach der Entbindung. Manche Kaiserschnittnarben in der Gebärmutter heilen schlecht und hinterlassen eine kleine taschenartige Aussparung in der Gebärmutterwand, eine sogenannte „Nische“. Dieser Defekt kann zu lang anhaltenden Blutungen, Schmerzen und Fruchtbarkeitsproblemen führen und das Risiko in späteren Schwangerschaften erhöhen. Dennoch verstehen Ärztinnen und Ärzte noch nicht vollständig, warum einige Narben gut heilen, andere nicht. Diese Studie nutzt moderne Einzelzellanalysen und Tierexperimente, um aufzudecken, was in der mikroskopischen Heilungsumgebung dieser Gebärmutternarben schiefgeht, und weist auf neue Möglichkeiten hin, den Heilungsverlauf vorherzusagen und möglicherweise zu verbessern.
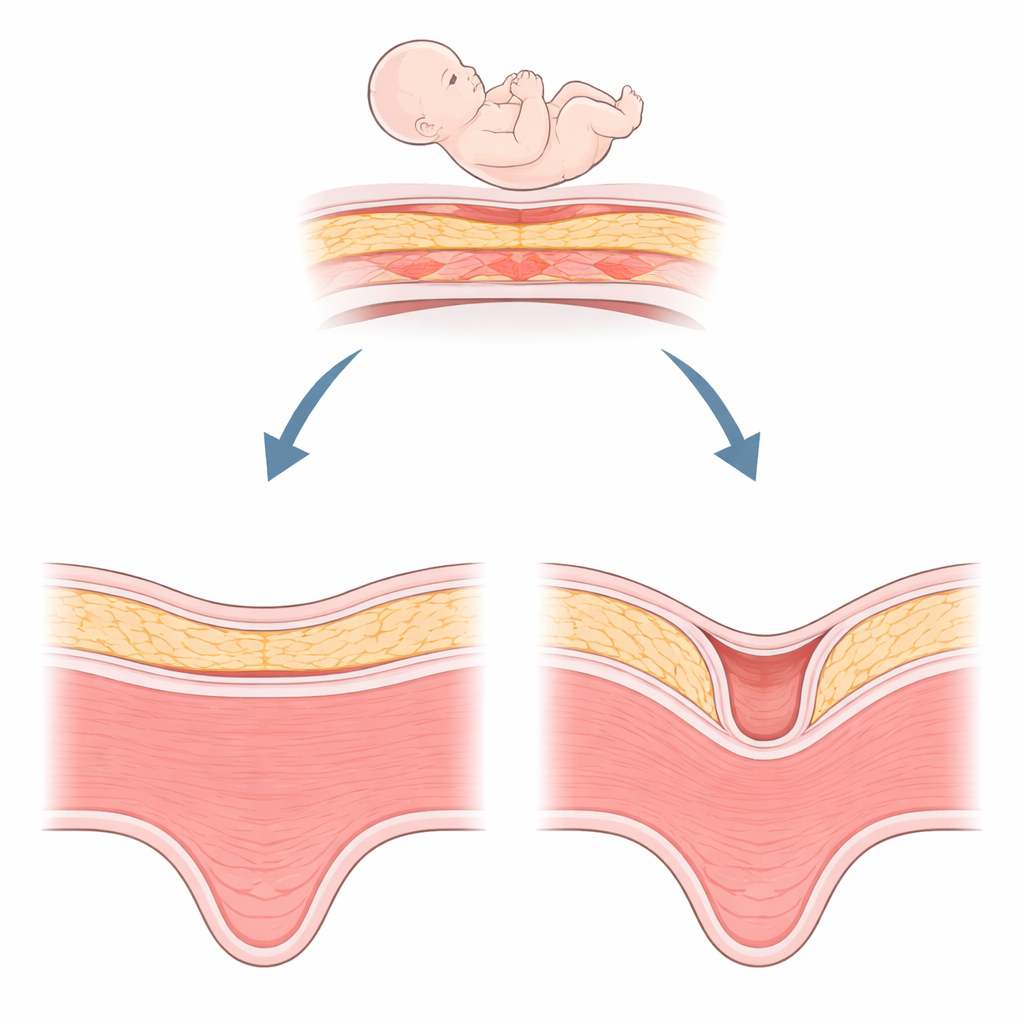
Ein verborgenes Problem nach dem Kaiserschnitt
Eine Nische ist im Grunde eine Vertiefung in der Muskelschicht der Gebärmutter an der Stelle eines früheren Kaiserschnittschnitts, mindestens zwei Millimeter tief. Sie ist überraschend häufig — bei etwa der Hälfte der Frauen nach einem Kaiserschnitt zu sehen — und wird durch bessere Ultraschall- und MRT-Bildgebung zunehmend entdeckt. Frauen mit einer Nische bemerken möglicherweise Schmierblutungen nach der Periode, chronische Beckenschmerzen oder Schwierigkeiten, schwanger zu werden. In späteren Schwangerschaften kann eine Nische mit gefährlichen Problemen wie abnormer Plazentahaftung oder Uterusruptur verbunden sein. Chirurgen können versuchen, diesen Defekt auszuschneiden und zu reparieren, doch die Heilung ist nicht immer zufriedenstellend. Das hat Klinikerinnen und Kliniker dazu veranlasst, nach biologischen Erklärungen jenseits der chirurgischen Technik zu suchen.
Ein Blick auf einzelne Zellen in der Narbe
Die Forschenden entnahmen Gewebe aus drei Bereichen bei Frauen, die sich einer Operation unterzogen: gut verheilte Kaiserschnittnarben, schlecht verheilte Nischentissue und nahegelegenes offenbar normales Myometrium. Anschließend verwendeten sie Einzelzell-RNA-Sequenzierung, eine Technologie, die abliest, welche Gene in Tausenden einzelner Zellen aktiv sind, um die zelluläre Landschaft dieser Regionen zu kartieren. Insgesamt profilierten sie mehr als 135.000 Zellen und identifizierten acht Haupttypen, darunter glatte Muskelzellen, Immunzellen, Gefäßzellen und Fibroblasten — die Bindegewebszellen, die das Gerüst einer Narbe aufbauen. Im Vergleich zu gut verheilten Narben enthielt das Nischengewebe mehr Fibroblasten, aber weniger Endothelzellen, die Blutgefäße auskleiden und die Gewebereparatur koordinieren.
Das fehlende Signal zwischen Gefäßen und Narbenbildnern
Ein genauerer Blick zeigte, dass nicht alle Fibroblasten gleich sind. Eine Untergruppe, im Papier FB3 genannt, zeigte Genaktivität, die mit Kollagenproduktion und Wundheilung verknüpft ist, und war in gut verheilten Narben reichlich vorhanden, aber im Nischengewebe reduziert. Diese hilfreichen FB3-Zellen reagieren normalerweise auf ein Proteinsignal namens connective tissue growth factor (CTGF), das von einer speziellen Untergruppe aktivierter Endothelzellen freigesetzt wird. CTGF bindet an einen Rezeptor auf Fibroblasten namens LRP1. In gesunder Heilung schaltet diese CTGF–LRP1-Interaktion interne Signalwege (ERK und WNT) an, die den Fibroblasten sagen, stabiles Kollagen und andere Bestandteile der extrazellulären Matrix abzuschichten und so die Gebärmutterwand aufzufüllen und zu stärken. Im Nischengewebe waren dagegen die LRP1-Spiegel auf FB3-Fibroblasten deutlich reduziert, obwohl die CTGF-Produktion durch Gefäßzellen ähnlich war. Die Autorinnen und Autoren zeigten in Zellkulturen, dass bei reduziertem oder blockiertem LRP1 die Fibroblasten nicht auf CTGF reagierten, weniger Kollagen produzierten und die wichtigen Reparaturwege abgeschwächt waren.
Vom Labor zur Patientin und ins Tiermodell
Das Team fragte dann, ob dieses Signalpaar helfen könnte vorherzusagen, wie gut eine chirurgische Reparatur heilt. In Proben von 60 Frauen, die sich einer transvaginalen Nischenreparatur unterzogen hatten, wiesen jene, deren Narben später gut verheilt waren, höhere CTGF- und LRP1-Spiegel auf als jene, bei denen die Narben problematisch blieben; die Kombination beider Marker sagte das Ergebnis am besten voraus. Um zu testen, ob eine Aufstockung von CTGF die Heilung unterstützen könnte, verwendeten die Forschenden ein Rattenmodell, in dem eine kontrollierte Verletzung in der Gebärmutter gesetzt wurde. Ratten, die mit rekombinantem humanem CTGF behandelt wurden, entwickelten dickere Muskelschichten, weniger dichte Kollagennarben und besser organisiertes Gewebe um die Wunde als unbehandelte Tiere. Fibroblasten aus diesen Ratten produzierten ebenfalls mehr Kollagen bei CTGF-Exposition — es sei denn, LRP1 wurde experimentell herunterreguliert, was erneut die Bedeutung der CTGF–LRP1-Partnerschaft unterstreicht.
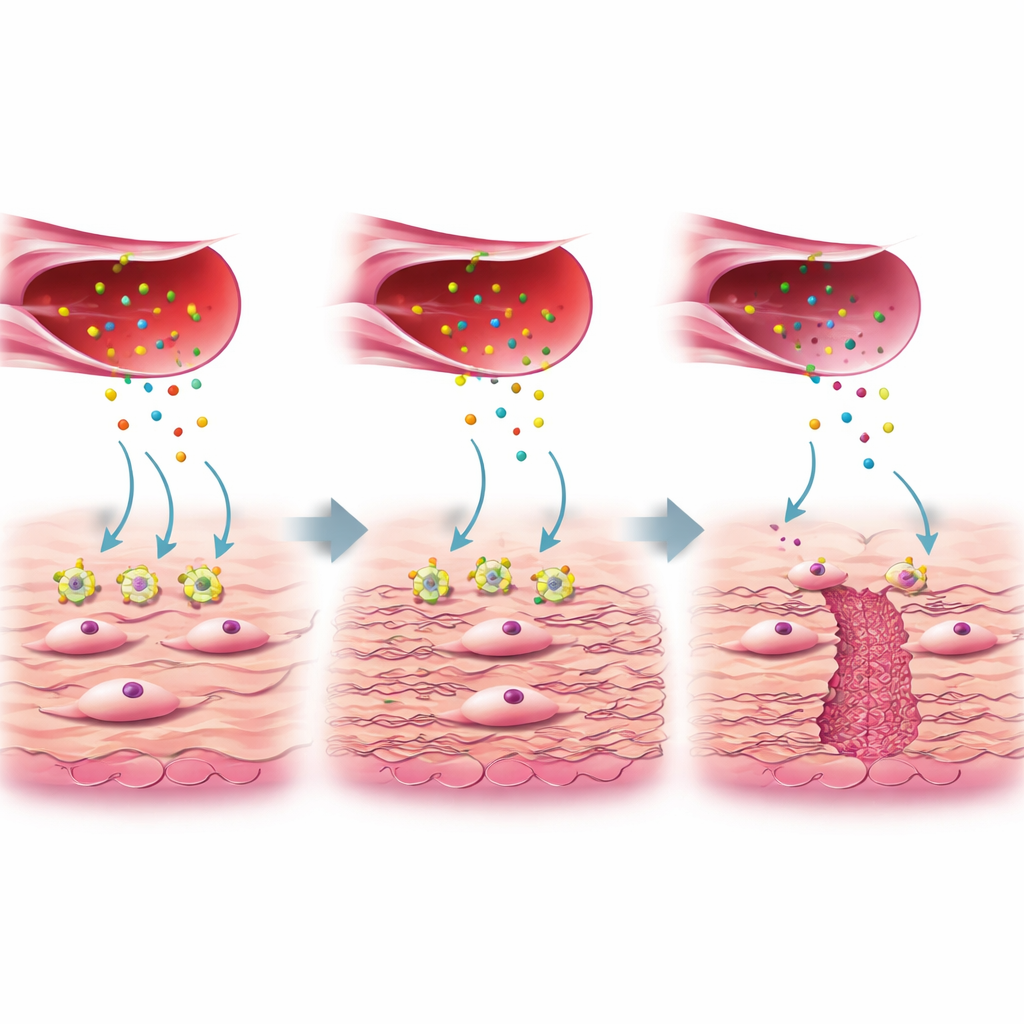
Was das für künftige Mütter bedeutet
In der Summe zeichnen die Ergebnisse das Bild, dass Nischenbildung eine Störung der Kommunikation zwischen Blutgefäßen und narbenbildenden Zellen auf mikroskopischer Ebene ist. Wenn Fibroblasten nicht genügend LRP1 besitzen, können sie CTGF nicht richtig „hören“ und werden nicht zum Wiederaufbau angeregt, wodurch statt einer glatten, stabilen Narbe ein schwacher, ausgedünnter Bereich in der Gebärmutterwand zurückbleibt. Die Arbeit legt nahe, dass das Messen von CTGF und LRP1 rund um den Kaiserschnitt oder die Nischenreparatur eines Tages Ärztinnen und Ärzten helfen könnte, vorherzusagen, wer ein Risiko für schlechte Heilung hat. Sie öffnet auch die Möglichkeit gezielter Behandlungen — etwa lokale CTGF-Gabe oder Medikamente, die die nachgeschalteten Reparaturwege sicher verstärken — die die Ergebnisse verbessern könnten. Solche Therapien müssen zwar sorgfältig auf Sicherheit und Langzeitfolgen geprüft werden, doch die Studie bietet eine detaillierte Landkarte, wie grundlegende zelluläre Einsichten in bessere Versorgung für Frauen nach Kaiserschnittgeburten verwandelt werden können.
Zitation: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Schlüsselwörter: Kaiserschnittnarbe Defekt, Wundheilung, Fibroblasten, Wachstumsfaktorsignalgebung, Uterusnische