Clear Sky Science · ru
Роль CTGF‑LRP1 при нарушенном заживлении разрезов кесарева сечения
Почему рубцы после кесарева сечения иногда заживают неправильно
По мере того как кесарево сечение становится всё более распространённым во всём мире, одно малозаметное осложнение затрагивает многих женщин задолго после родов. Некоторые рубцы на матке заживают плохо, образуя небольшую мешковидную впадину в стенке матки, называемую «нишой». Этот дефект может вызывать длительные кровянистые выделения, боль и проблемы с фертильностью, а также повышать риски при последующих беременностях. Тем не менее врачи до сих пор не полностью понимают, почему одни рубцы заживают хорошо, а другие — нет. В этом исследовании применены передовые методы одноклеточного анализа и эксперименты на животных, чтобы выяснить, что идёт не так в микросреде заживления таких маточных рубцов, и наметить новые способы прогнозирования и возможного улучшения восстановления.
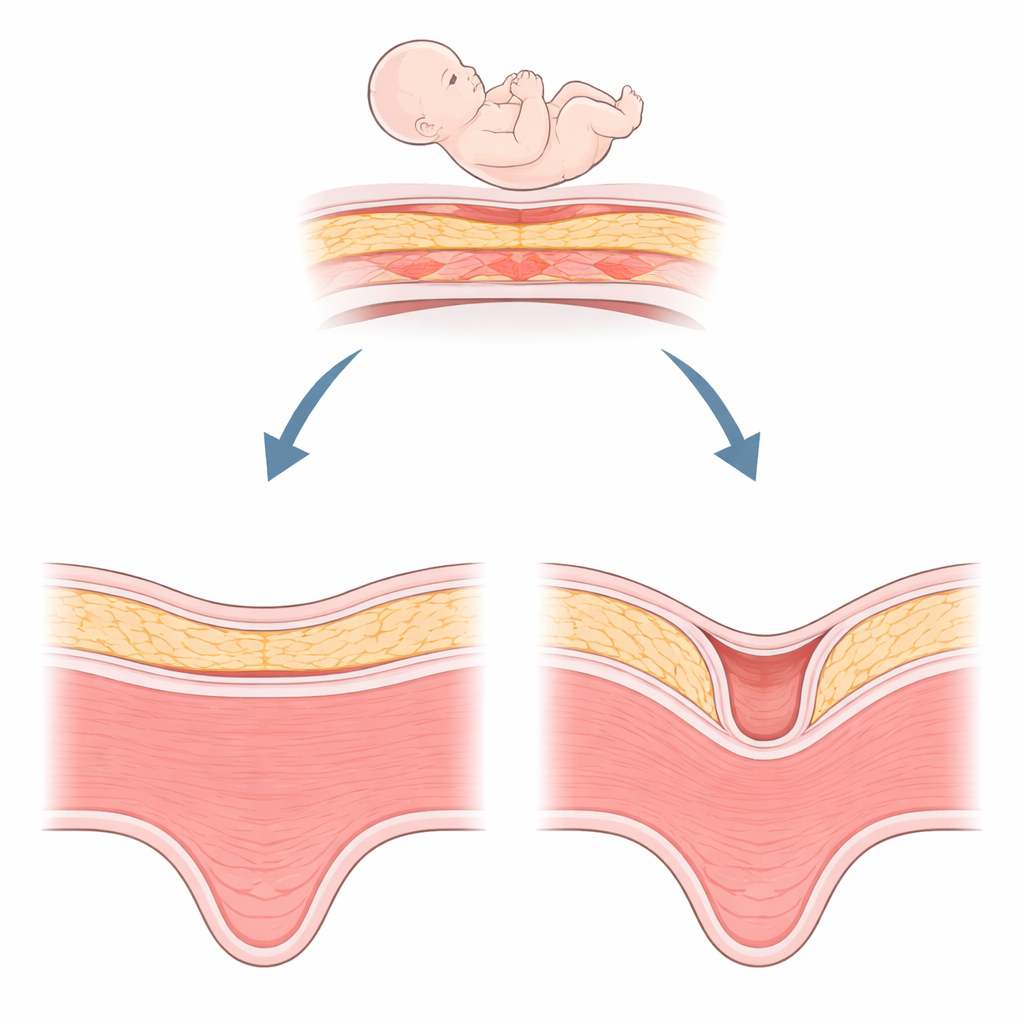
Скрытая проблема после кесарева сечения
Ниша по сути представляет собой вмятину в мышце матки в месте предыдущего разреза, глубиной не менее двух миллиметров. Это оказалось удивительно широко распространённым явлением — примерно у половины женщин после кесарева сечения — и благодаря улучшению УЗИ и МРТ такие дефекты выявляются всё чаще. Женщины с нишей могут замечать мазню между менструациями, хронический тазовый дискомфорт или трудности с зачатием. В последующих беременностях ниша ассоциируется с опасными осложнениями, такими как аномальное прикрепление плаценты или разрыв матки. Хирурги могут попытаться иссечь и восстановить этот дефект, но заживление не всегда оказывается удовлетворительным. Это побуждает клиницистов искать биологические объяснения, выходящие за рамки только хирургической техники.
Приближение к отдельным клеткам рубца
Исследователи взяли образцы ткани из трёх областей у женщин, которым проводилась операция: хорошо зажившие рубцы после кесарева сечения, плохо зажившая ткань ниши и соседняя, по виду нормальная маточная мышца. Затем они использовали одноклеточный секвенирование РНК — технологию, позволяющую прочитать, какие гены активны в тысячах отдельных клеток — чтобы сопоставить клеточный ландшафт этих зон. В сумме профилировано более 135 000 клеток, и выделено восемь основных типов, включая гладкомышечные клетки, иммунные клетки, клетки кровеносных сосудов и фибробласты — соединительнотканные клетки, которые формируют каркас рубца. По сравнению с хорошо зажившими рубцами, в ткани ниши было больше фибробластов, но меньше эндотелиальных клеток, выстилающих сосуды и помогающих координировать восстановление ткани.
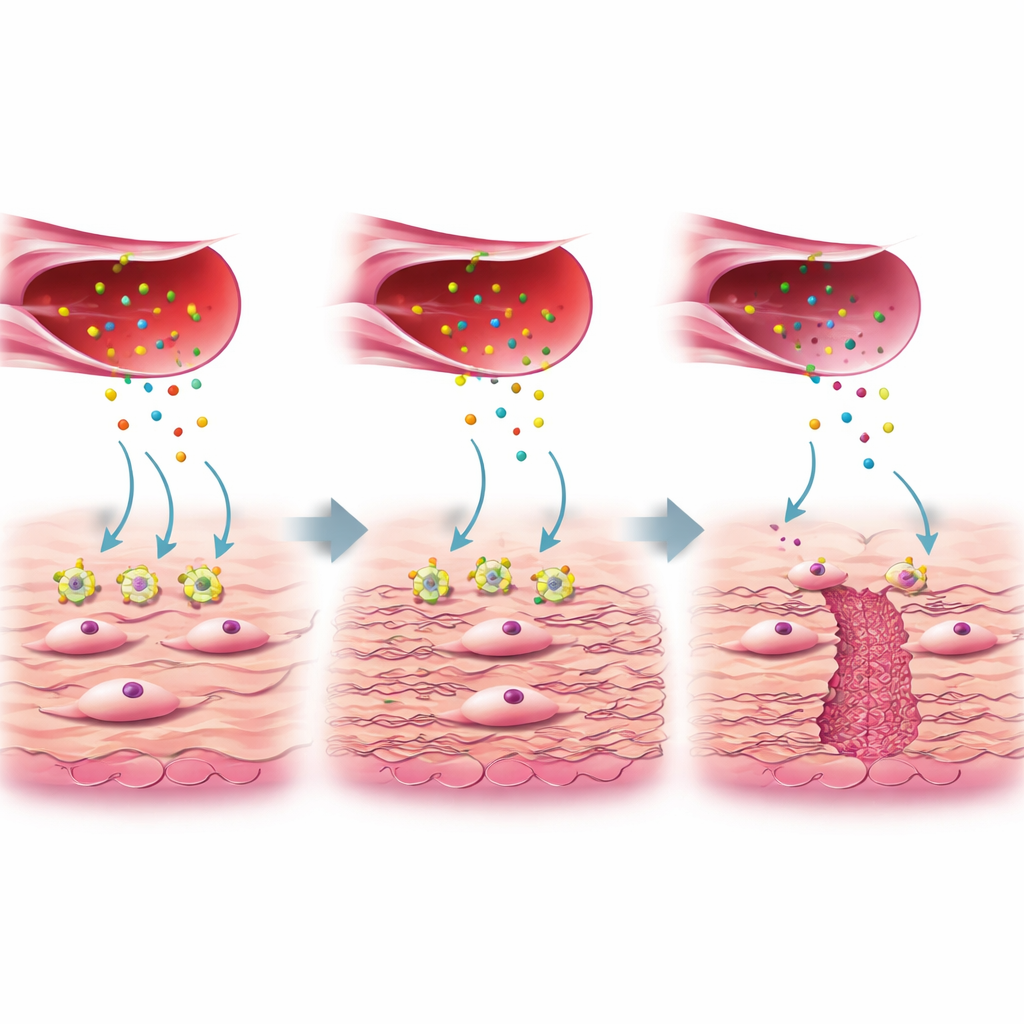
Пропавший сигнал между сосудами и «строителями» рубца
Более детальный анализ показал, что фибробласты неоднородны. Одна подгруппа, обозначенная в исследовании как FB3, проявляла активность генов, связанную с продукцией коллагена и заживлением ран, и была богата в хорошо заживших рубцах, но снижена в ткани ниши. Эти полезные клетки FB3 обычно реагируют на белок-сигнал — фактор соединительной ткани (CTGF), который выделяют специальная подгруппа активированных эндотелиальных клеток. CTGF связывается с рецептором на фибробластах, называемым LRP1. При нормальном заживлении взаимодействие CTGF–LRP1 включает внутриклеточные пути (ERK и WNT), которые заставляют фибробласты синтезировать прочный коллаген и другие компоненты внеклеточного матрикса, заполняя и укрепляя стенку матки. В ткани ниши, однако, уровень LRP1 на фибробластах FB3 был заметно ниже, хотя производство CTGF клетками сосудов оставалось сопоставимым. Авторы показали в клеточных культурах, что при снижении или блокировке LRP1 фибробласты не реагировали на CTGF, продуцировали меньше коллагена, и ключевые пути восстановления были подавлены.
От лабораторного стола к пациенткам и моделям на животных
Затем команда проверила, может ли эта парная сигнализация помочь предсказать, насколько успешно заживёт хирургическая коррекция. В образцах от 60 женщин, перенёсших трансвагинальную операцию по восстановлению ниши, у тех, чьи рубцы впоследствии зажили хорошо, уровни CTGF и LRP1 были выше, чем у женщин с сохраняющимися проблемами, а сочетание обоих маркеров давало наилучший прогноз. Чтобы проверить, может ли усиление CTGF улучшить заживление, исследователи использовали модель у крыс с контролируемым повреждением матки. Крысы, получавшие рекомбинантный человеческий CTGF, развивали более толстые мышечные слои, менее плотные коллагеновые спайки и более организованную ткань вокруг раны по сравнению с нечувствительными животными. Фибробласты этих крыс также производили больше коллагена при воздействии CTGF — если только LRP1 не был экспериментально подавлен, что снова подчёркивает важность взаимодействия CTGF–LRP1.
Что это означает для будущих мам
В совокупности результаты показывают нишу как сбой в коммуникации между кровеносными сосудами и клетками, строящими рубец, на микроскопическом уровне. Когда фибробластам не хватает LRP1, они не в состоянии «услышать» сигнал CTGF и правильно перестроить ткань, в результате в стенке матки остаётся слабая, истончённая зона вместо гладкого плотного рубца. Это исследование указывает на то, что измерение CTGF и LRP1 вблизи времени кесарева сечения или восстановления ниши в будущем может помочь врачам предсказывать риск плохого заживления. Также открывается перспектива целевых вмешательств — например локальной доставки CTGF или препаратов, безопасно усиливающих нисходящие пути восстановления — которые могли бы улучшить исходы. Хотя такие терапии потребуют тщательной проверки на предмет безопасности и долгосрочных эффектов, работа даёт детальную дорожную карту для переноса фундаментальных клеточных открытий в лучшую помощь женщинам после кесарева сечения.
Цитирование: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Ключевые слова: дефект рубца после кесарева сечения, заживление ран, фибробласты, сигналы факторов роста, маточная ниша