Clear Sky Science · nl
Rol van CTGF-LRP1 bij verstoorde genezing van keizersnede- incisies
Waarom keizersnede-littekens soms niet goed genezen
Naarmate keizersneden wereldwijd vaker voorkomen, treedt er bij veel vrouwen een stille complicatie op die lang na de bevalling merkbaar blijft. Sommige keizersnedelittekens in de baarmoeder genezen slecht en laten een klein zakachtig defect in de baarmoederwand achter, een zogenaamde “niche”. Dit defect kan langdurig bloedverlies, pijn en vruchtbaarheidsproblemen veroorzaken en de risico’s bij latere zwangerschappen verhogen. Artsen begrijpen echter nog niet volledig waarom sommige littekens goed genezen en andere niet. Deze studie gebruikt geavanceerde single-cell-analyse en proeven bij dieren om bloot te leggen wat er misgaat in de microscopische genezingsomgeving van deze baarmoederlittekens en wijst op nieuwe wegen om herstel te voorspellen en mogelijk te verbeteren.
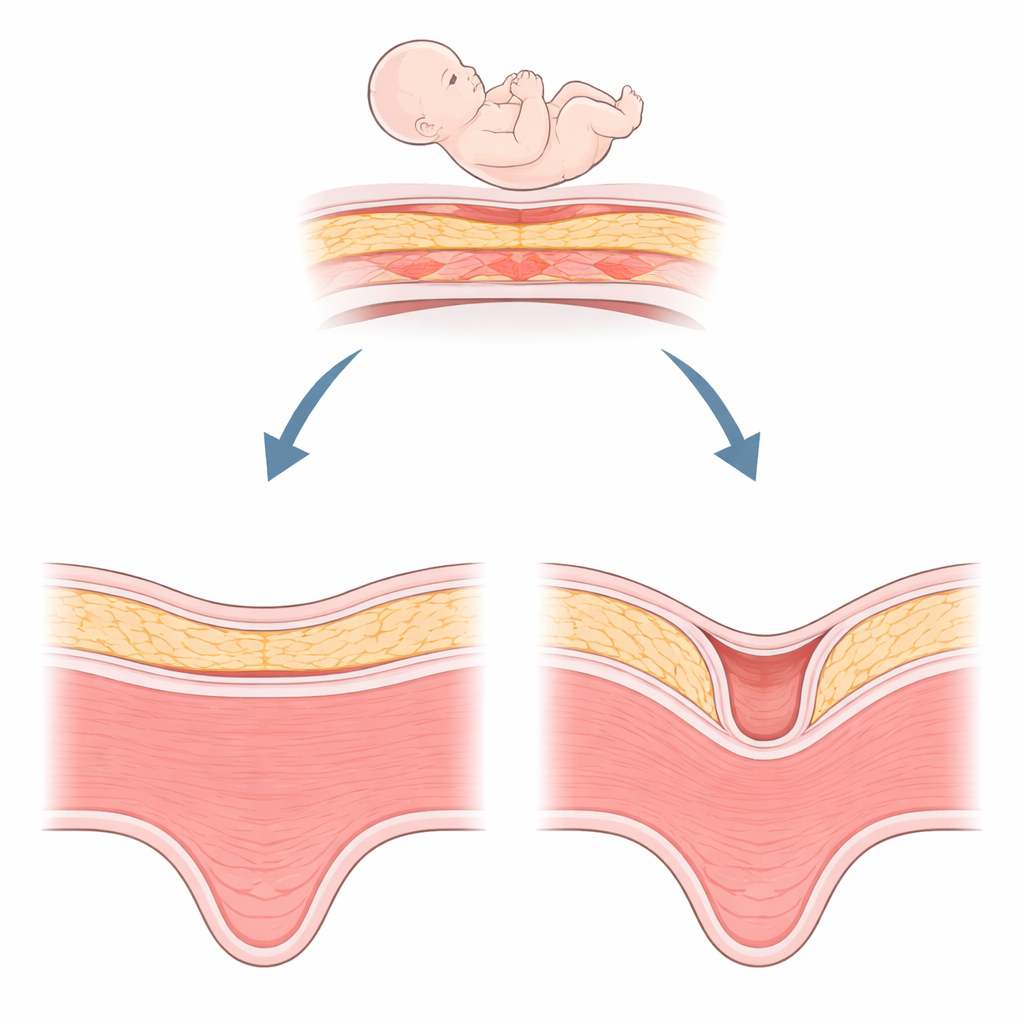
Een verborgen probleem na een keizersnede
Een niche is in essentie een indeuking in de spier van de baarmoeder op de plek van een eerdere keizersnede-incisie, minimaal twee millimeter diep. Het komt verrassend vaak voor—ongeveer bij de helft van de vrouwen na een keizersnede—and de detectie neemt toe door verbeterde echografie en MRI. Vrouwen met een niche kunnen spotting na de menstruatie, chronische bekkenpijn of moeite met zwanger worden opmerken. Bij latere zwangerschappen wordt een niche in verband gebracht met gevaarlijke problemen zoals abnormale bevestiging van de placenta of uteriene ruptuur. Chirurgen kunnen proberen het defect bij te snijden en te herstellen, maar het genezen verloopt niet altijd bevredigend. Dit heeft clinici ertoe gebracht naar biologische verklaringen te zoeken die verder gaan dan alleen de chirurgische techniek.
Inzoomen op individuele cellen in het litteken
De onderzoekers verzamelden weefsel uit drie gebieden bij vrouwen die een operatie ondergingen: goed genezen keizersnedelittekens, slecht genezende niche-weefsels en nabijgelegen schijnbaar normale baarmoederspier. Vervolgens gebruikten ze single-cell RNA-sequencing, een technologie die leest welke genen actief zijn in duizenden individuele cellen, om het cellulaire landschap van deze regio’s in kaart te brengen. In totaal profielen ze meer dan 135.000 cellen en identificeerden acht hoofdtypes, waaronder gladde spiercellen, immuuncellen, bloedvatcellen en fibroblasten—de bindweefselcellen die het geraamte van een litteken opbouwen. Vergeleken met goed genezen littekens bevatte niche-weefsel meer fibroblasten maar minder endotheelcellen, die bloedvaten bekleden en helpen het weefselherstel te coördineren.
Het ontbrekende signaal tussen vaten en littekenbouwers
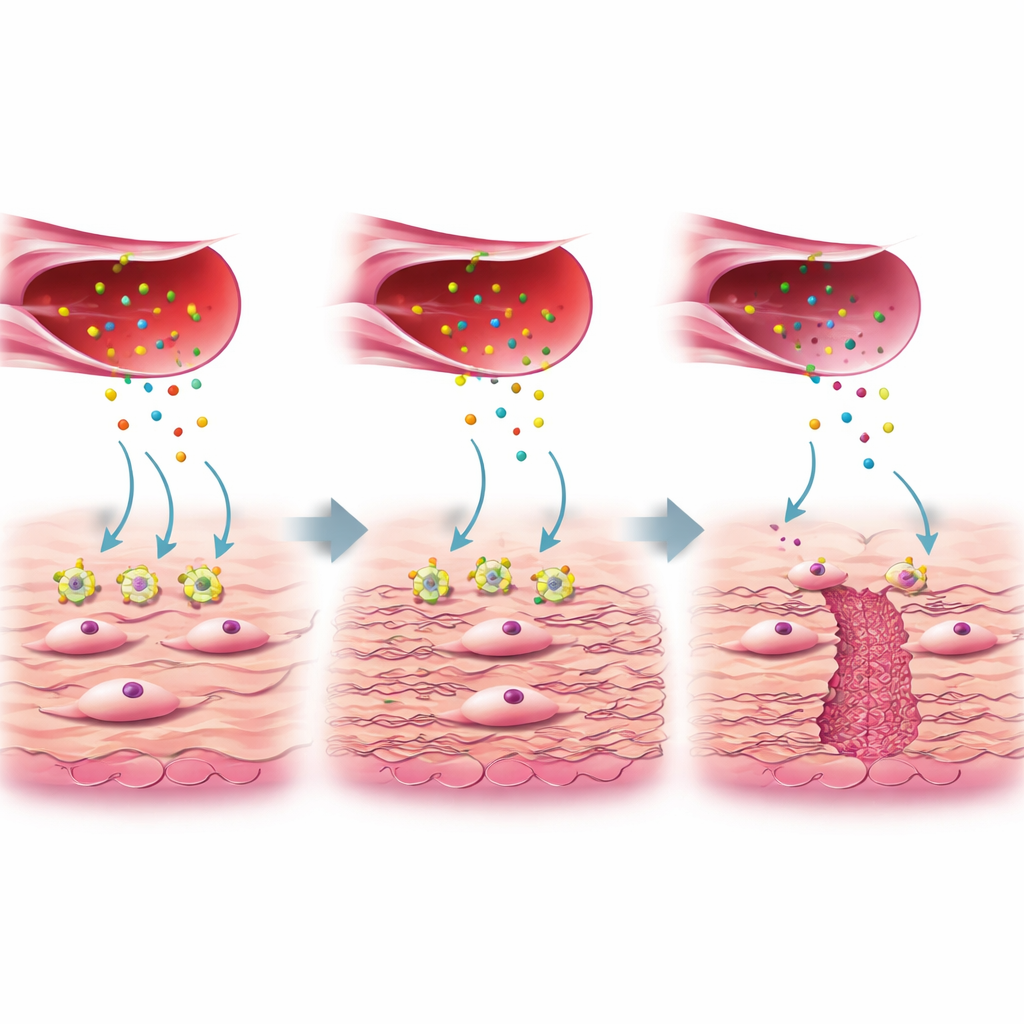
Een nadere blik toonde aan dat niet alle fibroblasten gelijk zijn. Een subgroep, aangeduid als FB3 in de studie, vertoonde genactiviteit gekoppeld aan collageenproductie en wondgenezing en was overvloedig aanwezig in goed genezen littekens maar verminderd in niche-weefsel. Deze behulpzame FB3-cellen reageren normaal op een eiwitsignaal dat connective tissue growth factor (CTGF) heet, dat wordt vrijgegeven door een speciale subgroep geactiveerde endotheelcellen. CTGF bindt aan een receptor op fibroblasten met de naam LRP1. Bij gezond herstel zet deze CTGF–LRP1-interactie interne routes (ERK en WNT) aan die fibroblasten instrueren om stevig collageen en andere extracellulaire matrixcomponenten neer te leggen, waardoor de baarmoederwand wordt opgevuld en versterkt. In niche-weefsel waren de LRP1-niveaus op FB3-fibroblasten echter aanzienlijk lager, hoewel CTGF-productie door bloedvatcellen vergelijkbaar was. De auteurs toonden in celkweken aan dat wanneer LRP1 werd verminderd of geblokkeerd, fibroblasten niet op CTGF reageerden, minder collageen produceerden en de belangrijke herstelroutes werden afgezwakt.
Van laboratoriumbank naar patiënten en diermodellen
Het team onderzocht vervolgens of dit signaleringspaar kon helpen voorspellen hoe goed een chirurgische reparatie zou genezen. In monsters van 60 vrouwen die een transvaginale niche-reparatie ondergingen, hadden degenen wiens littekens later goed genazen hogere CTGF- en LRP1-niveaus dan degenen bij wie de littekens problematisch bleven, en de combinatie van beide markers voorspelde het resultaat het beste. Om te testen of het versterken van CTGF het herstel kon bevorderen, gebruikten de onderzoekers een rattenmodel waarin een gecontroleerde verwonding in de baarmoeder werd aangebracht. Ratten die werden behandeld met recombinante humane CTGF ontwikkelden dikkere spierlagen, minder dicht collageenlittekenweefsel en beter georganiseerd weefsel rond de wond dan onbehandelde dieren. Fibroblasten van deze ratten produceerden ook meer collageen wanneer ze aan CTGF werden blootgesteld—tenzij LRP1 experimenteel werd uitgeschakeld, wat opnieuw het belang van het CTGF–LRP1-partnerschap onderstreept.
Wat dit betekent voor toekomstige moeders
Samengevoegd schetsen de bevindingen het ontstaan van een niche als een verstoring in de communicatie tussen bloedvaten en littekenopbouwende cellen op microscopisch niveau. Wanneer fibroblasten onvoldoende LRP1 hebben, kunnen ze de oproep van CTGF niet goed ‘horen’ om te herbouwen, waardoor een zwak, verdund gebied in de baarmoederwand achterblijft in plaats van een glad, sterk litteken. Dit werk suggereert dat het meten van CTGF en LRP1 rond de tijd van een keizersnede of niche-reparatie artsen ooit zou kunnen helpen voorspellen wie risico loopt op slechte genezing. Het roept ook de mogelijkheid op dat gerichte behandelingen—zoals lokale toediening van CTGF of medicijnen die veilig de downstream-herstelroutes versterken—de uitkomsten kunnen verbeteren. Hoewel dergelijke therapieën zorgvuldige testen op veiligheid en langetermijneffecten vereisen, biedt de studie een gedetailleerde routekaart om fundamentele cellulaire inzichten om te zetten in betere zorg voor vrouwen na een keizersnede.
Bronvermelding: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Trefwoorden: cesarean scar defect, wondgenezing, fibroblasten, groeifactor signalering, uteriene niche