Clear Sky Science · es
Papel de CTGF-LRP1 en la cicatrización deficiente de las incisiones por cesárea
Por qué las cicatrices de cesárea a veces no cicatrizan bien
A medida que los partos por cesárea se vuelven más frecuentes en todo el mundo, una complicación silenciosa afecta a muchas mujeres mucho después del parto. Algunas cicatrices de cesárea en el útero cicatrizan mal, dejando un pequeño defecto en forma de bolsa en la pared uterina llamado “nicho”. Este defecto puede causar sangrado prolongado, dolor y problemas de fertilidad, y puede aumentar los riesgos en embarazos posteriores. Sin embargo, los médicos aún no comprenden completamente por qué algunas cicatrices sanan bien y otras no. Este estudio utiliza análisis de células individuales de vanguardia y experimentos con animales para descubrir qué falla en el entorno microscópico de cicatrización de estas cicatrices uterinas y apunta a nuevas formas de predecir y posiblemente mejorar la recuperación.
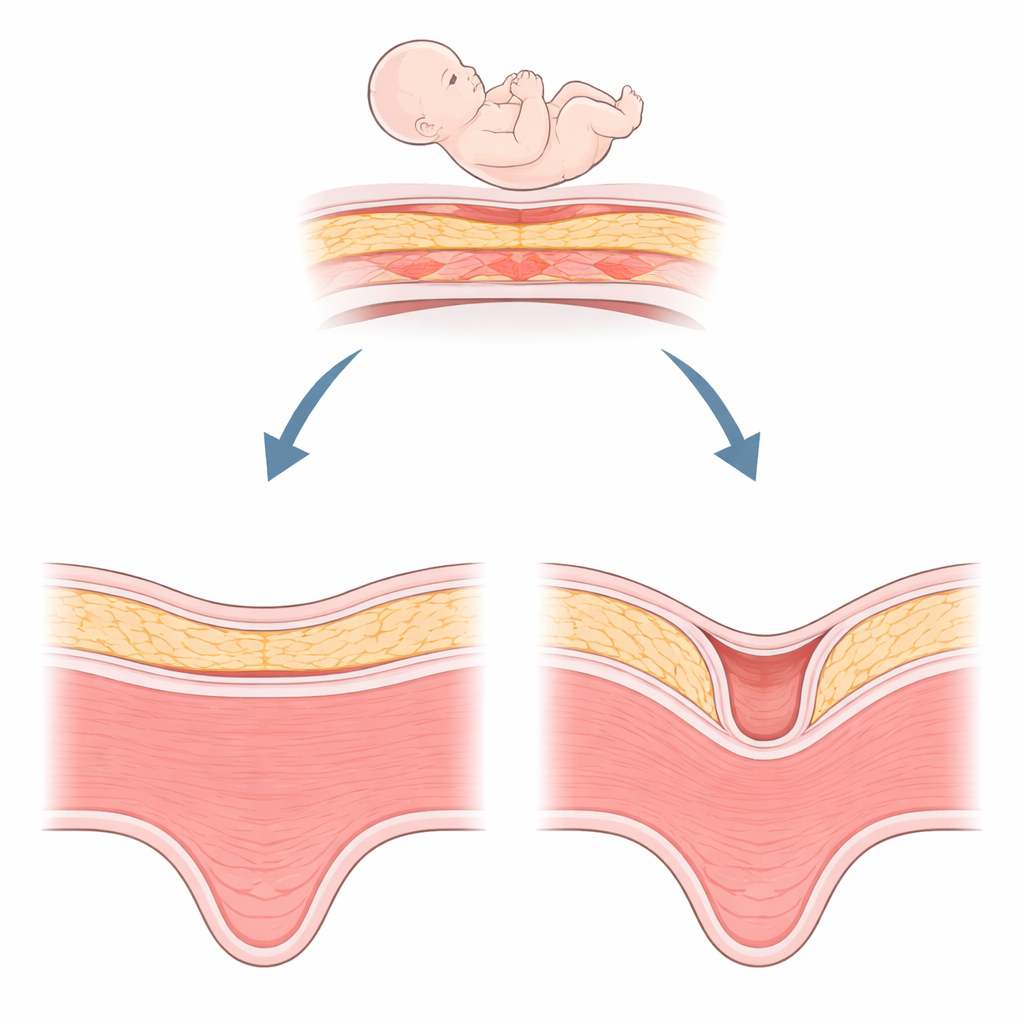
Un problema oculto tras el parto por cesárea
Un nicho es, esencialmente, una hendidura en el músculo del útero en el lugar de una incisión por cesárea previa, de al menos dos milímetros de profundidad. Es sorprendentemente común: se observa en aproximadamente la mitad de las mujeres después de una cesárea, y su detección está aumentando con mejores técnicas de ecografía y resonancia magnética. Las mujeres con un nicho pueden notar manchas entre periodos, molestias pélvicas crónicas o dificultad para concebir. En embarazos posteriores, un nicho puede asociarse con problemas peligrosos como la implantación anormal de la placenta o la ruptura uterina. Los cirujanos pueden intentar recortar y reparar este defecto, pero la cicatrización no siempre es satisfactoria. Esto ha llevado a los clínicos a buscar explicaciones biológicas más allá de la técnica quirúrgica.
Acercándose a las células individuales de la cicatriz
Los investigadores recolectaron tejido de tres áreas en mujeres sometidas a cirugía: cicatrices de cesárea bien cicatrizadas, tejido de nicho mal cicatrizado y músculo uterino aparentemente normal en las cercanías. Luego usaron secuenciación de ARN de célula única, una tecnología que lee qué genes están activos en miles de células individuales, para cartografiar el paisaje celular de estas regiones. En total, perfilaron más de 135.000 células e identificaron ocho tipos principales, incluidos células del músculo liso, células inmunitarias, células vasculares y fibroblastos, las células del tejido conectivo que construyen el armazón de una cicatriz. En comparación con las cicatrices bien cicatrizadas, el tejido de nicho contenía más fibroblastos pero menos células endoteliales, que recubren los vasos sanguíneos y ayudan a coordinar la reparación tisular.
La señal ausente entre los vasos y los constructores de la cicatriz
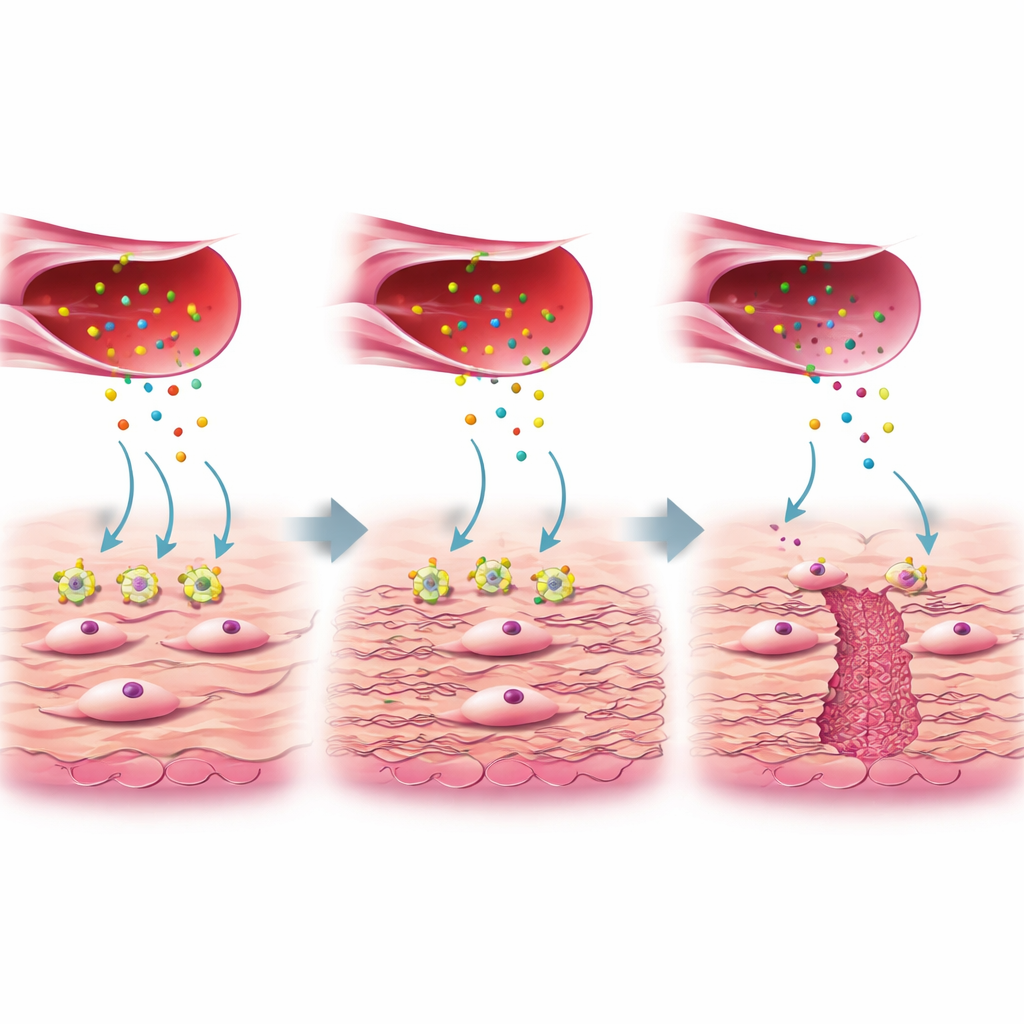
Un examen más detallado reveló que no todos los fibroblastos son iguales. Un subgrupo, llamado FB3 en el estudio, mostró actividad génica vinculada a la producción de colágeno y a la cicatrización y era abundante en cicatrices bien reparadas pero reducido en el tejido de nicho. Estos fibroblastos FB3 útiles normalmente responden a una señal proteica llamada factor de crecimiento del tejido conectivo (CTGF), que es liberada por un subgrupo especial de células endoteliales activadas. CTGF se une a un receptor en los fibroblastos llamado LRP1. En la cicatrización sana, esta interacción CTGF–LRP1 activa vías internas (ERK y WNT) que indican a los fibroblastos que depositen colágeno resistente y otros componentes de la matriz extracelular, rellenando y fortaleciendo la pared uterina. En el tejido de nicho, sin embargo, los niveles de LRP1 en los fibroblastos FB3 eran marcadamente más bajos, aunque la producción de CTGF por las células vasculares era similar. Los autores demostraron en cultivos celulares que cuando LRP1 se reducía o bloqueaba, los fibroblastos no respondían a CTGF, producían menos colágeno y las vías clave de reparación quedaban atenuadas.
Del banco de laboratorio a pacientes y modelos animales
El equipo preguntó entonces si este par de señalización podría ayudar a predecir qué tan bien cicatrizaría una reparación quirúrgica. En muestras de 60 mujeres sometidas a reparación transvaginal del nicho, aquellas cuyas cicatrices cicatrizaron bien más tarde tenían niveles más altos de CTGF y LRP1 que las cuyos tejidos seguían problemáticos, y la combinación de ambos marcadores fue la mejor para predecir el resultado. Para probar si aumentar CTGF podría ayudar a la cicatrización, los investigadores usaron un modelo de rata en el que se hizo una lesión controlada en el útero. Las ratas tratadas con CTGF humano recombinante desarrollaron capas musculares más gruesas, cicatrices de colágeno menos densas y tejido mejor organizado alrededor de la herida que los animales no tratados. Los fibroblastos de estas ratas también produjeron más colágeno cuando se expusieron a CTGF, a menos que LRP1 se redujera experimentalmente, lo que subraya nuevamente la importancia de la asociación CTGF–LRP1.
Qué significa esto para las futuras madres
En conjunto, los hallazgos dibujan la formación del nicho como una ruptura en la comunicación entre los vasos sanguíneos y las células constructoras de la cicatriz a nivel microscópico. Cuando los fibroblastos no tienen suficiente LRP1, no pueden “oír” correctamente la señal de CTGF para reconstruir, dejando una zona débil y adelgazada en la pared uterina en lugar de una cicatriz lisa y sólida. Este trabajo sugiere que medir CTGF y LRP1 alrededor del momento de la cesárea o de la reparación del nicho podría algún día ayudar a los médicos a predecir quién está en riesgo de mala cicatrización. También plantea la posibilidad de que tratamientos dirigidos —como la entrega local de CTGF o fármacos que refuercen de forma segura las vías de reparación aguas abajo— podrían mejorar los resultados. Si bien dichas terapias requieren pruebas cuidadosas de seguridad y efectos a largo plazo, el estudio ofrece una hoja de ruta detallada para convertir insights celulares básicos en una mejor atención para las mujeres después del parto por cesárea.
Cita: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Palabras clave: defecto de la cicatriz por cesárea, cicatrización de heridas, fibroblastos, señalización de factores de crecimiento, nicho uterino