Clear Sky Science · fr
Rôle du CTGF-LRP1 dans la mauvaise cicatrisation des incisions de césarienne
Pourquoi les cicatrices de césarienne ne cicatrisent parfois pas correctement
À mesure que les accouchements par césarienne deviennent plus fréquents dans le monde, une complication discrète affecte de nombreuses femmes longtemps après l’accouchement. Certaines cicatrices de césarienne dans l’utérus cicatrisent mal, laissant un petit défaut en forme de poche dans la paroi utérine appelé « niche ». Ce défaut peut provoquer des saignements prolongés, des douleurs et des problèmes de fertilité, et augmenter les risques lors de grossesses ultérieures. Pourtant, les médecins ne comprennent pas encore totalement pourquoi certaines cicatrices guérissent bien tandis que d’autres échouent. Cette étude utilise des analyses unicellulaires de pointe et des expériences animales pour dévoiler ce qui dysfonctionne dans l’environnement microscopique de cicatrisation de ces cicatrices utérines et pointe vers de nouvelles façons de prédire et possiblement d’améliorer la récupération.
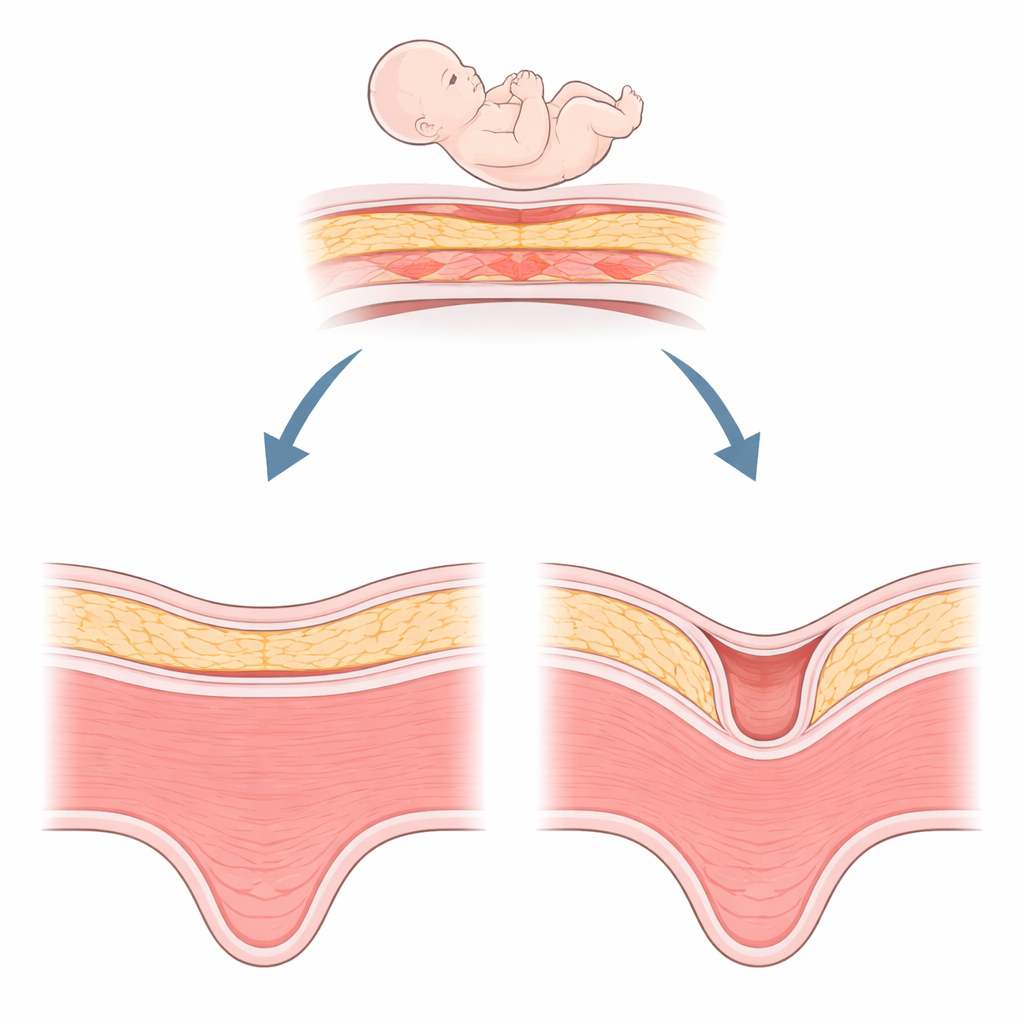
Un problème caché après une césarienne
Une niche est essentiellement un creux dans le muscle de l’utérus au niveau d’une incision de césarienne précédente, d’au moins deux millimètres de profondeur. Elle est étonnamment fréquente — observée chez environ la moitié des femmes après une césarienne — et sa détection augmente avec l’amélioration des échographies et de l’IRM. Les femmes présentant une niche peuvent constater des métrorragies après leurs règles, des douleurs pelviennes chroniques ou des difficultés à concevoir. Lors de grossesses ultérieures, une niche peut être associée à des complications dangereuses comme un placenta anormalement implanté ou une rupture utérine. Les chirurgiens peuvent tenter de réséquer et de réparer ce défaut, mais la cicatrisation n’est pas toujours satisfaisante. Cela a poussé les cliniciens à rechercher des explications biologiques au-delà de la seule technique chirurgicale.
Zoom sur les cellules individuelles de la cicatrice
Les chercheurs ont prélevé des tissus de trois zones chez des femmes subissant une intervention : des cicatrices de césarienne bien cicatrisées, du tissu de niche mal cicatrisé et du muscle utérin adjacent apparemment normal. Ils ont ensuite utilisé le séquençage d’ARN unicellulaire, une technologie qui lit les gènes actifs dans des milliers de cellules individuelles, pour dresser la carte du paysage cellulaire de ces régions. Au total, ils ont profilé plus de 135 000 cellules et identifié huit types cellulaires majeurs, notamment des cellules musculaires lisses, des cellules immunitaires, des cellules vasculaires et des fibroblastes — les cellules conjonctives qui construisent l’armature d’une cicatrice. Par rapport aux cicatrices bien cicatrisées, le tissu de niche contenait davantage de fibroblastes mais moins de cellules endothéliales, qui tapissent les vaisseaux sanguins et aident à coordonner la réparation tissulaire.
Le signal manquant entre les vaisseaux et les bâtisseurs de cicatrice
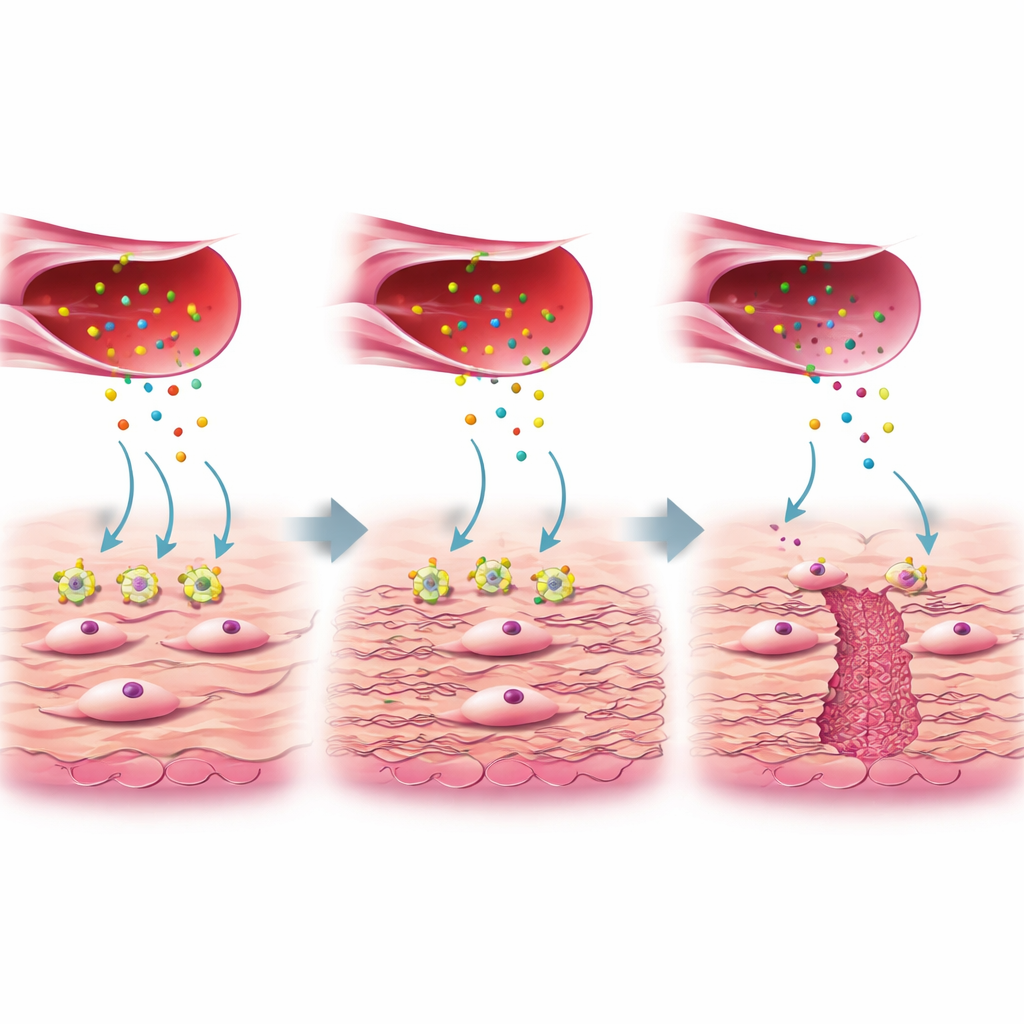
Un examen plus approfondi a révélé que tous les fibroblastes ne se valent pas. Un sous-groupe, appelé FB3 dans l’étude, présentait une activité génique liée à la production de collagène et à la cicatrisation et était abondant dans les cicatrices bien cicatrisées mais réduit dans le tissu de niche. Ces fibroblastes FB3 utiles répondent normalement à un signal protéique appelé facteur de croissance des tissus conjonctifs (CTGF), libéré par un sous-groupe spécial de cellules endothéliales activées. Le CTGF se lie à un récepteur sur les fibroblastes nommé LRP1. Lors d’une cicatrisation saine, cette interaction CTGF–LRP1 active des voies intracellulaires (ERK et WNT) qui indiquent aux fibroblastes de déposer un collagène robuste et d’autres composants de la matrice extracellulaire, comblant et renforçant la paroi utérine. Dans le tissu de niche, toutefois, les niveaux de LRP1 sur les fibroblastes FB3 étaient nettement plus faibles, même si la production de CTGF par les cellules vasculaires était similaire. Les auteurs ont montré en cultures cellulaires que lorsque LRP1 était réduit ou bloqué, les fibroblastes ne répondaient pas au CTGF, produisaient moins de collagène et les voies de réparation clés étaient atténuées.
Du laboratoire aux patientes et aux modèles animaux
L’équipe a ensuite demandé si cette paire de signalisation pouvait aider à prévoir la qualité de la cicatrisation après une réparation chirurgicale. Dans des échantillons de 60 femmes ayant subi une réparation vaginale de niche, celles dont les cicatrices ont ensuite bien guéri présentaient des niveaux plus élevés de CTGF et de LRP1 que celles dont les cicatrices restaient problématiques, et la combinaison des deux marqueurs prédisait le mieux le résultat. Pour tester si l’augmentation du CTGF pouvait favoriser la cicatrisation, les chercheurs ont utilisé un modèle de rat dans lequel une lésion contrôlée était pratiquée dans l’utérus. Les rats traités par CTGF humain recombinant ont développé des couches musculaires plus épaisses, des cicatrices de collagène moins denses et un tissu mieux organisé autour de la plaie que les animaux non traités. Les fibroblastes issus de ces rats produisaient aussi davantage de collagène lorsqu’ils étaient exposés au CTGF — sauf si LRP1 était expérimentalement diminué, ce qui souligne à nouveau l’importance du partenariat CTGF–LRP1.
Ce que cela signifie pour les futures mères
Pris ensemble, les résultats dessinent le portrait d’une formation de niche comme d’une rupture de communication entre les vaisseaux sanguins et les cellules bâtisseuses de cicatrice au niveau microscopique. Lorsque les fibroblastes ne disposent pas d’un nombre suffisant de LRP1, ils ne peuvent pas correctement « entendre » l’appel du CTGF pour reconstruire, laissant une zone affaiblie et amincie dans la paroi utérine au lieu d’une cicatrice lisse et solide. Ce travail suggère que mesurer le CTGF et le LRP1 autour du moment de la césarienne ou de la réparation de niche pourrait un jour aider les médecins à prédire qui risque une mauvaise cicatrisation. Il évoque aussi la possibilité de traitements ciblés — tels que l’administration locale de CTGF ou des médicaments qui stimulent en toute sécurité les voies de réparation en aval — pour améliorer les résultats. Si de telles thérapies devront être soigneusement évaluées pour la sécurité et les effets à long terme, l’étude fournit une feuille de route détaillée pour transformer des connaissances cellulaires fondamentales en de meilleurs soins pour les femmes après une césarienne.
Citation: He, C., Ge, S., Xia, W. et al. Role of CTGF-LRP1 in impaired healing of cesarean section incisions. Nat Commun 17, 3278 (2026). https://doi.org/10.1038/s41467-026-69747-9
Mots-clés: défaut de cicatrice de césarienne, cicatrisation, fibroblastes, signalisation des facteurs de croissance, niche utérine