Clear Sky Science · sv
Bioaktivt lipidmedierad strukturell och funktionell reglering av den essentiella mänskliga kaliumkanalen Kir7.1
Varför små portar i våra celler spelar roll
Inbäddade i membranen hos många av våra celler finns mikroskopiska portar som släpper in och ut kaliumjoner. En av dessa portar, kallad Kir7.1, är avgörande för frisk syn, hjärnfunktion och till och med tidpunkten för förlossning. När denna port är defekt kan människor tidigt förlora synen, och djur får problem med födointag och graviditet. Denna studie visar, på atomnivå, hur naturliga fetter och hormonliknande molekyler fäster vid Kir7.1 och fungerar som dess av/på-strömbrytare, vilket öppnar nya vägar för läkemedelsutveckling.
En särskild port för elektrisk balans
Kir7.1 tillhör en familj av kanaler som vanligtvis låter kaliumjoner röra sig lättare in i en cell än ut ur den, vilket hjälper till att ställa in den elektriska balansen över cellmembranet. I ögats retinala pigmentepitel håller Kir7.1 miljön kring ljussensoriska celler stabil; utan den dör fotoreceptorerna långsamt och synen försvagas. Kir7.1 formar också nervkretsar som styr aptit och bidrar till att hålla livmodern lugn under graviditet. Dessa breda roller har gjort kanalen till ett attraktivt men illa förstått läkemedelsmål, särskilt eftersom dess naturliga regulatorer, bortsett från några kända membranlipider, var gåtfulla.
Att se porten i tre distinkta poser
För att avslöja hur Kir7.1 fungerar producerade forskarna stora mängder av det mänskliga proteinet i däggdjursceller, renade det och avbildade det med högupplöst kryo-elektronmikroskopi. De fångade kanalen i tre huvudsakliga former. I det ”utsträckta” tillståndet sitter den nedre, cytoplasmatiska delen längre från membranet och den centrala tunneln för joner är lång och relativt smal, en sannolikt icke-ledande pose. I det ”dockade” tillståndet roterar denna nedre domän och rör sig uppåt mot membranet, vilket förkortar och något vidgar tunneln. I ett tredje tillstånd är kanalen bunden till en kraftfull syntetisk steroid tillsammans med en signalgivande lipid kallad PIP2, vilket ger en konfiguration som verkar ”färdig” för öppning. En liten förändring i en enda aminosyra nära selektivitetsfiltret hjälper till att förklara varför Kir7.1 kan leda cesiumjoner, till skillnad från de flesta närbesläktade kanaler.
Hur fetter och hormoner delar kontroll
De strukturella ögonblicksbilderna visade att Kir7.1 ständigt bär en PIP2-molekyl vid en konservrad plats där andra familjemedlemmar också binder denna lipid. PIP2 ensam räcker dock inte för att helt öppna Kir7.1. En andra ficka, kilad mellan dess membranöverbyggande helixar, innehåller en annan typ av lipid. I det vila‑utsträckta tillståndet rymmer denna ficka kolesterol, en välkänd membransteroal. Elektrofysiologiska experiment visade att tillsatt kolesterol dämpar Kir7.1‑strömmar, medan vissa steroider, inklusive graviditetshormonet progesteron och neurosteroiden DHEA, kraftigt förstärker dem. Uppgifterna stöder en modell där kolesterol fungerar som en naturlig broms: aktiverande steroider måste först tränga undan kolesterolet från fickan, och när de gör det i närvaro av PIP2 kan kanalens nedre domän rotera och jonvägen vidgas.
Att upptäcka starkare molekylära nycklar
För att omvandla denna insikt till praktiska verktyg screenade teamet ett brett panel av naturliga och syntetiska steroider och deras spegelbildsformer. De fann flera nya molekyler som slår på Kir7.1, många vid låga mikromolära eller till och med submikromolära koncentrationer. En särskild hitt var en enantiomer av läkemedlet 17‑hydroxyprogesteron caproat, som band tätt i samma hydrofoba ficka som normalt hyser kolesterol. I strukturen med denna aktivator närvarande bildade steroidens polära topp en nära vätebindning med en nyckel‑threonin‑sidokedja, medan dess oljiga kropp låg an mot kanalens helixar. Denna täta passform hjälper till att förklara dess potens och dess förmåga att hålla kanalen aktiv även i närvaro av en standard Kir7.1‑hämmare.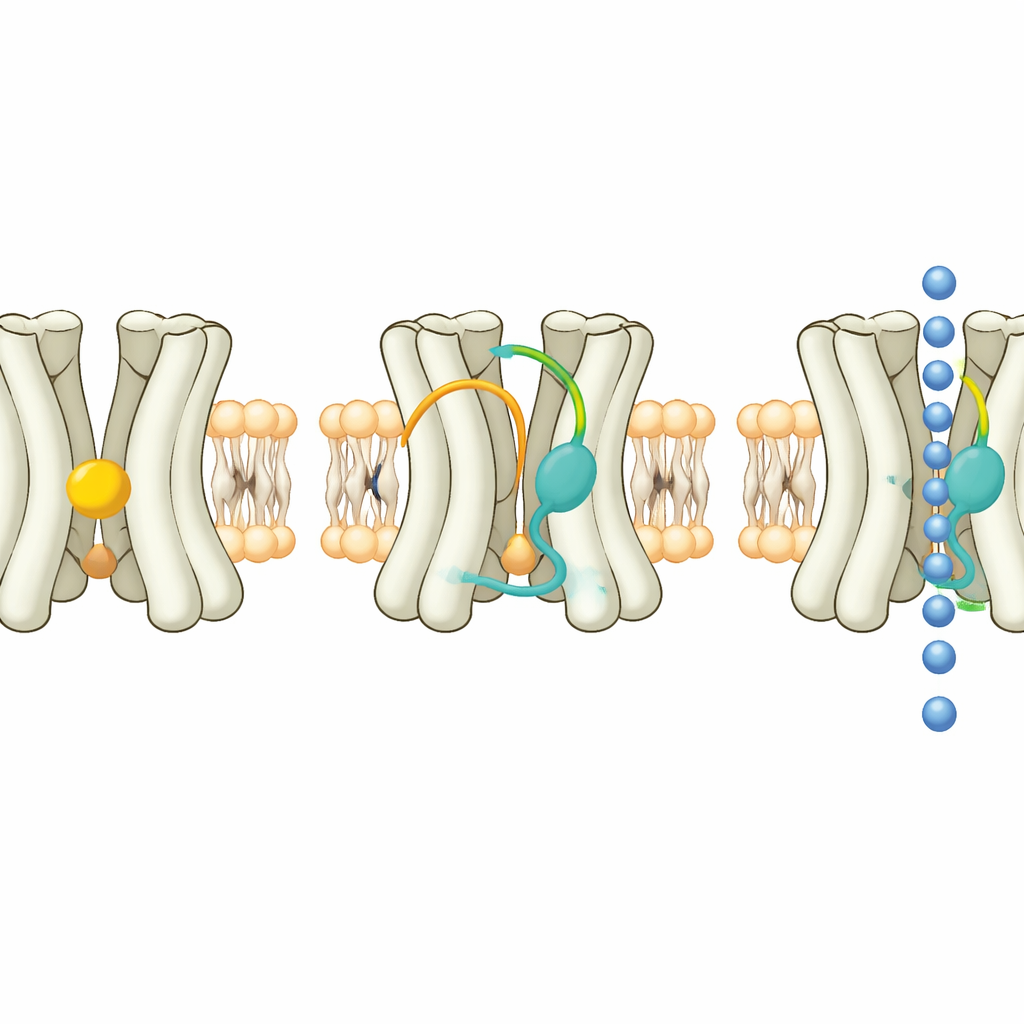
Från strukturell karta till terapeutiskt löfte
Tillsammans visar arbetet att Kir7.1 styrs av ett samspelande partnerskap mellan PIP2, hämmande kolesterol och utvalda aktiverande steroider. PIP2 förankrar och delvis organiserar kanalen; kolesterol håller den i en utsträckt, mindre ledande form; och steroider som fördriver kolesterolet lossar helixarna och låter den nedre domänen skifta mot ett mer öppet, ledande tillstånd. Genom att lösa dessa interaktioner atom för atom och beskriva hur små kemiska förändringar ändrar steroidpotens erbjuder studien en ritning för att designa nya läkemedel som återställer eller finjusterar Kir7.1‑aktivitet vid sjukdomar i öga, hjärna och livmoder.
Citering: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Nyckelord: Kir7.1-kaliumkanal, kolesterolreglering, steroidmodulatorer, cryo-EM-struktur, retinalt pigmentepitel