Clear Sky Science · it
Regolazione strutturale e funzionale del canale potassio umano essenziale Kir7.1 mediata da lipidi bioattivi
Perché contano i piccoli cancelli nelle nostre cellule
Nelle membrane di molte delle nostre cellule sono incastonati piccoli cancelli microscopici che permettono il passaggio degli ioni potassio dentro e fuori. Uno di questi cancelli, chiamato Kir7.1, è cruciale per una visione sana, il funzionamento del cervello e persino la tempistica del parto. Se questo cancello si guasta, le persone possono perdere la vista precocemente e gli animali sviluppano problemi di alimentazione e di gravidanza. Questo studio rivela, a livello atomico, come grassi naturali e molecole simili a ormoni si agganciano a Kir7.1 e ne fanno gli interruttori on–off, aprendo nuove strade per la progettazione di farmaci.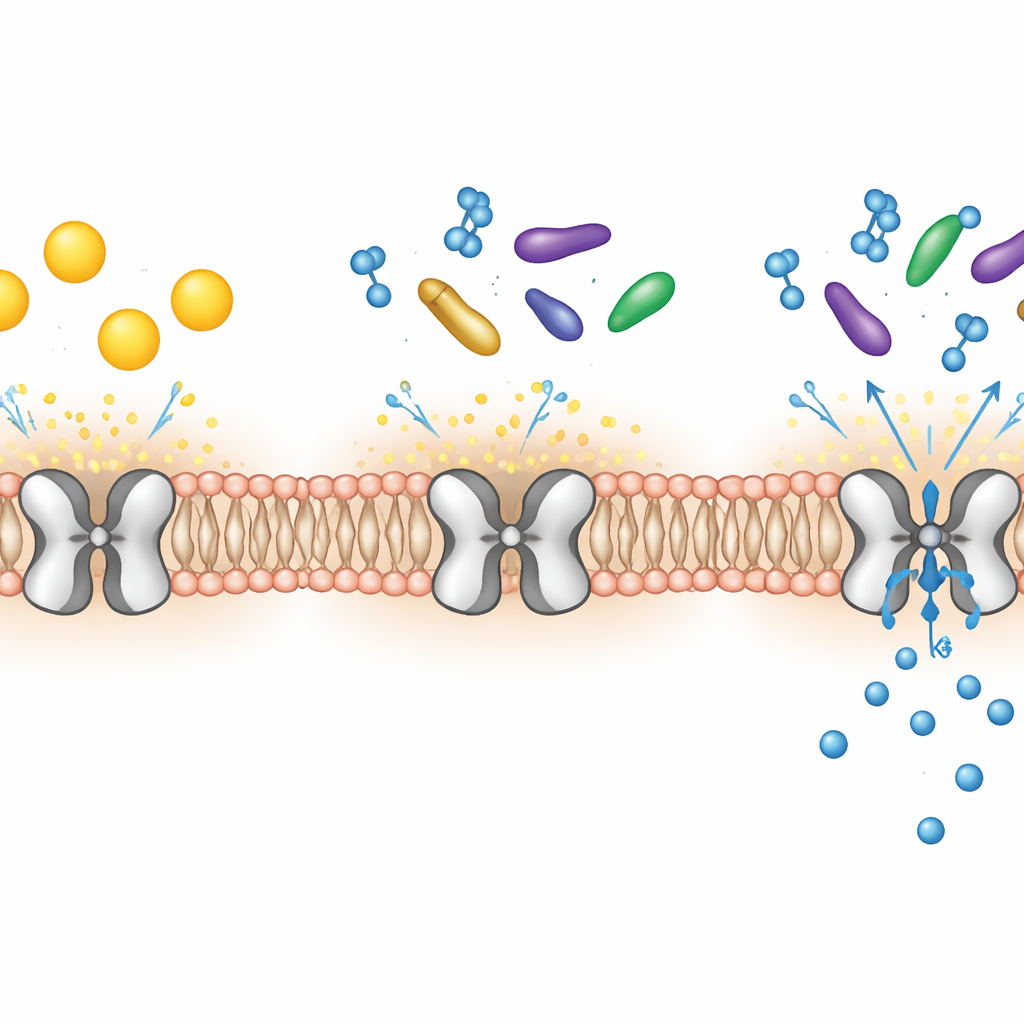
Un cancello speciale per l’equilibrio elettrico
Kir7.1 appartiene a una famiglia di canali che normalmente permettono agli ioni potassio di entrare in una cellula più facilmente di quanto possano uscirne, contribuendo a stabilire l’equilibrio elettrico attraverso la membrana cellulare. Nell’epitelio pigmentato retinico dell’occhio, Kir7.1 mantiene stabile l’ambiente attorno alle cellule fotosensibili; senza di esso, i fotorecettori lentamente muoiono e la vista si affievolisce. Kir7.1 modella anche i circuiti nervosi che controllano l’appetito e aiuta a mantenere l’utero quiescente durante la gravidanza. Questi ruoli estesi hanno reso il canale un bersaglio farmacologico attraente ma poco compreso, specialmente perché i suoi regolatori naturali, oltre ad alcune note lipidi di membrana, restavano misteriosi.
Vedere il cancello in tre pose distinte
Per scoprire come funziona Kir7.1, i ricercatori hanno prodotto grandi quantità della proteina umana in cellule di mammifero, l’hanno purificata e immaginata usando la microscopia crio-elettronica ad alta risoluzione. Hanno catturato il canale in tre forme principali. Nallo stato “esteso”, la parte inferiore citoplasmatica del canale si trova più lontano dalla membrana e il tunnel centrale per gli ioni è lungo e relativamente stretto, una conformazione probabilmente non conduttiva. Nello stato “ancorato” (docked), questo dominio inferiore ruota e si sposta verso l’alto verso la membrana, accorciando e leggermente allargando il tunnel. In un terzo stato, il canale è legato a uno steroide sintetico potente insieme a un lipide di segnalazione chiamato PIP2, producendo una configurazione che appare “pronta” per aprirsi. Una piccola variazione in un singolo amminoacido vicino al filtro di selettività aiuta a spiegare perché Kir7.1 può condurre ioni cesio, a differenza della maggior parte dei canali correlati.
Come grassi e ormoni condividono il controllo
Le istantanee strutturali hanno rivelato che Kir7.1 porta costantemente una molecola di PIP2 in un sito conservato dove anche altri membri della famiglia legano questo lipide. Tuttavia, il solo PIP2 non è sufficiente ad aprire completamente Kir7.1. Una seconda tasca, incuneata tra i suoi eliche transmembrana, contiene un diverso tipo di lipide. Nello stato esteso di riposo, questa tasca ospita colesterolo, uno sterolo di membrana familiare. Esperimenti di elettrofisiologia hanno mostrato che l’aggiunta di colesterolo extra attenua le correnti di Kir7.1, mentre certi steroidi, incluso l’ormone della gravidanza progesterone e il neurosteroide DHEA, le potenziano fortemente. I dati supportano un modello in cui il colesterolo agisce come un freno naturale: gli steroidi attivanti devono prima rimuovere il colesterolo dalla tasca e, quando lo fanno in presenza di PIP2, il dominio inferiore del canale può ruotare e il percorso ionico può allargarsi.
Alla ricerca di chiavi molecolari più potenti
Per trasformare questa intuizione in strumenti pratici, il gruppo ha testato un ampio pannello di steroidi naturali e sintetici e le loro forme enantiomeriche. Hanno trovato diverse nuove molecole che attivano Kir7.1, molte a concentrazioni micromolari basse o anche submicromolari. Una in particolare, un enantiomero del farmaco 17-idrossiprogesterone caproato, si è legato saldamente nella stessa tasca idrofobica che normalmente ospita il colesterolo. Nella struttura con questo attivatore, la punta polare dello steroide formava un vicino legame a idrogeno con una catena laterale chiave di treonina, mentre il suo corpo oleoso si adagiava contro le eliche del canale. Questo incastro compatto aiuta a spiegare la sua potenza e la sua capacità di mantenere il canale attivo anche in presenza di un bloccante standard di Kir7.1.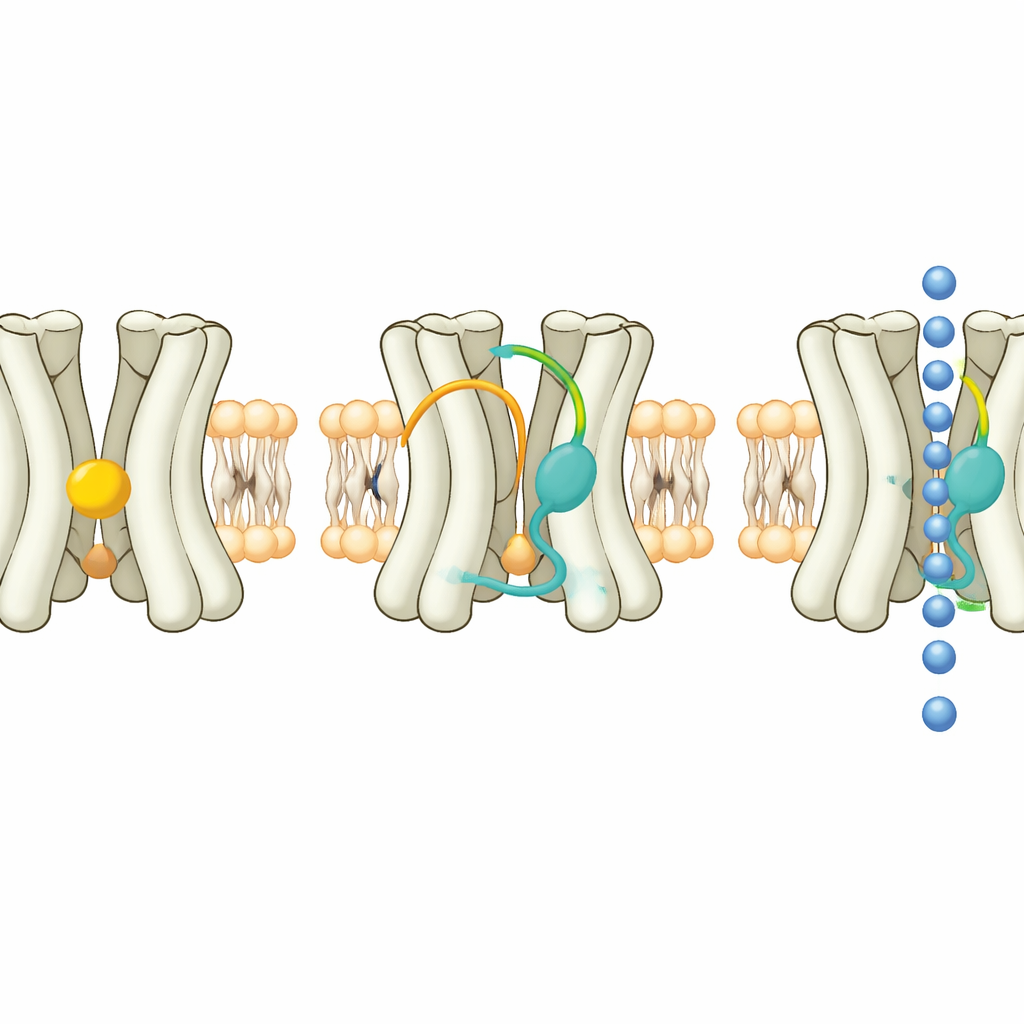
Dalla mappa strutturale alla promessa terapeutica
Nel complesso, il lavoro mostra che Kir7.1 è governato da una partnership cooperativa tra PIP2, il colesterolo inibitorio e specifici steroidi attivanti. PIP2 ancora e parzialmente organizza il canale; il colesterolo lo mantiene in una forma estesa e meno conduttiva; e gli steroidi che espellono il colesterolo allentano le eliche e permettono al dominio inferiore di spostarsi verso uno stato più aperto e conduttivo. Risolvendo queste interazioni atomo per atomo e delineando come piccole modifiche chimiche cambiano la potenza degli steroidi, lo studio offre una guida per progettare nuovi farmaci che ripristinino o modulino l’attività di Kir7.1 nelle malattie dell’occhio, del cervello e dell’utero.
Citazione: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Parole chiave: Canale potassio Kir7.1, regolazione colesterolo, modulatori steroidei, cryo-EM structure, epitelio pigmentato retinico