Clear Sky Science · he
ויסות מבני ותפקודי של תעלת האשלגן האנושית החיונית Kir7.1 באמצעות ליפידים ביואקטיביים
מדוע דלתות זעירות בתאים שלנו חשובות
טבועים בממברנות של רבים מתאי הגוף שלנו יש שערים זעירים שמאפשרים ליון האשלגן לזרום פנימה והחוצה. אחד מהשערים הללו, הקרוי Kir7.1, חיוני לראייה תקינה, לפעילות המוחית ואפילו לתזמון הלידה. כאשר השער הזה ניזוק, אנשים עלולים להיעזר בעיוורון מוקדם בחיים, ובחיות מתפתחות בעיות באכילה ובהריון. המחקר חושף, ברזולוציה אטומית, כיצד שומנים טבעיים ומולקולות דמויות־הורמון נקשרים ל־Kir7.1 ומשמשים כמפסקי כיבוי־הדלקה שלו, ופותח נתיבים חדשים לתכנון תרופות.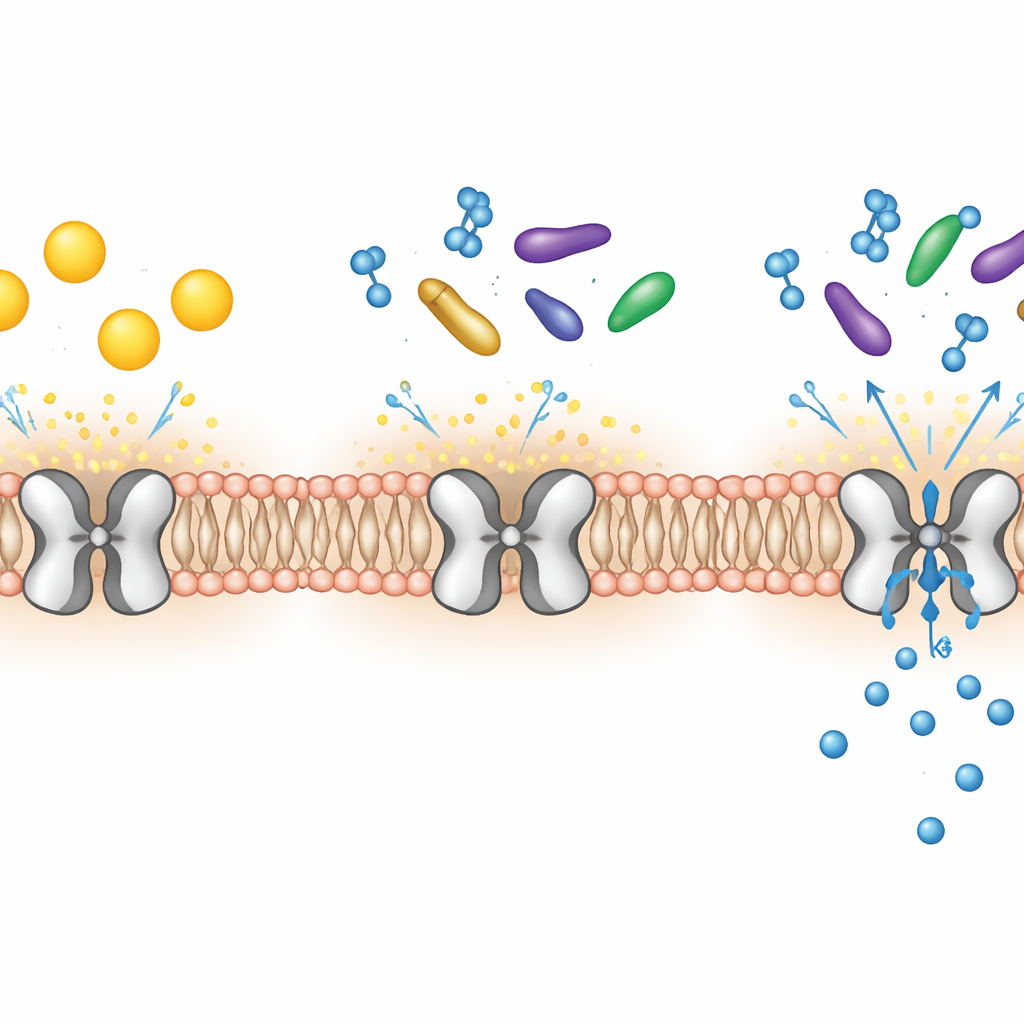
שער מיוחד לאיזון חשמלי
Kir7.1 שייך למשפחה של תעלות שבדרך כלל מאפשרות ליוני אשלגן להיכנס אל התא ביתר קלות מאשר לצאת ממנו, ובכך מסייעות לקביעת שיווי המשקל החשמלי על גבי הממברנה. באפיתל הפיגמנטרי של הרשתית, Kir7.1 שומרת על סביבה יציבה סביב התאים החשים באור; בהיעדרה, תאי הפוטורצפטורים נרקבים לאט והראייה נחלשת. Kir7.1 גם מעצבת מעגלים עצביים ששולטים בתיאבון ועוזרת לשמור על רוגע הרחם במהלך ההריון. התפקידים הרחבים הללו הפכו את התעלה למטרה תרופתית אטרקטיבית אך לא מובנת די הצורך, במיוחד משום שמווסתיה הטבעיים, מעבר למספר ליפידים ממברנליים ידועים, לא היו ברורים.
לראות את השער בשלוש תנוחות מובחנות
כדי לחשוף כיצד Kir7.1 פועלת, החוקרים ייצרו כמויות גדולות של החלבון האנושי בתאים יונקים, טיהרו אותו וצילמו אותו באמצעות מיקרוסקופיה קירו־אלקטרונית ברזולוציה גבוהה. הם תפסו את התעלה בשלוש צורות עיקריות. במצב ה"מוארך", החלק התאי המצומד של התעלה ממוקם רחוק יותר מהממברנה ומנהרת האיונים המרכזית ארוכה יחסית וצרה, תנוחה שנראית כנוטה לא להוליך. במצב ה"מוצמד" אותו תחום תחתון מסתובב ונע מעלה לעבר הממברנה, מקצר וקצת מרחיב את המנהרה. במצב שלישי, התעלה קשורה לסטרואיד סינתטי חזק יחד עם ליפיד סיגנלינג בשם PIP2, ויוצרת קונפיגורציה שנראית כ"מוכנה" לפתיחה. שינוי קטן בחומצת אמינו בודדת קרוב לסינון הסלקטיבי מסביר מדוע Kir7.1 יכולה להוליך יוני צזיום, בניגוד לרוב התעלות הקרובות אליה.
כיצד שומנים והורמונים חולקים שליטה
צילום מבני של הרגעים הראה ש־Kir7.1 נושאת באופן תמידי מולקולת PIP2 באתר שמור שבו גם בני המשפחה האחרים נקשרים לליפיד זה. עם זאת, PIP2 לבדו אינו מספיק כדי לפתוח באופן מלא את Kir7.1. כיס שני, הממוקם בין ההליקסים החוצים את הממברנה, מכיל סוג אחר של ליפיד. במצב המנוחה המוארך, כיס זה מאכלס כולסטרול, סטרול ממברנלי מוכר. ניסויי אלקטרופיזיולוגיה הראו שהוספת כולסטרול חיצוני מדכאת את הזרמים של Kir7.1, בעוד שסטרואידים מסוימים, כולל הורמון ההריון פרוגסטרון והנוירוסטירואיד DHEA, מגבירים אותם בעוצמה. הממצאים תומכים במודל שבו הכולסטרול פועל כבלם טבעי: סטרואידים מפעילים חייבים להדיח קודם את הכולסטרול מהכיס, וכאשר הם עושים זאת בנוכחות PIP2, התחום התאי של התעלה יכול להסתובב ונתיב היונים יכול להתרחב.
גילוי מפתחות מולקולריים חזקים יותר
כדי להפוך תובנה זו לכלים שימושיים, הצוות סרק פאנל רחב של סטרואידים טבעיים ומעבדתיים וצורותיהם המראה-מראה (אננטיומרים). הם מצאו מספר מולקולות חדשות שמדליקות את Kir7.1, רבות בריכוזים נמוכים במיקרומטר או אפילו תת־מיקרומטר. אחת הבולטות, אננטיומר של התרופה 17‑hydroxyprogesterone caproate, נקשרה בחוזקה לאותו כיס הידרופובי שבדרך כלל מאכלס כולסטרול. במבנה עם המאקטב הזה נוצרה בין קצה הקוטבי של הסטרואיד וקבוצה צדדית תראונין מפתח קשר מימן צמוד, בעוד שהחלק השומני התמקם מול ההליקסים של התעלה. התאמה צמודה זו מסבירה את העוצמה שלו ואת יכולתו לשמר את פעילות התעלה אפילו בנוכחות חוסם סטנדרטי של Kir7.1.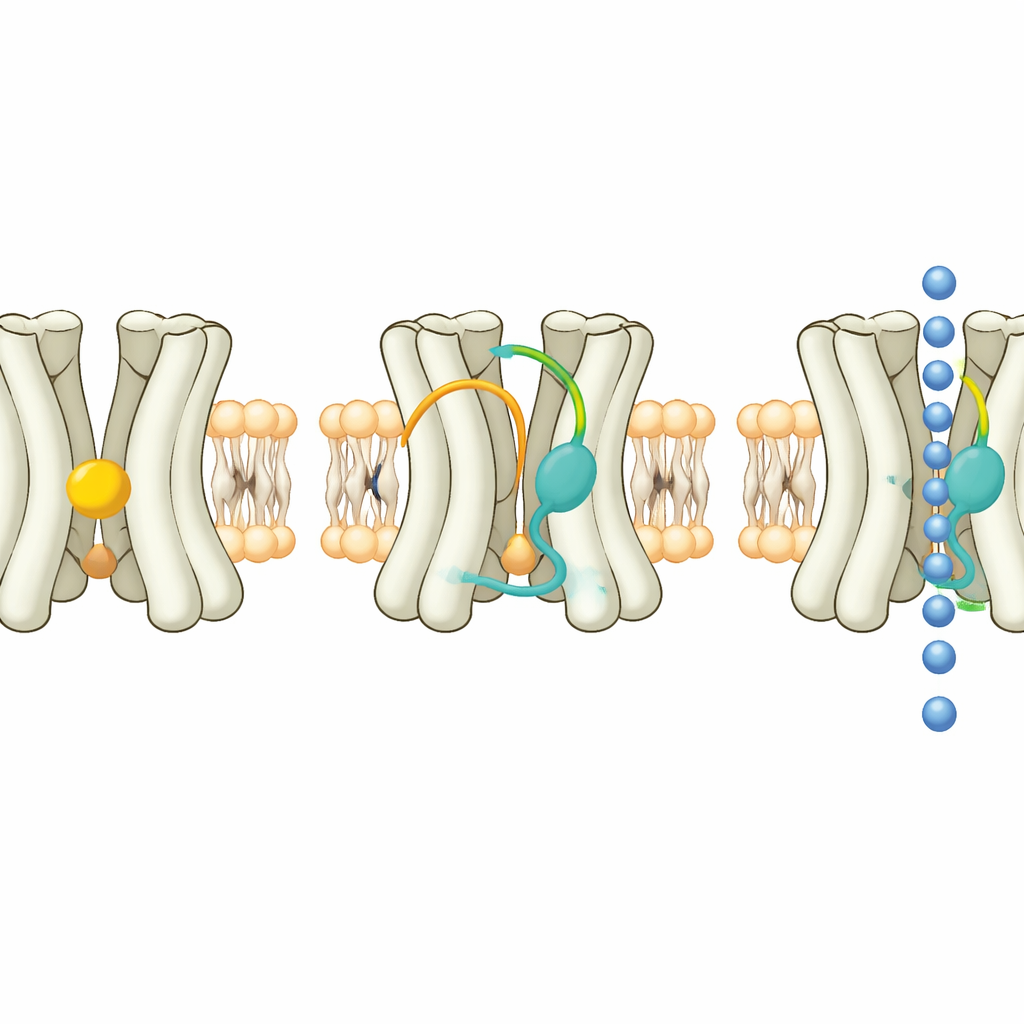
ממפת המבנה להבטחה טיפולית
ביחד, העבודה מראה ש־Kir7.1 נשלטת על ידי שותפות שיתופית בין PIP2, כולסטרול מעכב וסטרואידים בוחרים שמפעילים אותה. PIP2 מעגן ומארגן חלקית את התעלה; הכולסטרול מחזיק אותה במצב מוארך ופחות מוליך; וסטרואידים שמדירים את הכולסטרול מרפדים את ההליקסים ומאפשרים לתחום התאי לנוע לעבר מצב פתוח ויותר מוליך. על ידי פירוק אינטראקציות אלה אטום אחר אטום ותיאור כיצד שינויים כימיים קטנים משנים את עוצמת הסטרואידים, המחקר מציע שרטוט לתכנון תרופות חדשות שישחזרו או יכוונו במדויק את פעילות Kir7.1 במחלות של העין, המוח והרחם.
ציטוט: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
מילות מפתח: תעלת האשלגן Kir7.1, ויסות על ידי כולסטרול, מודולטורים סטרואידיים, מבנה קריו-אלקטרון-מיקרוסקופיה, אפיתל פיגמנטרי של הרשתית