Clear Sky Science · fr
Régulation structurelle et fonctionnelle du canal potassique humain essentiel Kir7.1 médiée par des lipides bioactifs
Pourquoi de minuscules portails dans nos cellules comptent
Enfouis dans les membranes de nombreuses cellules, des portails microscopiques laissent passer les ions potassium. L’un d’eux, appelé Kir7.1, est crucial pour une vision saine, le fonctionnement cérébral et même le déclenchement de l’accouchement. Lorsque ce portail est défaillant, des personnes peuvent devenir aveugles dès le jeune âge, et des animaux présentent des problèmes d’alimentation et de gestation. Cette étude révèle, au niveau atomique, comment des lipides naturels et des molécules de type hormonal se lient à Kir7.1 et font office d’interrupteurs marche–arrêt, ouvrant de nouvelles pistes pour la conception de médicaments.
Un portail spécial pour l’équilibre électrique
Kir7.1 appartient à une famille de canaux qui laissent généralement les ions potassium entrer plus facilement dans la cellule qu’en sortir, contribuant à établir l’équilibre électrique à travers la membrane. Dans l’épithélium pigmentaire rétinien de l’œil, Kir7.1 maintient l’environnement autour des cellules photoréceptrices stable ; sans lui, les photorécepteurs meurent progressivement et la vision décline. Kir7.1 façonne également des circuits nerveux qui contrôlent l’appétit et aide à maintenir l’utérus au repos pendant la grossesse. Ces rôles variés ont fait du canal une cible médicamenteuse attractive mais mal comprise, d’autant que ses régulateurs naturels, au-delà de quelques lipides membranaires connus, restaient mystérieux.
Voir le portail dans trois positions distinctes
Pour découvrir le fonctionnement de Kir7.1, les chercheurs ont produit de grandes quantités de la protéine humaine dans des cellules de mammifère, l’ont purifiée et l’ont imagée par cryo‑microscopie électronique haute résolution. Ils ont capturé le canal dans trois conformations principales. Dans l’état « étendu », la partie inférieure cytoplasmique du canal est plus éloignée de la membrane et le tunnel central pour les ions est long et relativement étroit, une conformation probablement non conductrice. Dans l’état « arrimé », ce domaine inférieur pivote et se déplace vers le haut en direction de la membrane, raccourcissant et élargissant légèrement le tunnel. Dans une troisième configuration, le canal est lié à un puissant stéroïde synthétique ainsi qu’à un lipide signal, le PIP2, produisant une conformation apparemment « amorcée » pour l’ouverture. Un petit changement sur un seul acide aminé près du filtre de sélectivité aide à expliquer pourquoi Kir7.1 peut conduire des ions césium, contrairement à la plupart des canaux apparentés.
Comment lipides et hormones partagent le contrôle
Les clichés structuraux ont montré que Kir7.1 porte en permanence une molécule de PIP2 à un site conservé où d’autres membres de la famille lient aussi ce lipide. Le PIP2 seul, toutefois, n’est pas suffisant pour ouvrir complètement Kir7.1. Une seconde poche, calée entre ses hélices transmembranaires, contient un autre type de lipide. À l’état étendu au repos, cette poche abrite le cholestérol, un stérol membranaire bien connu. Des expériences électrophysiologiques ont montré que l’ajout de cholestérol supplémentaire diminue les courants de Kir7.1, tandis que certains stéroïdes, dont l’hormone de grossesse progestérone et le neurostéroïde DHEA, les augmentent fortement. Les données soutiennent un modèle où le cholestérol joue le rôle d’un frein naturel : les stéroïdes activateurs doivent d’abord chasser le cholestérol de la poche, et lorsqu’ils le font en présence de PIP2, le domaine inférieur du canal peut pivoter et la voie ionique s’élargir.
Découvrir des clés moléculaires plus puissantes
Pour transformer cette connaissance en outils pratiques, l’équipe a testé un large panel de stéroïdes naturels et synthétiques et leurs énantiomères. Ils ont identifié plusieurs nouvelles molécules qui activent Kir7.1, beaucoup à des concentrations micromolaires faibles voire submicromolaires. Un candidat remarquable, un énantiomère du médicament 17‑hydroxyprogestérone caproate, se liait fortement dans la même poche hydrophobe qui accueille normalement le cholestérol. Dans la structure avec cet activateur présent, l’extrémité polaire du stéroïde formait une liaison hydrogène rapprochée avec une chaîne latérale de thréonine clé, tandis que son corps apolaire s’imbriquait contre les hélices du canal. Cet ajustement précis explique sa puissance et sa capacité à maintenir le canal actif même en présence d’un bloqueur standard de Kir7.1.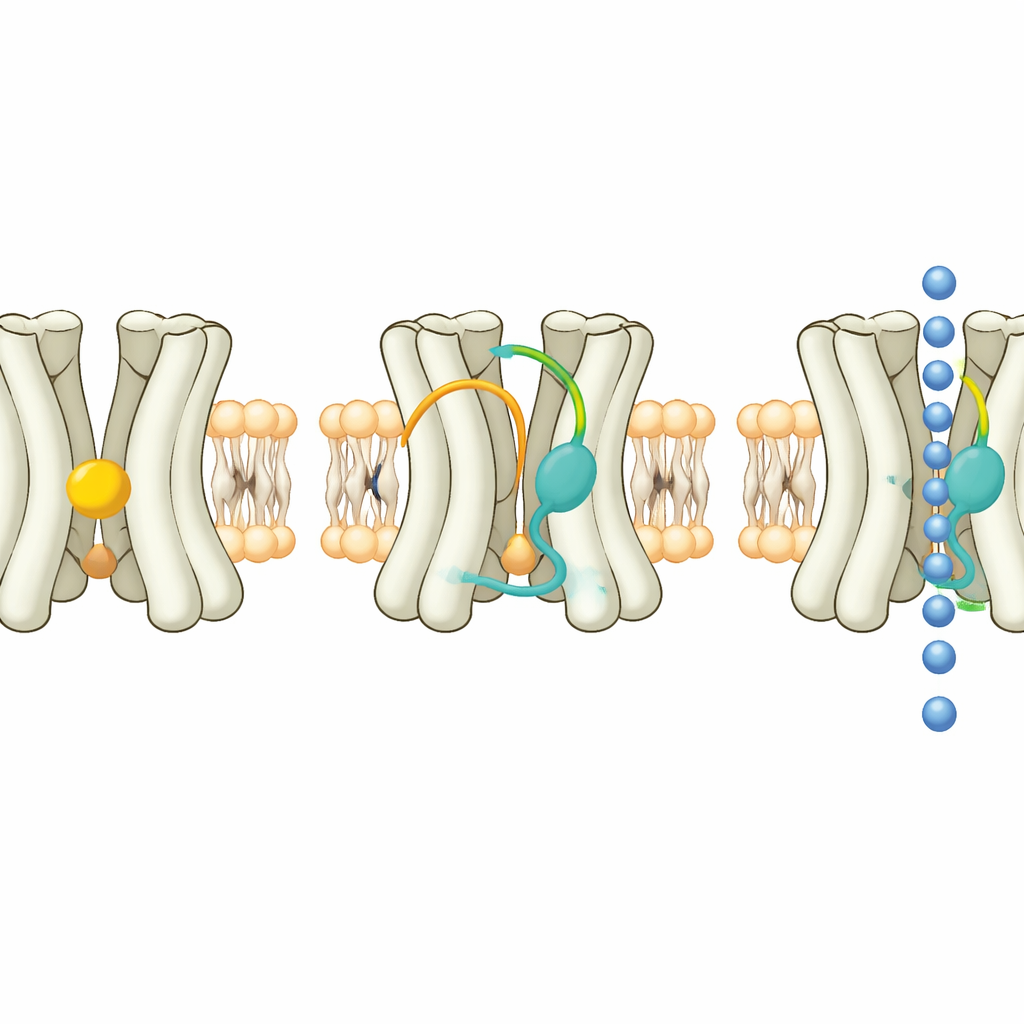
De la carte structurelle à la promesse thérapeutique
Ensemble, ces travaux montrent que Kir7.1 est gouverné par un partenariat coopératif entre le PIP2, le cholestérol inhibiteur et certains stéroïdes activateurs. Le PIP2 ancre et organise partiellement le canal ; le cholestérol le maintient dans une conformation étendue et moins conductrice ; et les stéroïdes qui expulsent le cholestérol desserrent les hélices et permettent au domaine inférieur de se déplacer vers un état plus ouvert et conducteur. En résolvant ces interactions atome par atome et en décrivant comment de petits ajustements chimiques modulent la puissance des stéroïdes, l’étude fournit une feuille de route pour concevoir de nouveaux médicaments visant à restaurer ou affiner l’activité de Kir7.1 dans les maladies de l’œil, du cerveau et de l’utérus.
Citation: Niu, Q., Vu, S., Xu, Y. et al. Bioactive lipid-mediated structural and functional regulation of the essential human potassium channel Kir7.1. Nat Commun 17, 2764 (2026). https://doi.org/10.1038/s41467-026-68819-0
Mots-clés: canal potassique Kir7.1, régulation par le cholestérol, modulateurs stéroïdiens, structure cryo-EM, épithélium pigmentaire rétinien